蛋白检测原理:食品中的蛋白在催化加热条件下被分解,产生的氨和硫酸结合产生硫酸铵。碱化蒸馏使氨游离,用硼酸吸收后以硫酸或者盐酸标准滴定溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质的含量。使用试剂:硫酸铜(CuSO4)、硫酸钾(K2SO4)、硫酸(H2SO4)、20g/L硼酸、混合指示剂、纯净水、甲基红指示液、40g/L氢氧化钠(NAOH)、0.02011mol/L盐酸滴定液(HCL)试剂配置:使用器材:2 2装置详介-|||-2-水蒸气发生器-|||-3 3一螺旋夹-|||-出水口 4一小漏斗及棒状 状玻塞-|||--8 6一反应室外层-|||-5一反应室-|||-进水口 8-冷凝管-|||-7一橡皮管及螺旋夹-|||-9-蒸馏液接收瓶检验步骤:步骤一:向①-1加入0.2g________、6g________、20ml________和10ml________________,摇匀(呈褐色)后倾斜(如图①放置)中火加热至内容物全部炭化(即泡沫停止),转大火加热到呈透明蓝绿色(称为________________),继续加热0.5~1小时,关火取下自然冷却。步骤二:将________移入100ml容量瓶、清洗①-1,洗液并入容量瓶,续水至100ml刻度,混匀(得________________)。步骤三:在②-2内加水至2/3处,加入数颗________防爆,加入数滴________及2~3毫升________,使用冷水令②-8形成冷凝循环,煮沸②-2。步骤四:以纯净水清洗②-4、5、6,控制②-3、7使洗液流出。步骤五:向②-9中加入10ml________及2滴混合指示液。(得黑蓝色液体)步骤六:通过②-4向②-5分别加入10ml________、10ml________,每次加液后清洗②-4,洗液并入②-5。最后往②-4中加适量水保留防漏气。注:②-5中液体总量不超过②-5总容积一半。如再添加上述试液时有液体从②-6中流出,清空②-5并清洗,重新添加各种试液。步骤七:继续加热②-1,开始蒸馏,②-8下端端口没入②-9液面蒸馏10分钟,再离开②-9液面蒸馏1分钟。(得浅蓝绿色液体)步骤八:使用________开始滴定②-9至浅红色,记录盐酸滴定液使用量V1。步骤九:计算试样中蛋白质的含量X(g/100g);(10÷100试样处理液稀释倍数)V2 ——试剂空白消耗盐酸滴定液的体积。(一般为0.05ml)C ——盐酸滴定液溶液浓度。0.0140——盐酸滴定液相当的氮的质量,单位g。m ——检测试样液的质量或者体积,单位为g或者ml。F ——氮换算为蛋白质的系数。一般食物6.25;花生5.46。
蛋白检测
原理:
食品中的蛋白在催化加热条件下被分解,产生的氨和硫酸结合产生硫酸铵。碱化蒸馏使氨游离,用硼酸吸收后以硫酸或者盐酸标准滴定溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质的含量。
使用试剂:
硫酸铜(CuSO4)、硫酸钾(K2SO4)、硫酸(H2SO4)、20g/L硼酸、混合指示剂、纯净水、甲基红指示液、40g/L氢氧化钠(NAOH)、0.02011mol/L盐酸滴定液(HCL)
试剂配置:
使用器材:
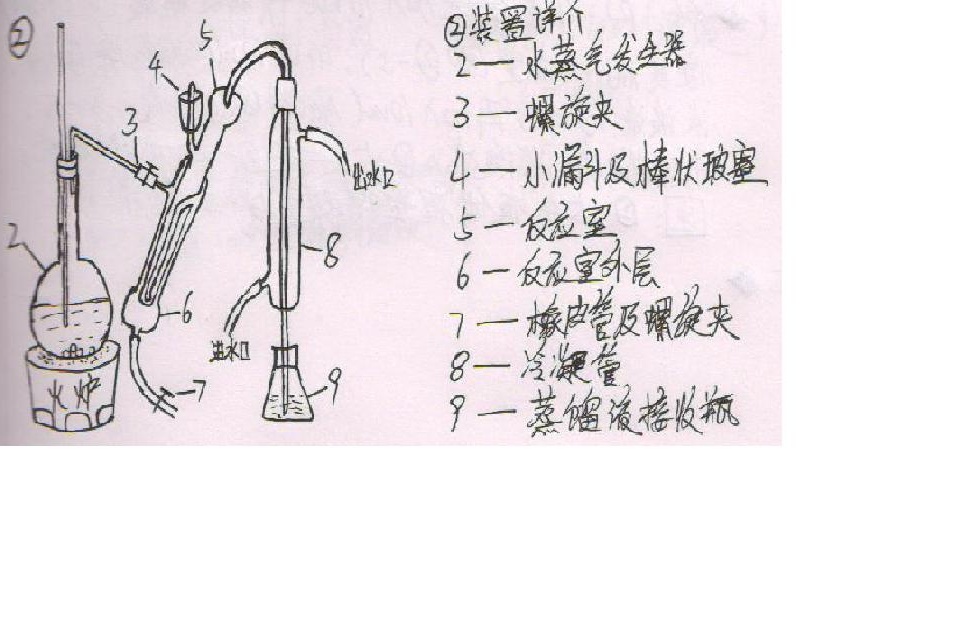
检验步骤:
步骤一:向①-1加入0.2g________、6g________、20ml________和10ml________________,摇匀(呈褐色)后倾斜(如图①放置)中火加热至内容物全部炭化(即泡沫停止),转大火加热到呈透明蓝绿色(称为________________),继续加热0.5~1小时,关火取下自然冷却。
步骤二:将________移入100ml容量瓶、清洗①-1,洗液并入容量瓶,续水至100ml刻度,混匀(得________________)。
步骤三:在②-2内加水至2/3处,加入数颗________防爆,加入数滴________及2~3毫升________,使用冷水令②-8形成冷凝循环,煮沸②-2。
步骤四:以纯净水清洗②-4、5、6,控制②-3、7使洗液流出。
步骤五:向②-9中加入10ml________及2滴混合指示液。(得黑蓝色液体)
步骤六:通过②-4向②-5分别加入10ml________、10ml________,每次加液后清洗②-4,洗液并入②-5。最后往②-4中加适量水保留防漏气。
注:②-5中液体总量不超过②-5总容积一半。如再添加上述试液时有液体从②-6中流出,清空②-5并清洗,重新添加各种试液。
步骤七:继续加热②-1,开始蒸馏,②-8下端端口没入②-9液面蒸馏10分钟,再离开②-9液面蒸馏1分钟。(得浅蓝绿色液体)
步骤八:使用________开始滴定②-9至浅红色,记录盐酸滴定液使用量V1。
步骤九:计算试样中蛋白质的含量X(g/100g)
;
(10÷100试样处理液稀释倍数)
V2 ——试剂空白消耗盐酸滴定液的体积。(一般为0.05ml)
C ——盐酸滴定液溶液浓度。
0.0140——盐酸滴定液相当的氮的质量,单位g。
m ——检测试样液的质量或者体积,单位为g或者ml。
F ——氮换算为蛋白质的系数。一般食物6.25;花生5.46。
题目解答
答案
硫酸铜 硫酸钾 硫酸 试样 s1 试样处理液 s2 s2 试样处理稀释液 s3 玻璃珠 甲基红指示液 硫酸 硼酸 s3 氢氧化钠 盐酸滴定液
解析
本题考查凯氏定氮法测定食品中蛋白质含量的实验步骤填空。关键在于掌握实验中各步骤所用试剂的作用及操作术语:
- 步骤一需加入催化剂(硫酸铜、硫酸钾)、酸化剂(硫酸)和试样,最终形成凯氏带(蓝绿色透明液体)。
- 步骤二将消化后的产物定容为试样处理液,稀释后为试样处理稀释液。
- 步骤三蒸馏前需加玻璃珠防暴沸,用甲基红指示液和硫酸调节环境。
- 步骤五、六通过硼酸吸收氨气,氢氧化钠碱化蒸馏,最后用盐酸滴定液滴定。
步骤一
- 硫酸铜(CuSO₄)和硫酸钾(K₂SO₄)作为催化剂,加速蛋白质分解。
- 硫酸(H₂SO₄)提供酸性环境,促进碳化和后续反应。
- 试样经加热炭化后,形成凯氏带(蓝绿色透明液体)。
步骤二
将消化后的液体转移并定容至100ml,得到试样处理液,稀释后为试样处理稀释液。
步骤三
- 玻璃珠防止液体暴沸。
- 甲基红指示液监测pH变化,硫酸维持酸性环境。
步骤五、六
- 硼酸吸收蒸馏出的氨气。
- 氢氧化钠(NaOH)碱化蒸馏液,使氨游离。
- 盐酸滴定液(HCl)用于滴定吸收的氨。
步骤八
用盐酸滴定液滴定至浅红色,记录体积计算蛋白质含量。