题目
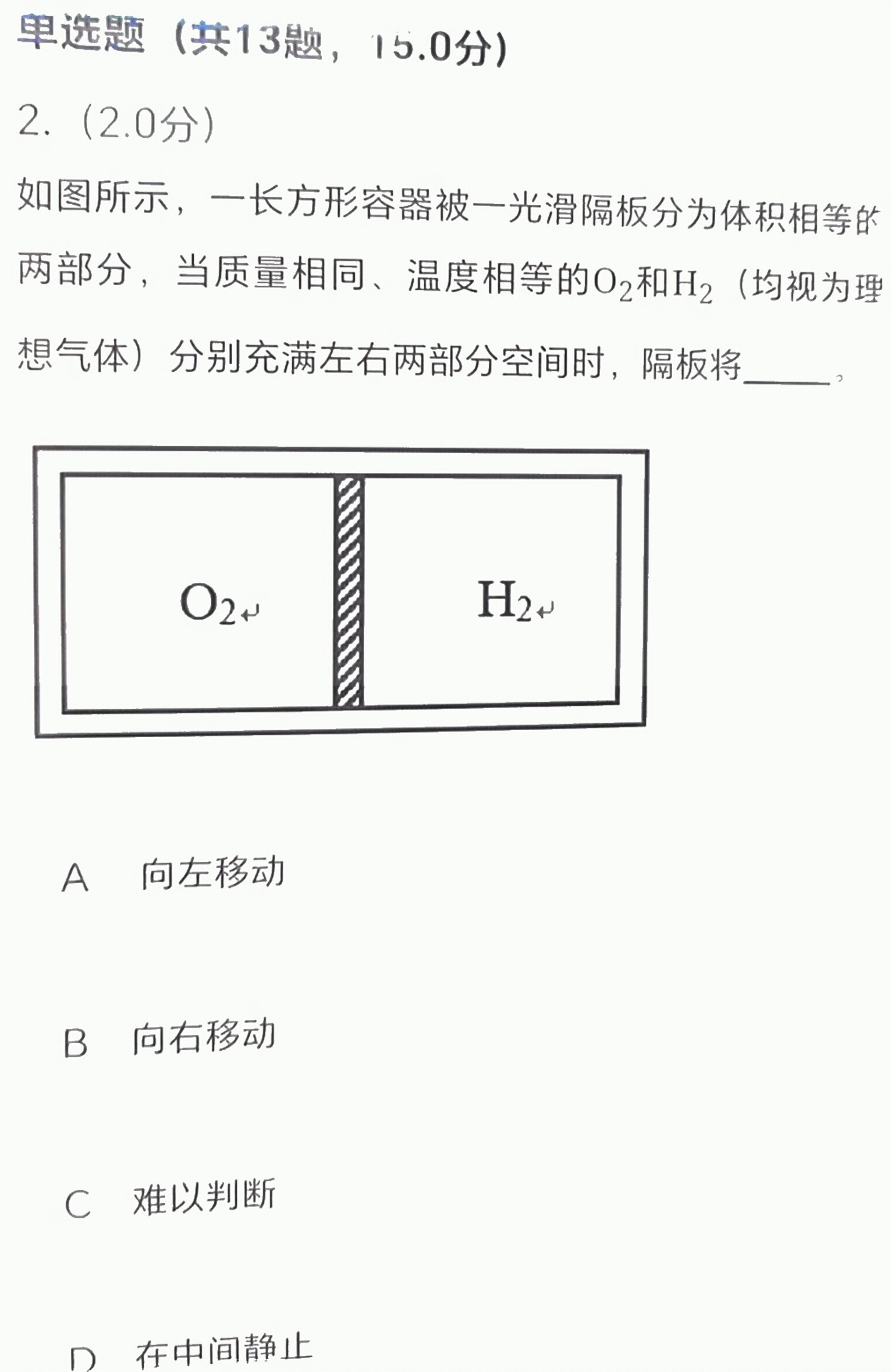
单选题(共13题,15.0分)-|||-2.(2.0分)-|||-如图所示,一长方形容器被一光滑隔板分为体积相等的-|||-两部分,当质量相同、温度相等的O2和H2(均视为理-|||-想气体)分别充满左右两部分空间时,隔板将 __-|||-O2 H2-|||-A 向左移动-|||-B 向右移动-|||-C 难以判断-|||-D 在中间静止
题目解答
答案
2.解析:根据理想气体状态方程,pV=nRT,可知,当质量相同、温度相等时,气体的物质的量与摩尔质量成反比,即n(O2):n(H2)=M(H2):M(O2)=2:32;所以根据PV=nRT可知,氧气的体积小于氢气体积,所以隔板应向左移动。
2.答案:A
2.答案:A
解析
步骤 1:理想气体状态方程
理想气体状态方程为 pV=nRT,其中 p 是气体的压强,V 是气体的体积,n 是气体的物质的量,R 是理想气体常数,T 是气体的温度。
步骤 2:物质的量与摩尔质量的关系
当质量相同、温度相等时,气体的物质的量与摩尔质量成反比,即 n(O2):n(H2)=M(H2):M(O2)=2:32。
步骤 3:体积与压强的关系
根据理想气体状态方程,当温度和物质的量相同时,气体的体积与压强成反比。由于氧气的物质的量小于氢气的物质的量,所以氧气的体积小于氢气的体积,因此氧气的压强大于氢气的压强。
步骤 4:隔板的移动方向
由于氧气的压强大于氢气的压强,隔板将受到更大的向左的力,因此隔板将向左移动。
理想气体状态方程为 pV=nRT,其中 p 是气体的压强,V 是气体的体积,n 是气体的物质的量,R 是理想气体常数,T 是气体的温度。
步骤 2:物质的量与摩尔质量的关系
当质量相同、温度相等时,气体的物质的量与摩尔质量成反比,即 n(O2):n(H2)=M(H2):M(O2)=2:32。
步骤 3:体积与压强的关系
根据理想气体状态方程,当温度和物质的量相同时,气体的体积与压强成反比。由于氧气的物质的量小于氢气的物质的量,所以氧气的体积小于氢气的体积,因此氧气的压强大于氢气的压强。
步骤 4:隔板的移动方向
由于氧气的压强大于氢气的压强,隔板将受到更大的向左的力,因此隔板将向左移动。