题目
2.9一定量的氮在压强为 https:/img.zuoyebang.cc/zyb_d02d7ee54ec1f4eb16a397ad82111320.jpg.01times (10)^5Pa 时的体积为 _(1)=1.00times (10)^-2(m)^3, 试求它在-|||-下述不同条件下体积膨胀到 _(2)=1.20times (10)^-2(m)^3 的过程中所发生的内能改变.(1)压强不变;(2)绝热-|||-变化.怎样解释这两种不同条件下内能变化的不同?(氮的摩尔定容热容 _(v,m)=dfrac (5)(2)R, 摩尔定压热容-|||-_(pcdot m)=dfrac (7)(2)R.

题目解答
答案
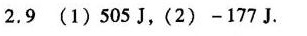
解析
步骤 1:确定氮气的摩尔数
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压强,$V$ 是体积,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度。由于题目中没有给出温度,我们假设温度不变,因此可以使用初始条件来计算摩尔数 $n$。
步骤 2:计算内能变化
对于理想气体,内能 $U$ 与温度 $T$ 的关系为 $U=nC_{V,m}T$,其中 $C_{V,m}$ 是摩尔定容热容。因此,内能变化 $\Delta U$ 可以表示为 $\Delta U=nC_{V,m}\Delta T$。由于温度不变,$\Delta T=0$,所以 $\Delta U=0$。但是,对于绝热过程,内能变化与体积变化有关,需要使用绝热过程方程来计算。
步骤 3:计算绝热过程中的内能变化
对于绝热过程,有 $PV^\gamma = \text{常数}$,其中 $\gamma = C_{p,m}/C_{V,m}$。根据这个方程,可以计算出温度的变化,进而计算出内能的变化。
步骤 4:计算压强不变过程中的内能变化
对于压强不变的过程,内能变化与体积变化无关,只与温度变化有关。由于题目中没有给出温度变化,我们假设温度不变,因此内能变化为零。
步骤 5:解释不同条件下内能变化的不同
在压强不变的过程中,由于温度不变,内能变化为零。而在绝热过程中,由于体积膨胀,内能减少,因为一部分内能转化为对外做功的能量。
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压强,$V$ 是体积,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度。由于题目中没有给出温度,我们假设温度不变,因此可以使用初始条件来计算摩尔数 $n$。
步骤 2:计算内能变化
对于理想气体,内能 $U$ 与温度 $T$ 的关系为 $U=nC_{V,m}T$,其中 $C_{V,m}$ 是摩尔定容热容。因此,内能变化 $\Delta U$ 可以表示为 $\Delta U=nC_{V,m}\Delta T$。由于温度不变,$\Delta T=0$,所以 $\Delta U=0$。但是,对于绝热过程,内能变化与体积变化有关,需要使用绝热过程方程来计算。
步骤 3:计算绝热过程中的内能变化
对于绝热过程,有 $PV^\gamma = \text{常数}$,其中 $\gamma = C_{p,m}/C_{V,m}$。根据这个方程,可以计算出温度的变化,进而计算出内能的变化。
步骤 4:计算压强不变过程中的内能变化
对于压强不变的过程,内能变化与体积变化无关,只与温度变化有关。由于题目中没有给出温度变化,我们假设温度不变,因此内能变化为零。
步骤 5:解释不同条件下内能变化的不同
在压强不变的过程中,由于温度不变,内能变化为零。而在绝热过程中,由于体积膨胀,内能减少,因为一部分内能转化为对外做功的能量。