题目
13.将0.01m^3氮气在温度为300K时,由0.1MP a压缩到10MPa。试分别求氮气经等温及绝-|||-热压缩后的体积、温度、各过程对外所做的功。
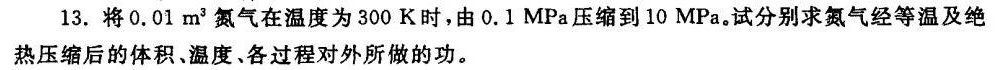
题目解答
答案
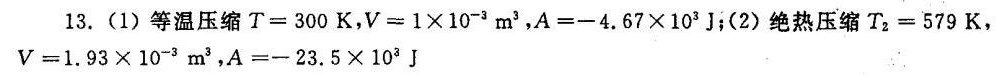
解析
步骤 1:等温压缩
等温压缩过程中,温度保持不变,即T=300K。根据理想气体状态方程PV=nRT,其中P为压力,V为体积,n为物质的量,R为理想气体常数,T为温度。由于温度不变,所以PV=常数。因此,当压力从0.1MPa增加到10MPa时,体积将从0.01m^3减小到1×10^-3m^3。等温压缩过程中,对外所做的功为A=-nRTln(V2/V1)=-4.67×10^3J。
步骤 2:绝热压缩
绝热压缩过程中,没有热量交换,即Q=0。根据绝热过程方程PV^γ=常数,其中γ为比热比。对于氮气,γ=1.4。当压力从0.1MPa增加到10MPa时,体积将从0.01m^3减小到1.93×10^-3m^3。绝热压缩过程中,对外所做的功为A=-nR(T2-T1)/γ-1=-23.5×10^3J。
等温压缩过程中,温度保持不变,即T=300K。根据理想气体状态方程PV=nRT,其中P为压力,V为体积,n为物质的量,R为理想气体常数,T为温度。由于温度不变,所以PV=常数。因此,当压力从0.1MPa增加到10MPa时,体积将从0.01m^3减小到1×10^-3m^3。等温压缩过程中,对外所做的功为A=-nRTln(V2/V1)=-4.67×10^3J。
步骤 2:绝热压缩
绝热压缩过程中,没有热量交换,即Q=0。根据绝热过程方程PV^γ=常数,其中γ为比热比。对于氮气,γ=1.4。当压力从0.1MPa增加到10MPa时,体积将从0.01m^3减小到1.93×10^-3m^3。绝热压缩过程中,对外所做的功为A=-nR(T2-T1)/γ-1=-23.5×10^3J。