题目
一定量的理想气体,从a态出发经过①或②过程到达b态,acb为等温线(如图),则①、②两过程中外界对系统传递的热量Q1、Q2是( )p-|||-a ①-|||-C-|||-② bA.Q1>0,Q2>0B.Q1<0,Q2<0C.Q1>0,Q2<0D.Q1<0,Q2>0
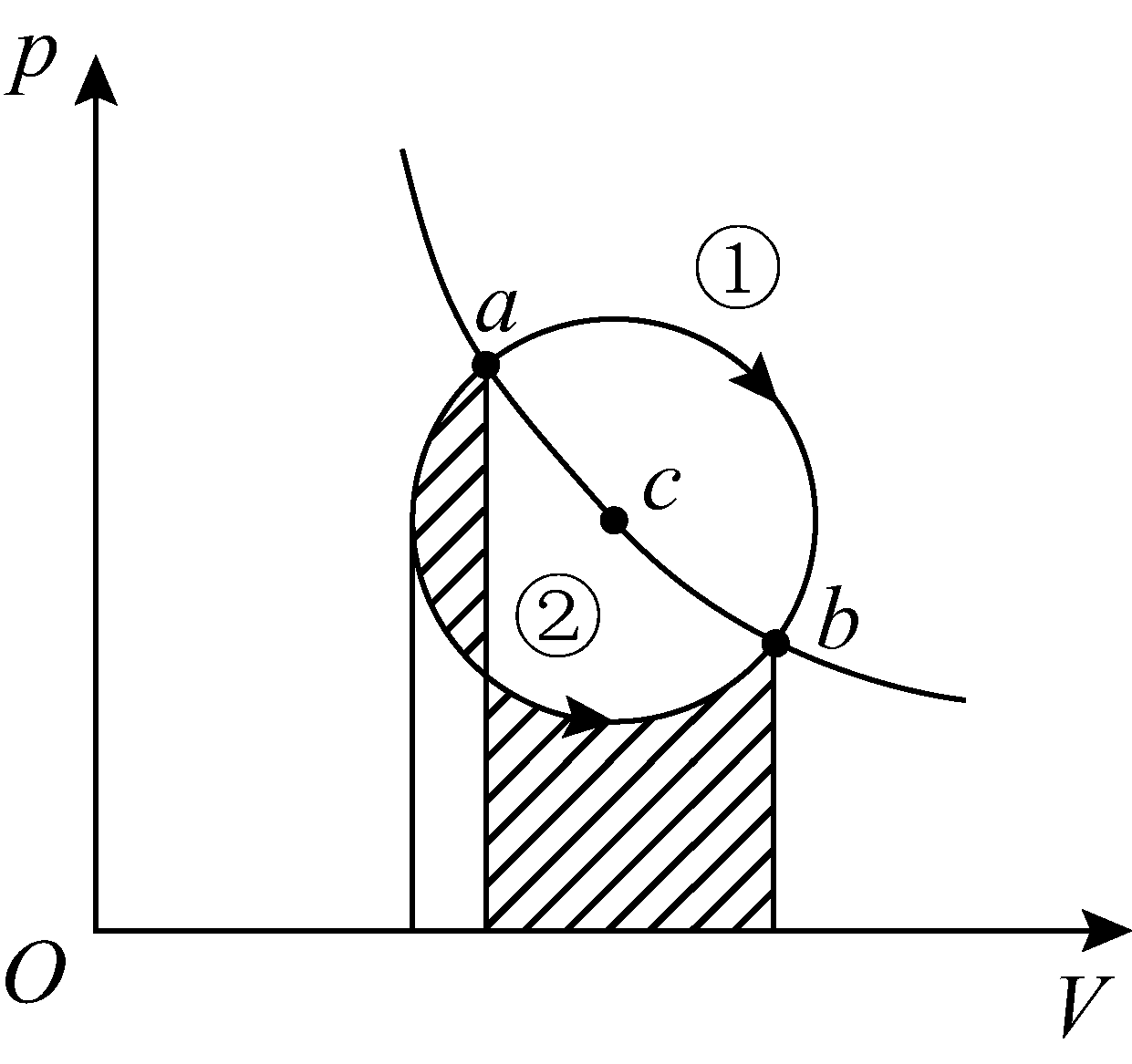
一定量的理想气体,从a态出发经过①或②过程到达b态,acb为等温线(如图),则①、②两过程中外界对系统传递的热量Q1、Q2是( )
- A.Q1>0,Q2>0
- B.Q1<0,Q2<0
- C.Q1>0,Q2<0
- D.Q1<0,Q2>0
题目解答
答案
A
解析
步骤 1:分析过程①
过程①是从a态到b态,沿着acb等温线进行。根据热力学第一定律,对于理想气体,内能只与温度有关。由于acb为等温线,所以过程①中气体的内能不变,即ΔU=0。根据热力学第一定律,Q=W+ΔU,所以Q=W。由于过程①中气体体积减小,外界对气体做正功,即W>0,所以Q1>0。
步骤 2:分析过程②
过程②是从a态到b态,沿着a到b的直线进行。由于acb为等温线,而过程②不是等温过程,所以过程②中气体的内能变化ΔU≠0。根据热力学第一定律,Q=W+ΔU。由于过程②中气体体积减小,外界对气体做正功,即W>0。由于过程②不是等温过程,所以ΔU≠0。由于过程②中气体的温度降低,所以ΔU<0。因此,Q2=W+ΔU>0+ΔU>0,即Q2>0。
步骤 3:总结
根据步骤1和步骤2的分析,可以得出结论:Q1>0,Q2>0。
过程①是从a态到b态,沿着acb等温线进行。根据热力学第一定律,对于理想气体,内能只与温度有关。由于acb为等温线,所以过程①中气体的内能不变,即ΔU=0。根据热力学第一定律,Q=W+ΔU,所以Q=W。由于过程①中气体体积减小,外界对气体做正功,即W>0,所以Q1>0。
步骤 2:分析过程②
过程②是从a态到b态,沿着a到b的直线进行。由于acb为等温线,而过程②不是等温过程,所以过程②中气体的内能变化ΔU≠0。根据热力学第一定律,Q=W+ΔU。由于过程②中气体体积减小,外界对气体做正功,即W>0。由于过程②不是等温过程,所以ΔU≠0。由于过程②中气体的温度降低,所以ΔU<0。因此,Q2=W+ΔU>0+ΔU>0,即Q2>0。
步骤 3:总结
根据步骤1和步骤2的分析,可以得出结论:Q1>0,Q2>0。