题目
13-14 一压强为 https:/img.zuoyebang.cc/zyb_24c102e246cf63b4c1c04e5b55e5236f.jpg.0times (10)^5Pa, 体积为 https:/img.zuoyebang.cc/zyb_24c102e246cf63b4c1c04e5b55e5236f.jpg.0times (10)^-3(m)^3 的氧气自 习题 13-13 图-|||-0℃加热到100℃,问:(1)当压强不变时,需要多少热量?当体积不变时,需要多少热量?-|||-(2)在等压或等容过程中各做了多少功?

题目解答
答案
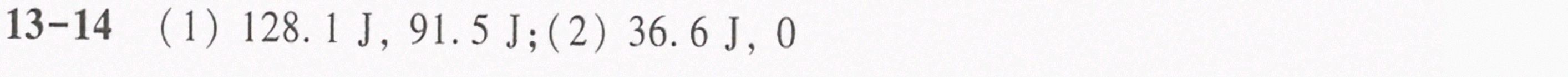
解析
步骤 1:计算氧气的摩尔数
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压强,$V$ 是体积,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是绝对温度。已知 $P=1.0\times {10}^{5}Pa$,$V=1.0\times {10}^{-3}{m}^{3}$,$T=273K$(0℃),$R=8.31J/(mol\cdot K)$,可以计算出摩尔数 $n$。
步骤 2:计算等压过程中的热量
等压过程中的热量 $Q_p$ 可以用公式 $Q_p=nC_p\Delta T$ 计算,其中 $C_p$ 是摩尔定压热容,对于氧气,$C_p=29.1J/(mol\cdot K)$,$\Delta T$ 是温度变化量,从0℃到100℃,即 $\Delta T=100K$。
步骤 3:计算等容过程中的热量
等容过程中的热量 $Q_v$ 可以用公式 $Q_v=nC_v\Delta T$ 计算,其中 $C_v$ 是摩尔定容热容,对于氧气,$C_v=20.8J/(mol\cdot K)$,$\Delta T$ 是温度变化量,从0℃到100℃,即 $\Delta T=100K$。
步骤 4:计算等压过程中的功
等压过程中的功 $W_p$ 可以用公式 $W_p=nR\Delta T$ 计算,其中 $R$ 是理想气体常数,$\Delta T$ 是温度变化量,从0℃到100℃,即 $\Delta T=100K$。
步骤 5:计算等容过程中的功
等容过程中的功 $W_v$ 为0,因为体积不变,没有对外做功。
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压强,$V$ 是体积,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是绝对温度。已知 $P=1.0\times {10}^{5}Pa$,$V=1.0\times {10}^{-3}{m}^{3}$,$T=273K$(0℃),$R=8.31J/(mol\cdot K)$,可以计算出摩尔数 $n$。
步骤 2:计算等压过程中的热量
等压过程中的热量 $Q_p$ 可以用公式 $Q_p=nC_p\Delta T$ 计算,其中 $C_p$ 是摩尔定压热容,对于氧气,$C_p=29.1J/(mol\cdot K)$,$\Delta T$ 是温度变化量,从0℃到100℃,即 $\Delta T=100K$。
步骤 3:计算等容过程中的热量
等容过程中的热量 $Q_v$ 可以用公式 $Q_v=nC_v\Delta T$ 计算,其中 $C_v$ 是摩尔定容热容,对于氧气,$C_v=20.8J/(mol\cdot K)$,$\Delta T$ 是温度变化量,从0℃到100℃,即 $\Delta T=100K$。
步骤 4:计算等压过程中的功
等压过程中的功 $W_p$ 可以用公式 $W_p=nR\Delta T$ 计算,其中 $R$ 是理想气体常数,$\Delta T$ 是温度变化量,从0℃到100℃,即 $\Delta T=100K$。
步骤 5:计算等容过程中的功
等容过程中的功 $W_v$ 为0,因为体积不变,没有对外做功。