题目
16.14 将1 kg 氦气和Mkg氢气混合,平衡后混合气体的内能是 .45times (10)^6J, 氦分子平均动能是-|||-times (10)^-21J, 求氢气质量M.

题目解答
答案
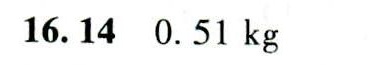
解析
步骤 1:计算氦气的摩尔数
氦气的摩尔质量为 $4g/mol$,所以1 kg氦气的摩尔数为 $n_{He} = \frac{1000g}{4g/mol} = 250mol$。
步骤 2:计算氦气的内能
氦气是单原子分子,其内能为 $U_{He} = \frac{3}{2}n_{He}RT$。由于题目给出氦分子的平均动能为 $6\times {10}^{-21}J$,而单原子分子的平均动能为 $\frac{3}{2}kT$,其中 $k$ 是玻尔兹曼常数,$T$ 是温度。因此,氦气的内能也可以表示为 $U_{He} = n_{He} \times 2 \times 6\times {10}^{-21}J$。
步骤 3:计算氢气的内能
氢气是双原子分子,其内能为 $U_{H_2} = \frac{5}{2}n_{H_2}RT$。由于氢气的摩尔数为 $n_{H_2} = \frac{M}{2g/mol}$,所以氢气的内能也可以表示为 $U_{H_2} = \frac{5}{2} \times \frac{M}{2g/mol} \times RT$。
步骤 4:计算混合气体的内能
混合气体的内能为 $U_{total} = U_{He} + U_{H_2} = 2.45\times {10}^{6}J$。
步骤 5:求解氢气质量M
将步骤 2 和步骤 3 中的内能表达式代入步骤 4 中的内能表达式,解出氢气质量M。
氦气的摩尔质量为 $4g/mol$,所以1 kg氦气的摩尔数为 $n_{He} = \frac{1000g}{4g/mol} = 250mol$。
步骤 2:计算氦气的内能
氦气是单原子分子,其内能为 $U_{He} = \frac{3}{2}n_{He}RT$。由于题目给出氦分子的平均动能为 $6\times {10}^{-21}J$,而单原子分子的平均动能为 $\frac{3}{2}kT$,其中 $k$ 是玻尔兹曼常数,$T$ 是温度。因此,氦气的内能也可以表示为 $U_{He} = n_{He} \times 2 \times 6\times {10}^{-21}J$。
步骤 3:计算氢气的内能
氢气是双原子分子,其内能为 $U_{H_2} = \frac{5}{2}n_{H_2}RT$。由于氢气的摩尔数为 $n_{H_2} = \frac{M}{2g/mol}$,所以氢气的内能也可以表示为 $U_{H_2} = \frac{5}{2} \times \frac{M}{2g/mol} \times RT$。
步骤 4:计算混合气体的内能
混合气体的内能为 $U_{total} = U_{He} + U_{H_2} = 2.45\times {10}^{6}J$。
步骤 5:求解氢气质量M
将步骤 2 和步骤 3 中的内能表达式代入步骤 4 中的内能表达式,解出氢气质量M。