如图所示,一定量的理想气体,沿着图中直线从状态a(压强(p)_(1)=4atm,体积(V)_(1)=2L)变到状态b(压强(p)_(2)=2atm,体积(V)_(2)=4L)则在此过程中( )(a(m)-|||-4-|||-1-|||-3 1-|||-1-|||-2 b-|||-1 、 1 (1-|||-1-|||-0 1 2 3 4(A)气体对外作正功,向外界放出热量。(B)气体对外作正功,从外界吸热。(C)气体对外作负功,向外界放出热量。(D)气体对外作正功,内能减少。
如图所示,一定量的理想气体,沿着图中直线从状态a(压强${p}_{1}=4atm$,体积${V}_{1}=2L$)变到状态b(压强${p}_{2}=2atm$,体积${V}_{2}=4L$)则在此过程中( )
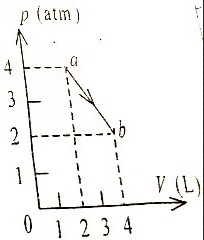
(A)气体对外作正功,向外界放出热量。
(B)气体对外作正功,从外界吸热。
(C)气体对外作负功,向外界放出热量。
(D)气体对外作正功,内能减少。
题目解答
答案
【解析】:
由于初状态压强${p}_{1}=4atm$,体积${V}_{1}=2L$,末状态压强${p}_{2}=2atm$,体积${V}_{2}=4L$,则${p}_{1}{V}_{1}={p}_{2}{V}_{2}$,所以此过程中温度不变,内能不变,状态a变到状态b过程中,体积增大,气体对外作正功,根据$\triangle U=Q+W$可知,气体从外界吸热,故B正确,ACD错误.
故本题选:B
解析
考查要点:本题主要考查理想气体状态方程的应用、热力学第一定律的理解,以及p-V图中气体做功的判断。
解题核心思路:
- 判断温度变化:通过比较初末状态的$pV$乘积,确定温度是否变化,从而得出内能变化。
- 分析做功情况:根据体积变化判断气体对外做功的正负。
- 应用热力学第一定律:结合内能变化和做功情况,推断吸放热情况。
破题关键点:
- 温度不变:若$p_1V_1 = p_2V_2$,则温度不变,内能$\Delta U = 0$。
- 对外做正功:体积增大时,气体对外做正功。
- 吸热判断:由$\Delta U = Q + W$($W$为外界对气体做的功),若$\Delta U = 0$且$W < 0$(气体对外做功),则$Q > 0$,即气体吸热。
步骤1:判断温度变化
根据理想气体状态方程$PV = nRT$,若$p_1V_1 = p_2V_2$,则温度$T$不变。计算得:
$p_1V_1 = 4 \, \text{atm} \times 2 \, \text{L} = 8 \, \text{L·atm}, \quad p_2V_2 = 2 \, \text{atm} \times 4 \, \text{L} = 8 \, \text{L·atm}$
因此,温度不变,内能$\Delta U = 0$。
步骤2:分析做功情况
气体体积从$V_1 = 2 \, \text{L}$增加到$V_2 = 4 \, \text{L}$,体积增大,说明气体对外做正功。
步骤3:应用热力学第一定律
热力学第一定律为$\Delta U = Q + W$($W$为外界对气体做的功)。由于$\Delta U = 0$且气体对外做功($W < 0$),代入得:
$0 = Q + W \quad \Rightarrow \quad Q = -W$
因$W < 0$,故$Q > 0$,即气体从外界吸热。