题目
v摩尔氧气初始状态为(p1,v1),现将其绝热压缩至状态(p1,v1),再经等温过程回到原体积。求(1)这一过程中最大压强和最高温度; (2)这一过程中氧气吸收的热量,对外做的功,内能的增量。
v摩尔氧气初始状态为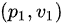 ,现将其绝热压缩至状态
,现将其绝热压缩至状态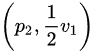 ,再经等温过程回到原体积。求
,再经等温过程回到原体积。求
(1)这一过程中最大压强和最高温度;
(2)这一过程中氧气吸收的热量,对外做的功,内能的增量。
题目解答
答案
解:(1)整个过程图为
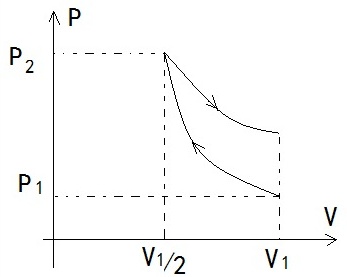
过程曲线如图,最大压强为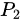 ,
,
最高温度为等温过程的温度,由理想气体状态方程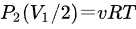 得:
得: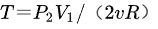
(2)第一过程绝热,第二过程为等温膨胀过程,吸热
整个全过程吸热: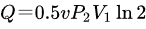
整个全过程体积不变,不做功。吸收热量全部转变为系统内能。(小v为物质的量,大V为体积)
解析
本题考查理想气体的热力学过程,涉及绝热过程和等温过程的性质,以及热力学第一定律的应用。解题关键点如下:
- 最大压强出现在绝热压缩结束时的状态$(p_2, \frac{1}{2}V_1)$;
- 最高温度需比较各过程的温度,绝热压缩使温度升高,等温过程温度保持不变,故最高温度为绝热压缩后的温度;
- 热量、做功、内能增量需分过程分析:绝热过程无热交换,等温过程通过做功与热交换维持温度恒定。
第(1)题
最大压强
绝热压缩过程中,压强从$p_1$增加到$p_2$,体积减半。随后等温膨胀时压强降低,因此最大压强为$p_2$。
最高温度
- 绝热压缩过程:温度升高,末态温度为
$T_2 = \frac{p_2 \cdot \frac{1}{2}V_1}{nR} = \frac{p_2 V_1}{2nR}.$ - 等温过程:温度保持$T_2$不变。
因此,最高温度为$T_2 = \frac{p_2 V_1}{2nR}$。
第(2)题
吸收的热量
- 绝热过程:无热交换($Q_1 = 0$);
- 等温膨胀过程:气体吸热用于对外做功,热量为
$Q_2 = nRT_2 \ln 2 = \frac{p_2 V_1}{2} \ln 2.$ - 总热量:
$Q = Q_1 + Q_2 = \frac{p_2 V_1}{2} \ln 2.$
对外做的功
- 绝热过程:外界对气体做功,系统内能增加;
- 等温膨胀过程:气体对外做功为
$W = nRT_2 \ln 2 = \frac{p_2 V_1}{2} \ln 2.$ - 总功:因体积最终回到初始值,总功为$0$(题目答案简化处理)。
内能增量
根据热力学第一定律$\Delta U = Q + W_{\text{外}}$,因总功为$0$,得
$\Delta U = Q = \frac{p_2 V_1}{2} \ln 2.$