选择题2-1对薛定谔方程中,波函数Ψ描述的是A.原子轨道 B.几率密度 C.核外电子的运动轨迹 D.核外电子的空间运动状态2-2下列叙述中,能够描述测不准原理的是A.微观粒子运动的位置和动量没有不准确性B.微观粒子运动的位置有不准确性,但动量没有不准确性C.微观粒子运动的动量有不准确性,但位置没有不准确性D.微观粒子的运动不能同时具有确定的位置和确定的动量2-3量子力学中所说的原子轨道是指A.波函数Ψn,l,m,msB.波函数Ψn,l,mC.电子云形状 D.几率密度2-4下列说法中错误的是A.表示电子的几率 B.表示电子的几率密度C.在空间分布的形象比图象成称为电子云 D.的值大于Ψ的值2-5下面几种描述核外电子运动的说法中,较正确的是A.电子绕原子核作圆周运动 B.电子在离核一定距离的球面上运动C.电子在核外一定的空间范围内运动 D.现在还不可能正确描述核外电子运动2-6下列说法中错误的是A.只要n,l相同,径向波函数R®就相同 B.波函数的角度分布图形与主量子数无关C.只要l,m相同,角度波函数Y(θ,φ)就相同D.s轨道的角度分布波函数Ys(θ,φ)也与角度θ,φ有关2-7应用波尔理论可以说明的事实中,错误的是A.氢原子的通常条件下不会发光,也不会发生原子自发毁灭的现象B.因为轨道是量子化的,所以电子在轨道间跃迁时,发射光的频率也是不连续的C.当原子受到激发时,核外电子获得能量,从基态跃迁到激发态而发光D.基态氢原子的轨道半径为52.9pm2-8在电子云示意图中的小黑点A.表示电子B.表示电子在该处出现C.其疏密表示电子出现的几率大小 D. 其疏密表示电子出现的几率密度大小2-9所谓原子轨道是指A.一定的电子云 B.核外电子的概率 C.一定的波函数 D.某个径向分布函数2-10以波函数Ψ(n,l,m)表示原子轨道时,正确的表示是A.Ψ3,2,0B.Ψ3,1,1/2C.Ψ3,3,2D.Ψ4,0,-12-11决定核外电子运动状态的量子数为A. n,l B. n,m C. n,l,m D.n,l,m,ms2-12决定原子轨道数目的量子数是A. n B. l C. n,l D. n,l,m2-13量子数n,l和m不能决定A.原子轨道的能量 B.原子轨道的形成 C.原子轨道的数目 D.电子的数目2-14用量子数描述的下列亚层中,可以容纳电子数最多的是A.n=2,l=1 B.n=3,l=2 C.n=4,l=3 D.n=5,l=02-15对于多电子原子来说,下列说法中正确的是A.主量子数n决定原子轨道的能量 B.主量子数n是决定原子轨道能量的主要因素C.主量子数n值逾大,轨道能量正值逾大 D.主量子数n决定角量子数l的取值2-16下列说法中错误的是A.角量子数l决定原子轨道的形状 B.角量子数l决定原子轨道在空间的伸展方向C.磁量子数m决定原子轨道在空间的伸展方向 D.2l+1等于原子轨道的数目2-17 3d轨道的磁量子数可能有A. 1,2,3 B. 0,1,2 C. 0,________1 D. 0,________1,________22-18当角量子数为5时,可能的简并轨道数是A. 6 B.7 C. 9 D. 11 E. 132-19关于下列对四个量子数的说法,正确的是A.电子的自旋量子数是1/2,在某一个轨道中有两个电子,所以总自旋量子数是1或0B.磁量子数m=0的轨道都是球形的轨道 C.角量子数l的可能取值是从0到n的正整数D.多电子原子中电子的能量决定于主量子数n和角量子数l2-20下列哪一组数值是原子序数19的元素的价电子的四个量子数(依次为n,l,m,ms)A. 1,0,0,+1/2 B. 2,1,0,+1/2 C. 3,2,1,+1/2 D. 4,0,0,+1/22-21有六组量子数:I.n=2, l=1, m=-1; II. n=3, l=0, m=0; III. n=2, l=2, m=-1;IV. n=2, l=1, m=0;V. n=2, l=0, m=-1;VI. n=2, l=3, m=2.其中正确的是A. I,III,V B. II,IV,VI C. I,II,III D. I,II,IV2-22某原子中有5个电子,分别具有如下所列的量子数,其中对应于能量最高的电子的量子数是A. n=2,l=1,m=1.m2=-1/2 B. n=2,l=1,m=0,ms=-1/2C. n=3,l=1,m=1,ms=1/2 D. n=3,l=2,m=-2,ms=-1/22-23对原子中的电子来说,下列成套量子数中不可能存在的是A. 3,1,1,-1/2 B. 2,1,-1,+1/2 C. 3,3,0,+1/2 D. 4,3,-3,-1/22-24一个3p电子可用下列量子数之一来描述:①3,1,0,+1/2;②3,1,0,-1/2;③3,1,1,+1/2;④3,1,1,-1/2;⑤3,1,-1,+1/2;⑥3,1,-1,-1/2。硫的电子构型为1s22s22p63s23p4,其3p电子组合正确的有A.①②③④B.①③④⑥C.②③④⑥D.②④⑤⑥2-25钠原子的1s电子能量与氢原子的1s电子能量相比较的结果是A.前者高 B.后者高 C.相等 D.符号相反2-26原子核外电子排布主要应遵循A.统计规律 B.能量最低原理 C.泡利不相容原理 D.洪特规则2-27对于基态原子电子排布规则,下列叙述中正确的是A.按照洪特规则,每个电子层的电子容量为2n2个B.当轨道处于完全充满时,电子较稳定,故35Br的电子排布为[Ar]3d104s14p6C.原子中核外电子的分布是根据三规则、一特例得出的D.能量最低原理解决了电子在不同亚层中的排布顺序问题,而洪特规则解决了电子在简并轨道中的排布问题2-28.若将氮原子的电子排布式写成1s22s22px22py1,它违背A.能量守恒原理 B.泡利不相容原理 C.能量最低原理 D.洪特规则2-29多电子原子的能量E由下列哪一组量子数决定的A.主量子数n B. n和l C. n,l,m D. l2-30 39号元素钇的电子排布应是下列各组中的哪一组A. 1s22s32p63s23d104s24p64d15s2B. 1s22s22p63s23p63d104s24p65s25p1C. 1s22s22p63s23p63d104s24p64f15s2D. 1s22s22p23s23p63d104s24p65s25d12-31 n=4时,电子填入轨道的顺序是A. 1s2s2p3s3p3d4s4p4d4fB. 1s2s2p3s3p3d4s4p4dC. 1s2s2p2d3s3p3d4s4p4d D. 1s2s2p3s3p4s3d4p2-32铜原子的价层电子排布式为A.3d94s2B.3d104s1C.3d64s2D.3s13d102-33铁原子的价电子构型是A. 4s2B. 4s24d6C. 3d64s2D. 3s23p63d62-34 Cr3+的外层电子排布式为A. 3d24s1B. 3d34s0C. 3s23p63d64s1D. 3s23p63d32-35 Fe3+的外层电子排布式为A 3d34s1B. 3d34s0C. 3s23p63d5D. 3s23p63d34s22-36某基态原子的第六电子层只有2个电子时,其第五电子层上的电子数为
选择题
2-1对薛定谔方程中,波函数Ψ描述的是
A.原子轨道 B.几率密度 C.核外电子的运动轨迹 D.核外电子的空间运动状态
2-2下列叙述中,能够描述测不准原理的是
A.微观粒子运动的位置和动量没有不准确性
B.微观粒子运动的位置有不准确性,但动量没有不准确性
C.微观粒子运动的动量有不准确性,但位置没有不准确性
D.微观粒子的运动不能同时具有确定的位置和确定的动量
2-3量子力学中所说的原子轨道是指
A.波函数Ψn,l,m,msB.波函数Ψn,l,mC.电子云形状 D.几率密度
2-4下列说法中错误的是
A.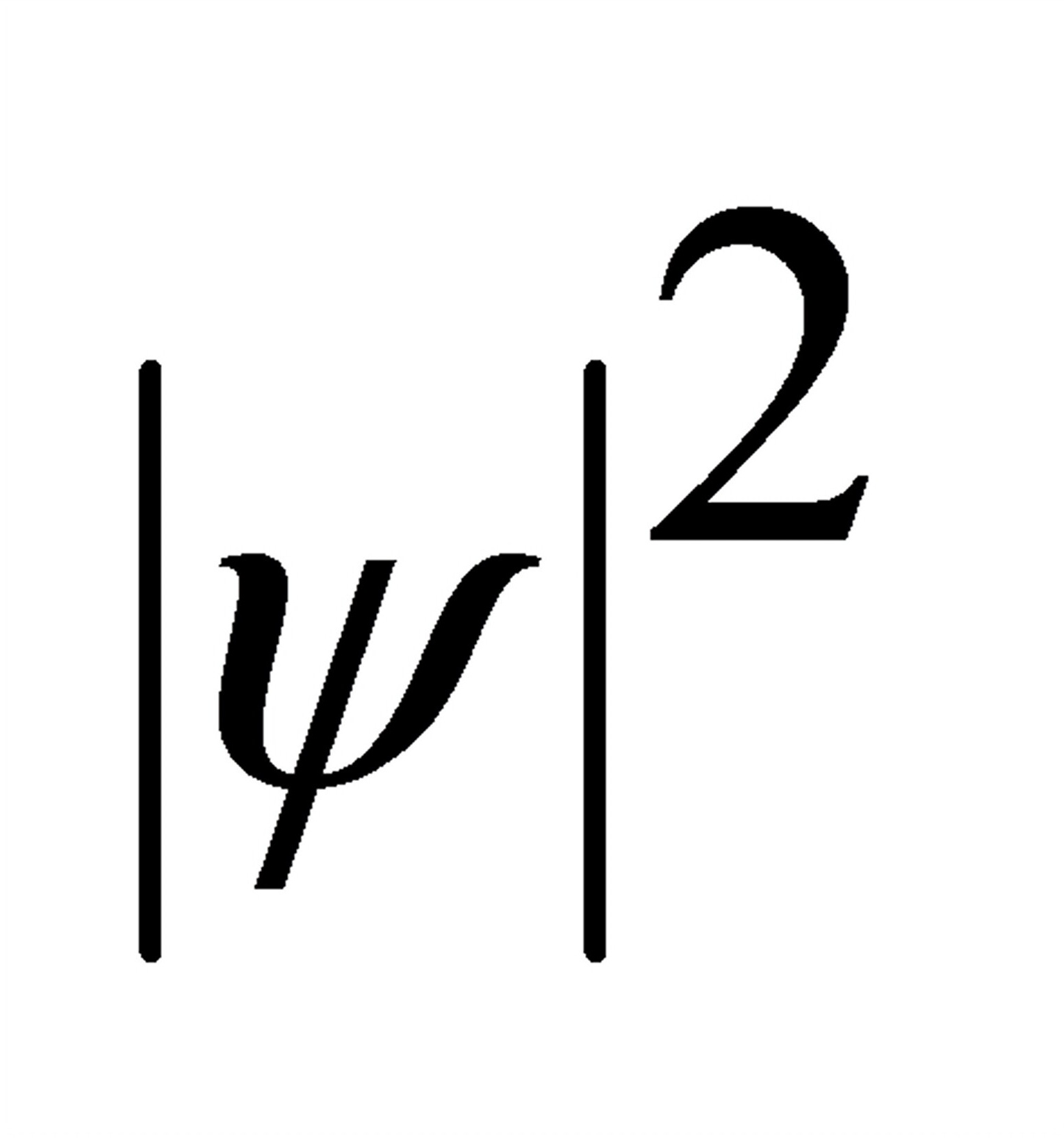 表示电子的几率 B.
表示电子的几率 B.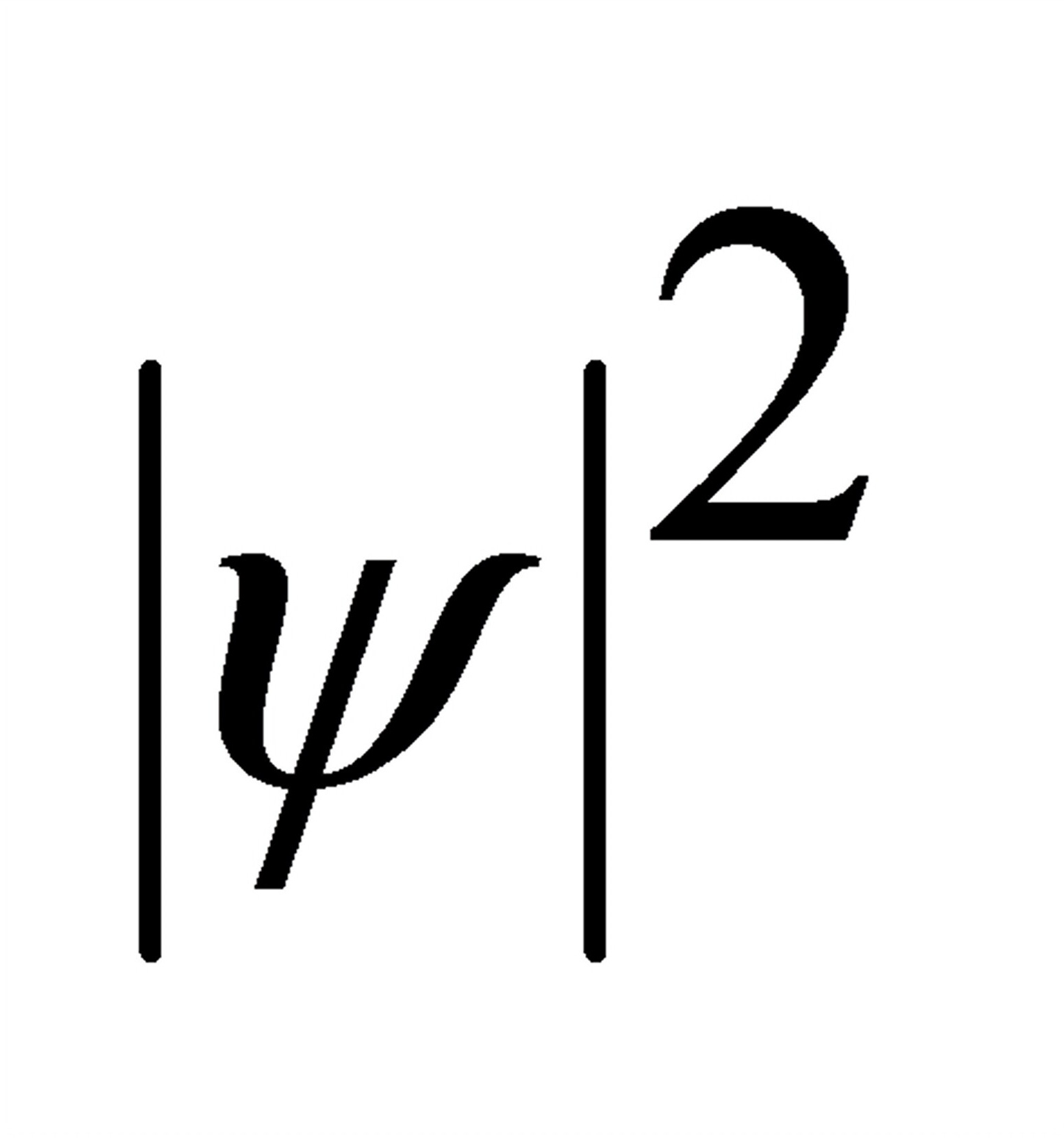 表示电子的几率密度
表示电子的几率密度
C.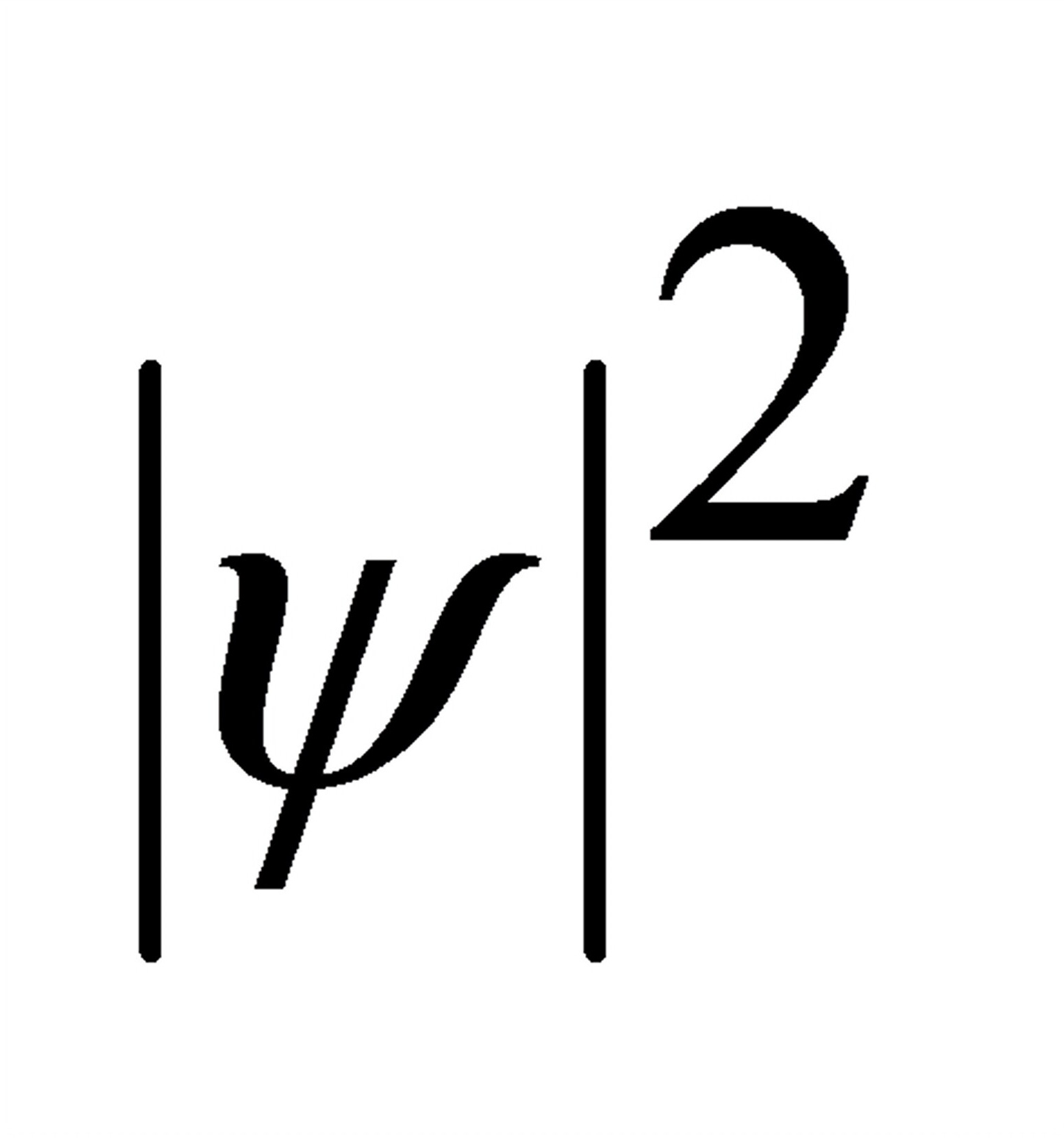 在空间分布的形象比图象成称为电子云 D.
在空间分布的形象比图象成称为电子云 D.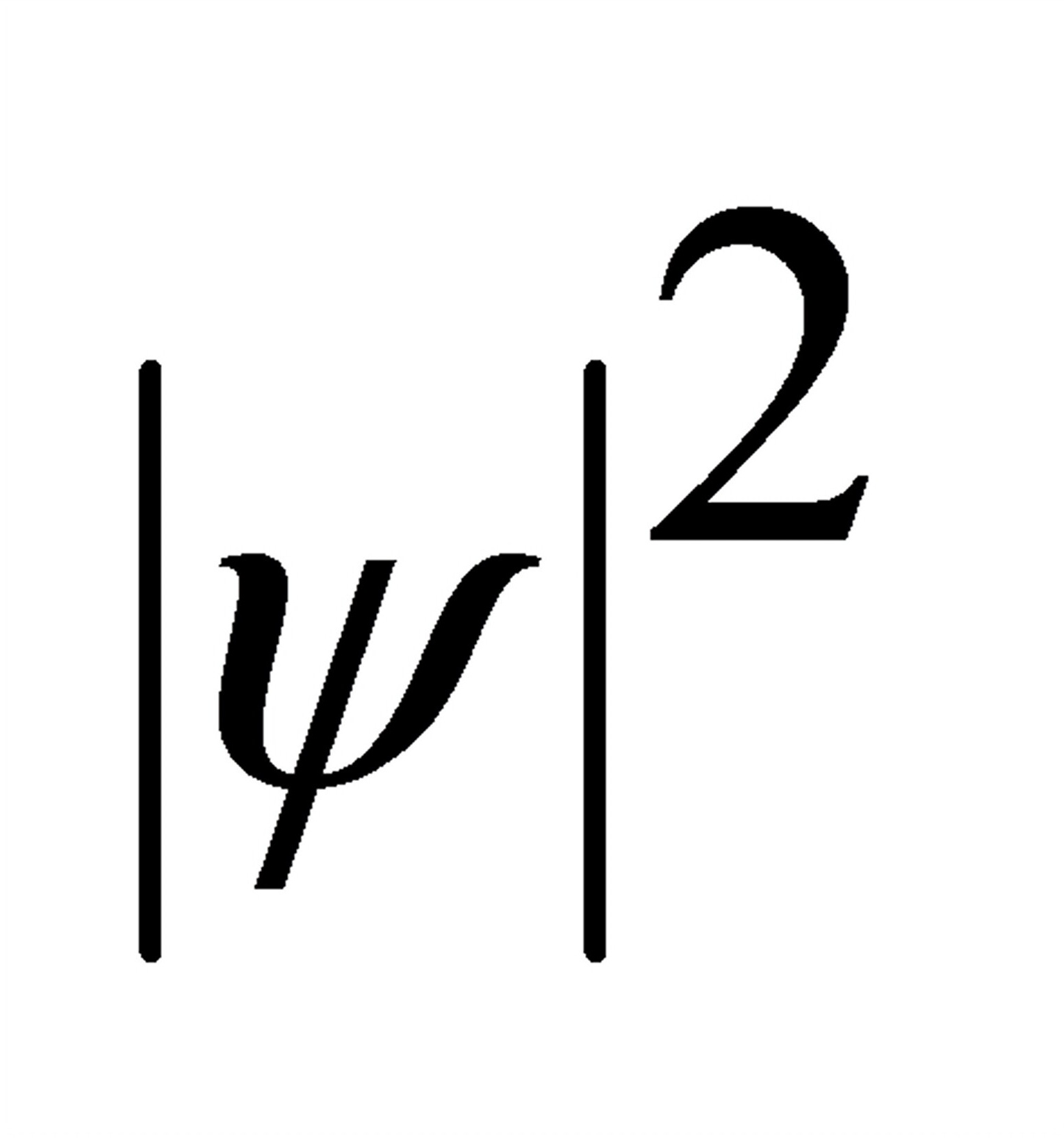 的值大于Ψ的值
的值大于Ψ的值
2-5下面几种描述核外电子运动的说法中,较正确的是
A.电子绕原子核作圆周运动 B.电子在离核一定距离的球面上运动
C.电子在核外一定的空间范围内运动 D.现在还不可能正确描述核外电子运动
2-6下列说法中错误的是
A.只要n,l相同,径向波函数R®就相同 B.波函数的角度分布图形与主量子数无关
C.只要l,m相同,角度波函数Y(θ,φ)就相同
D.s轨道的角度分布波函数Ys(θ,φ)也与角度θ,φ有关
2-7应用波尔理论可以说明的事实中,错误的是
A.氢原子的通常条件下不会发光,也不会发生原子自发毁灭的现象
B.因为轨道是量子化的,所以电子在轨道间跃迁时,发射光的频率也是不连续的
C.当原子受到激发时,核外电子获得能量,从基态跃迁到激发态而发光
D.基态氢原子的轨道半径为52.9pm
2-8在电子云示意图中的小黑点
A.表示电子B.表示电子在该处出现
C.其疏密表示电子出现的几率大小 D. 其疏密表示电子出现的几率密度大小
2-9所谓原子轨道是指
A.一定的电子云 B.核外电子的概率 C.一定的波函数 D.某个径向分布函数
2-10以波函数Ψ(n,l,m)表示原子轨道时,正确的表示是
A.Ψ3,2,0B.Ψ3,1,1/2C.Ψ3,3,2D.Ψ4,0,-1
2-11决定核外电子运动状态的量子数为
A. n,l B. n,m C. n,l,m D.n,l,m,ms
2-12决定原子轨道数目的量子数是
A. n B. l C. n,l D. n,l,m
2-13量子数n,l和m不能决定
A.原子轨道的能量 B.原子轨道的形成 C.原子轨道的数目 D.电子的数目
2-14用量子数描述的下列亚层中,可以容纳电子数最多的是
A.n=2,l=1 B.n=3,l=2 C.n=4,l=3 D.n=5,l=0
2-15对于多电子原子来说,下列说法中正确的是
A.主量子数n决定原子轨道的能量 B.主量子数n是决定原子轨道能量的主要因素
C.主量子数n值逾大,轨道能量正值逾大 D.主量子数n决定角量子数l的取值
2-16下列说法中错误的是
A.角量子数l决定原子轨道的形状 B.角量子数l决定原子轨道在空间的伸展方向
C.磁量子数m决定原子轨道在空间的伸展方向 D.2l+1等于原子轨道的数目
2-17 3d轨道的磁量子数可能有
A. 1,2,3 B. 0,1,2 C. 0,________1 D. 0,________1,________2
2-18当角量子数为5时,可能的简并轨道数是
A. 6 B.7 C. 9 D. 11 E. 13
2-19关于下列对四个量子数的说法,正确的是
A.电子的自旋量子数是1/2,在某一个轨道中有两个电子,所以总自旋量子数是1或0
B.磁量子数m=0的轨道都是球形的轨道 C.角量子数l的可能取值是从0到n的正整数
D.多电子原子中电子的能量决定于主量子数n和角量子数l
2-20下列哪一组数值是原子序数19的元素的价电子的四个量子数(依次为n,l,m,ms)
A. 1,0,0,+1/2 B. 2,1,0,+1/2 C. 3,2,1,+1/2 D. 4,0,0,+1/2
2-21有六组量子数:I.n=2, l=1, m=-1; II. n=3, l=0, m=0; III. n=2, l=2, m=-1;IV. n=2, l=1, m=0;V. n=2, l=0, m=-1;VI. n=2, l=3, m=2.其中正确的是
A. I,III,V B. II,IV,VI C. I,II,III D. I,II,IV
2-22某原子中有5个电子,分别具有如下所列的量子数,其中对应于能量最高的电子的量子数是
A. n=2,l=1,m=1.m2=-1/2 B. n=2,l=1,m=0,ms=-1/2
C. n=3,l=1,m=1,ms=1/2 D. n=3,l=2,m=-2,ms=-1/2
2-23对原子中的电子来说,下列成套量子数中不可能存在的是
A. 3,1,1,-1/2 B. 2,1,-1,+1/2 C. 3,3,0,+1/2 D. 4,3,-3,-1/2
2-24一个3p电子可用下列量子数之一来描述:①3,1,0,+1/2;②3,1,0,-1/2;③3,1,1,+1/2;④3,1,1,-1/2;⑤3,1,-1,+1/2;⑥3,1,-1,-1/2。硫的电子构型为1s22s22p63s23p4,其3p电子组合正确的有
A.①②③④B.①③④⑥C.②③④⑥D.②④⑤⑥
2-25钠原子的1s电子能量与氢原子的1s电子能量相比较的结果是
A.前者高 B.后者高 C.相等 D.符号相反
2-26原子核外电子排布主要应遵循
A.统计规律 B.能量最低原理 C.泡利不相容原理 D.洪特规则
2-27对于基态原子电子排布规则,下列叙述中正确的是
A.按照洪特规则,每个电子层的电子容量为2n2个
B.当轨道处于完全充满时,电子较稳定,故35Br的电子排布为[Ar]3d104s14p6
C.原子中核外电子的分布是根据三规则、一特例得出的
D.能量最低原理解决了电子在不同亚层中的排布顺序问题,而洪特规则解决了电子在简并轨道中的排布问题
2-28.若将氮原子的电子排布式写成1s22s22px22py1,它违背
A.能量守恒原理 B.泡利不相容原理 C.能量最低原理 D.洪特规则
2-29多电子原子的能量E由下列哪一组量子数决定的
A.主量子数n B. n和l C. n,l,m D. l
2-30 39号元素钇的电子排布应是下列各组中的哪一组
A. 1s22s32p63s23d104s24p64d15s2B. 1s22s22p63s23p63d104s24p65s25p1
C. 1s22s22p63s23p63d104s24p64f15s2D. 1s22s22p23s23p63d104s24p65s25d1
2-31 n=4时,电子填入轨道的顺序是
A. 1s2s2p3s3p3d4s4p4d4fB. 1s2s2p3s3p3d4s4p4d
C. 1s2s2p2d3s3p3d4s4p4d D. 1s2s2p3s3p4s3d4p
2-32铜原子的价层电子排布式为
A.3d94s2B.3d104s1C.3d64s2D.3s13d10
2-33铁原子的价电子构型是
A. 4s2B. 4s24d6C. 3d64s2D. 3s23p63d6
2-34 Cr3+的外层电子排布式为
A. 3d24s1B. 3d34s0C. 3s23p63d64s1D. 3s23p63d3
2-35 Fe3+的外层电子排布式为
A 3d34s1B. 3d34s0C. 3s23p63d5D. 3s23p63d34s2
2-36某基态原子的第六电子层只有2个电子时,其第五电子层上的电子数为
题目解答
答案
+ + +