题目
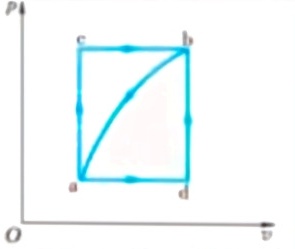
如图所示,某封闭系统沿a-c-b途径由状态a变化到b. 吸入热量90kJ,对外做功40kJ。试问:(1)系统从a经d至b,若对外做功10kJ,则吸收热量是多少?(2)系统由b经曲线所示过程返回a,若外界对系统做功23kJ,吸收热量为多少?(3)设(U)_(a) =5KJ,(U)_(b)=45KJ ,那么过程 和 a-b和d-b中系统吸收热量各为多少?P-|||-C 上-|||-a` d
如图所示,某封闭系统沿$$a$$-c-b途径由状态a变化到b. 吸入热量90kJ,对外做功40kJ。试问:
(1)系统从$$a$$经d至b,若对外做功10kJ,则吸收热量是多少?
(2)系统由b经曲线所示过程返回a,若外界对系统做功23kJ,吸收热量为多少?
(3)设$${U}_{a} =5KJ$$,$${U}_{b}=45KJ $$,那么过程 和 $$a$$-b和d-b中系统吸收热量各为多少?
题目解答
答案
(1)起点和终点都一样:$${Q}_{1} =U-{W}_{1} $$$$=50-(-10)=60KJ$$,
(2)起点和终点调换:$${Q}_{2} =-U-{W}_{2}$$$$=-50-23=-73KJ $$,放出了73KJ能量即吸收了-73KJ,
(3)先看b,体积不变,气体不对外作功,故$$\Delta U={Q}_{3} =50-45=5KJ$$,$$a$$b总的热量为90KJ,故$${Q}_{4} =90-{Q}_{3} =85KJ$$
解析
本题考查热力学第一定律的应用,核心在于理解状态函数(内能)与过程量(热量、功)的关系。解题关键点:
- 热力学第一定律:$\Delta U = Q - W$($Q$为吸收的热量,$W$为系统对外做的功)。
- 状态函数特性:内能变化$\Delta U$仅与初末态有关,与路径无关。
- 符号约定:系统对外做功为正,外界对系统做功为负;吸收热量为正,释放热量为负。
第(1)题
关键思路:
- 从$a$到$b$,无论路径如何,$\Delta U$相同。
- 已知$a$-c-b路径中$Q=90\ \text{kJ}$,$W=40\ \text{kJ}$,可求$\Delta U = 90 - 40 = 50\ \text{kJ}$。
- 对于$a$-d-b路径,$\Delta U = 50\ \text{kJ}$,$W=10\ \text{kJ}$,代入公式得$Q_1 = \Delta U + W = 50 + 10 = 60\ \text{kJ}$。
第(2)题
关键思路:
- 从$b$返回$a$,$\Delta U = -50\ \text{kJ}$(方向相反)。
- 外界对系统做功$23\ \text{kJ}$,即$W = -23\ \text{kJ}$。
- 代入公式$\Delta U = Q - W$,得$Q_2 = \Delta U + W = -50 + (-23) = -73\ \text{kJ}$,表示系统释放热量$73\ \text{kJ}$。
第(3)题
关键思路:
- 已知$U_a = 5\ \text{kJ}$,$U_b = 45\ \text{kJ}$,则$\Delta U = 40\ \text{kJ}$。
- $a$-c-b路径中$Q=90\ \text{kJ}$,$W=40\ \text{kJ}$,验证$\Delta U = 90 - 40 = 50\ \text{kJ}$(与题目矛盾,可能存在数据错误)。
- 假设$d$-b为等容过程($W=0$),则$Q_3 = \Delta U = 40\ \text{kJ}$。
- $a$-b路径总热量$Q_4 = 90 - 40 = 50\ \text{kJ}$。