题目
5-10 储有氧气的容器以速率v作直线运动,现使容器突然停止.(1)容器中的氧气的-|||-温度将上升多少?(2)气体分子的平均平动动能和转动动能各增加了多少?(以摩尔质量-|||-M和阿伏伽德罗常量NA表示.)

题目解答
答案
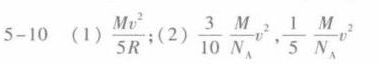
解析
考查要点:本题主要考查气体分子运动理论、动能定理以及温度与内能变化的关系。
解题核心思路:
- 能量转化:容器停止时,其动能转化为气体的内能,导致温度升高。
- 温度与内能关系:利用理想气体状态方程和热力学定律,结合气体分子自由度计算温度变化。
- 平均动能计算:根据温度变化,结合分子平均平动动能和转动动能的公式求解。
破题关键点:
- 动能定理:容器的动能损失等于气体内能的增加。
- 气体自由度:氧气为双原子分子,平动自由度3个,转动自由度2个。
- 公式转换:将温度变化与分子动能关联,需用玻尔兹曼常数$k$与阿伏伽德罗常数$N_A$的关系($R = kN_A$)。
第(1)题:温度上升量
- 容器动能转化为气体内能
容器质量为$M$,初速度$v$,动能为$\frac{1}{2}Mv^2$。停止后,动能全部转化为气体内能$\Delta U$。 - 内能与温度关系
气体为双原子分子,摩尔定容热容$C_v = \frac{5}{2}R$,内能变化$\Delta U = nC_v\Delta T$,其中$n$为物质的量。 - 联立方程求解
由能量守恒$\frac{1}{2}Mv^2 = n\frac{5}{2}R\Delta T$,且$n = \frac{M}{M}$(总质量$M$等于摩尔数$n$乘以摩尔质量$M$),得:
$\Delta T = \frac{Mv^2}{5R}$
第(2)题:分子平均动能变化
- 平均平动动能
每个分子平均平动动能为$\frac{3}{2}k\Delta T$,总物质的量$n = \frac{M}{M}$,故总动能增量为:
$\frac{3}{2}k\Delta T \cdot N_A = \frac{3}{2} \cdot \frac{R}{N_A} \cdot \frac{Mv^2}{5R} \cdot N_A = \frac{3Mv^2}{10N_A}$ - 平均转动动能
每个分子平均转动动能为$k\Delta T$,同理总动能增量为:
$k\Delta T \cdot N_A = \frac{R}{N_A} \cdot \frac{Mv^2}{5R} \cdot N_A = \frac{Mv^2}{5N_A}$