题目
如图示,若系统沿等温线由状态A变化到状态B,温度和内能如何变化?对外是否做功定是吸热还是放热?请一一作出解答。p A A-|||-B-|||-v-|||-0 V2-|||-1
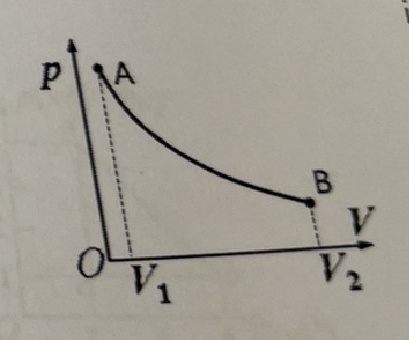
如图示,若系统沿等温线由状态A变化到状态B,温度和内能如何变化?对外是否做功定是吸热还是放热?请一一作出解答。
题目解答
答案
系统沿等温线由状态A变化到状态B的过程中,温度不变,根据一定质量的某种理想气体内能只与温度有关,所以系统内能不变,即△U=0,体积变大,气体对外界做正功,即W<0,根据热力学第一定律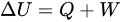 ,可得Q>0,即从外界吸热。
,可得Q>0,即从外界吸热。
解析
考查要点:本题主要考查理想气体等温变化过程中的温度、内能变化,以及做功和热传递的判断,需结合热力学第一定律进行分析。
解题核心思路:
- 等温过程:温度不变,理想气体的内能仅由温度决定,因此内能不变。
- 体积变化与做功:体积增大时,气体对外界做功。
- 热力学第一定律:通过能量守恒关系($\Delta U = Q + W$)判断吸放热情况。
破题关键点:
- 明确等温线的特性(温度不变)。
- 理解理想气体的内能与温度的关系。
- 正确应用热力学第一定律,注意功的符号约定(题目中假设$W$为外界对系统做的功)。
温度变化
系统沿等温线变化,温度保持不变,即$T_A = T_B$。
内能变化
对于理想气体,内能仅由温度决定。由于温度不变,故内能变化$\Delta U = 0$。
做功判断
从状态A到状态B,气体体积增大($V_1 \to V_2$),气体对外界做正功,因此功$W < 0$(根据题目中$W$的定义:外界对系统做功为正)。
吸放热判断
根据热力学第一定律:
$\Delta U = Q + W$
已知$\Delta U = 0$,$W < 0$,代入得:
$0 = Q + W \implies Q = -W$
由于$W$为负值,$Q$必为正值,说明气体从外界吸收热量。