题目
习题27 10g理想气体氦在127℃时压力为 times (10)^5Pa, 今在定温下外压恒定为10°,Pa-|||-进行压缩、计算此过程的Q、W、 △U. Delta H Delta S Delta A 及 Delta G-|||-[答案: =-8.31times (10)^3J =8.31times (10)^3J Delta U=Delta H=0;-|||-Delta S=-14.4] cdot (K)^-1 ;Delta A=Delta G=5.76times (10)^3JJ

题目解答
答案
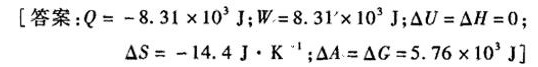
解析
步骤 1:计算初始体积
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压力,$V$ 是体积,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度。已知 $P=5\times {10}^{5}Pa$,$T=127℃=400K$,$n=\frac{10g}{4g/mol}=2.5mol$,$R=8.31J\cdot mol^{-1}\cdot K^{-1}$,代入公式计算初始体积 $V$。
步骤 2:计算终态体积
在定温下,外压恒定为 $10^6Pa$,根据理想气体状态方程 $PV=nRT$,计算终态体积 $V'$。
步骤 3:计算功
在定温下,外压恒定,根据公式 $W=-P_{外}\Delta V$ 计算功。
步骤 4:计算热量
根据热力学第一定律 $\Delta U=Q+W$,其中 $\Delta U$ 是内能变化,$Q$ 是热量,$W$ 是功。对于理想气体,定温过程内能变化 $\Delta U=0$,从而计算热量 $Q$。
步骤 5:计算熵变
根据熵变公式 $\Delta S=\frac{Q}{T}$,计算熵变 $\Delta S$。
步骤 6:计算亥姆霍兹自由能变化
根据亥姆霍兹自由能变化公式 $\Delta A=\Delta U-T\Delta S$,计算亥姆霍兹自由能变化 $\Delta A$。
步骤 7:计算吉布斯自由能变化
根据吉布斯自由能变化公式 $\Delta G=\Delta H-T\Delta S$,计算吉布斯自由能变化 $\Delta G$。
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压力,$V$ 是体积,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度。已知 $P=5\times {10}^{5}Pa$,$T=127℃=400K$,$n=\frac{10g}{4g/mol}=2.5mol$,$R=8.31J\cdot mol^{-1}\cdot K^{-1}$,代入公式计算初始体积 $V$。
步骤 2:计算终态体积
在定温下,外压恒定为 $10^6Pa$,根据理想气体状态方程 $PV=nRT$,计算终态体积 $V'$。
步骤 3:计算功
在定温下,外压恒定,根据公式 $W=-P_{外}\Delta V$ 计算功。
步骤 4:计算热量
根据热力学第一定律 $\Delta U=Q+W$,其中 $\Delta U$ 是内能变化,$Q$ 是热量,$W$ 是功。对于理想气体,定温过程内能变化 $\Delta U=0$,从而计算热量 $Q$。
步骤 5:计算熵变
根据熵变公式 $\Delta S=\frac{Q}{T}$,计算熵变 $\Delta S$。
步骤 6:计算亥姆霍兹自由能变化
根据亥姆霍兹自由能变化公式 $\Delta A=\Delta U-T\Delta S$,计算亥姆霍兹自由能变化 $\Delta A$。
步骤 7:计算吉布斯自由能变化
根据吉布斯自由能变化公式 $\Delta G=\Delta H-T\Delta S$,计算吉布斯自由能变化 $\Delta G$。