题目
1mol单原子理想气体,从101.325 kPa 300 K绝热压缩至600 K,则过程的Delta H等于
1mol单原子理想气体,从101.325 kPa 300 K绝热压缩至600 K,则过程的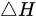 等于
等于
题目解答
答案
1. 焓变公式
对于单原子理想气体,焓变 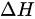 可通过以下公式计算:
可通过以下公式计算:
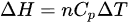
其中:
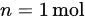
Cp 是单原子理想气体的定压摩尔热容, 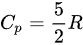
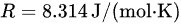 是气体常数
是气体常数
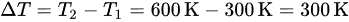
2. 计算定压热容 Cp
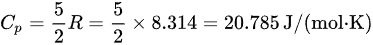
3. 计算焓变 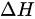
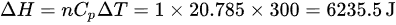
答案:
该过程的焓变 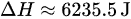
解析
步骤 1:确定焓变公式
对于单原子理想气体,焓变 $\Delta H$ 可通过以下公式计算:
$$\Delta H = nC_p\Delta T$$
其中:
- $n = 1$ mol
- $C_p$ 是单原子理想气体的定压摩尔热容,$C_p = \frac{5}{2}R$
- $R = 8.314$ J/(mol·K) 是气体常数
- $\Delta T = T_2 - T_1 = 600$ K - 300 K = 300 K
步骤 2:计算定压热容 $C_p$
$$C_p = \frac{5}{2}R = \frac{5}{2} \times 8.314 = 20.785 \text{ J/(mol·K)}$$
步骤 3:计算焓变 $\Delta H$
$$\Delta H = nC_p\Delta T = 1 \times 20.785 \times 300 = 6235.5 \text{ J}$$
对于单原子理想气体,焓变 $\Delta H$ 可通过以下公式计算:
$$\Delta H = nC_p\Delta T$$
其中:
- $n = 1$ mol
- $C_p$ 是单原子理想气体的定压摩尔热容,$C_p = \frac{5}{2}R$
- $R = 8.314$ J/(mol·K) 是气体常数
- $\Delta T = T_2 - T_1 = 600$ K - 300 K = 300 K
步骤 2:计算定压热容 $C_p$
$$C_p = \frac{5}{2}R = \frac{5}{2} \times 8.314 = 20.785 \text{ J/(mol·K)}$$
步骤 3:计算焓变 $\Delta H$
$$\Delta H = nC_p\Delta T = 1 \times 20.785 \times 300 = 6235.5 \text{ J}$$