题目
如图所示,某闭口系统,工质沿a—c-b由状态a变化到状态b时,吸热100kJ,对外做功40kJ。c b-|||-a d(1)当工质沿过程a—d—b变化到状态b时,对外做功20kJ,试求过程a-d-b中工质与外界交换的热量。(2)当工质沿曲线从b返回初态a时,外界对系统做功30kJ,试求此过程中工质与外界交换的热量。(3)如果(U)_(a) =0kJ,(U)_(d) =40kJ,求过程a-d、d-b与外界交换的热量。
如图所示,某闭口系统,工质沿a—c-b由状态a变化到状态b时,吸热100kJ,对外做功40kJ。
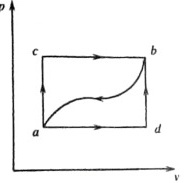
(1)当工质沿过程a—d—b变化到状态b时,对外做功20kJ,试求过程a-d-b中工质与外界交换的热量。(2)当工质沿曲线从b返回初态a时,外界对系统做功30kJ,试求此过程中工质与外界交换的热量。
(3)如果$${U}_{a} $$=0kJ,$${U}_{d} $$=40kJ,求过程a-d、d-b与外界交换的热量。
题目解答
答案
(1)吸热80KJ;
(2)散热90KJ;
(3)吸热40KJ,吸热40KJ。
解析
步骤 1:确定热力学第一定律
热力学第一定律表明,一个系统的内能变化等于系统吸收的热量减去系统对外做的功。用公式表示为:$$\Delta U = Q - W$$
步骤 2:计算过程a-c-b的内能变化
根据题目,工质沿a-c-b由状态a变化到状态b时,吸热100kJ,对外做功40kJ。因此,过程a-c-b的内能变化为:$$\Delta U_{a-c-b} = Q_{a-c-b} - W_{a-c-b} = 100kJ - 40kJ = 60kJ$$
步骤 3:计算过程a-d-b的热量交换
根据题目,工质沿过程a-d-b变化到状态b时,对外做功20kJ。由于a-c-b和a-d-b都是从a到b,内能变化相同,即$\Delta U_{a-d-b} = \Delta U_{a-c-b} = 60kJ$。因此,过程a-d-b的热量交换为:$$Q_{a-d-b} = \Delta U_{a-d-b} + W_{a-d-b} = 60kJ + 20kJ = 80kJ$$
步骤 4:计算过程b-a的热量交换
根据题目,工质沿曲线从b返回初态a时,外界对系统做功30kJ。由于b-a是a-b的逆过程,内能变化相反,即$\Delta U_{b-a} = -\Delta U_{a-b} = -60kJ$。因此,过程b-a的热量交换为:$$Q_{b-a} = \Delta U_{b-a} + W_{b-a} = -60kJ + 30kJ = -30kJ$$
步骤 5:计算过程a-d和d-b的热量交换
根据题目,如果$${U}_{a} $$=0kJ,$${U}_{d} $$=40kJ,那么过程a-d的内能变化为:$$\Delta U_{a-d} = {U}_{d} - {U}_{a} = 40kJ - 0kJ = 40kJ$$
过程d-b的内能变化为:$$\Delta U_{d-b} = {U}_{b} - {U}_{d} = 60kJ - 40kJ = 20kJ$$
因此,过程a-d的热量交换为:$$Q_{a-d} = \Delta U_{a-d} + W_{a-d} = 40kJ + 0kJ = 40kJ$$
过程d-b的热量交换为:$$Q_{d-b} = \Delta U_{d-b} + W_{d-b} = 20kJ + 20kJ = 40kJ$$
热力学第一定律表明,一个系统的内能变化等于系统吸收的热量减去系统对外做的功。用公式表示为:$$\Delta U = Q - W$$
步骤 2:计算过程a-c-b的内能变化
根据题目,工质沿a-c-b由状态a变化到状态b时,吸热100kJ,对外做功40kJ。因此,过程a-c-b的内能变化为:$$\Delta U_{a-c-b} = Q_{a-c-b} - W_{a-c-b} = 100kJ - 40kJ = 60kJ$$
步骤 3:计算过程a-d-b的热量交换
根据题目,工质沿过程a-d-b变化到状态b时,对外做功20kJ。由于a-c-b和a-d-b都是从a到b,内能变化相同,即$\Delta U_{a-d-b} = \Delta U_{a-c-b} = 60kJ$。因此,过程a-d-b的热量交换为:$$Q_{a-d-b} = \Delta U_{a-d-b} + W_{a-d-b} = 60kJ + 20kJ = 80kJ$$
步骤 4:计算过程b-a的热量交换
根据题目,工质沿曲线从b返回初态a时,外界对系统做功30kJ。由于b-a是a-b的逆过程,内能变化相反,即$\Delta U_{b-a} = -\Delta U_{a-b} = -60kJ$。因此,过程b-a的热量交换为:$$Q_{b-a} = \Delta U_{b-a} + W_{b-a} = -60kJ + 30kJ = -30kJ$$
步骤 5:计算过程a-d和d-b的热量交换
根据题目,如果$${U}_{a} $$=0kJ,$${U}_{d} $$=40kJ,那么过程a-d的内能变化为:$$\Delta U_{a-d} = {U}_{d} - {U}_{a} = 40kJ - 0kJ = 40kJ$$
过程d-b的内能变化为:$$\Delta U_{d-b} = {U}_{b} - {U}_{d} = 60kJ - 40kJ = 20kJ$$
因此,过程a-d的热量交换为:$$Q_{a-d} = \Delta U_{a-d} + W_{a-d} = 40kJ + 0kJ = 40kJ$$
过程d-b的热量交换为:$$Q_{d-b} = \Delta U_{d-b} + W_{d-b} = 20kJ + 20kJ = 40kJ$$