第三章 热力学第二定律[复习题][1]指出下列公式的适用围。(1)△...S=-R ∑n8 lnxR-|||-B;(2)△...S=-R ∑n8 lnxR-|||-B;(3)△...S=-R ∑n8 lnxR-|||-B;(4)△...S=-R ∑n8 lnxR-|||-B(5)△...S=-R ∑n8 lnxR-|||-B作为判据时必须满足的条件。[解] (1)封闭体系平衡态,理想气体的等温混合,混合前后每种气体单独存在时的压力都相等,且等于混合后气体的总压力。(2)非等温过程中熵的变化过程,对一定量的理想气体由状态A(P1、V1、T1)改变到状态A(P2、V2、T2)时,可由两种可逆过程的加和而求得。(3)均相单组分(或组成一定的多组分)封闭体系,非体积功为0的任何过程;或组成可变的多相多组分封闭体系,非体积功为0的可逆过程。(4)非体积功为0,组成不变的均相封闭体系的等温过程。(5)△...S=-R ∑n8 lnxR-|||-B:封闭体系的绝热过程,可判定过程的可逆与否;隔离体系,可判定过程的自发与平衡。△...S=-R ∑n8 lnxR-|||-B:封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否;△...S=-R ∑n8 lnxR-|||-B:封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;[2]判断下列说法是否正确,并说明原因。(1)不可逆过程一定是自发的,而自发过程一定是不可逆的;(2)凡熵增加过程都是自发过程;(3)不可逆过程的熵永不减少;(4)系统达平衡时,熵值最大,Gibbs自由能最小;(5)当某系统的热力学能和体积恒定时,△...S=-R ∑n8 lnxR-|||-B<0的过程不可能发生;(6)某系统从始态经过一个绝热不可逆过程到达终态,先在要在相同的始、终态之间设计一个绝热可逆过程;(7)在一个绝热系统中,发生了一个不可逆过程,系统从状态1变到了状态2,不论用什么方法,系统再也回不到原来状态了;(8)理想气体的等温膨胀过程,△...S=-R ∑n8 lnxR-|||-B,系统所吸的热全部变成了功,这与Kelvin的说法不符;(9)冷冻机可以从低温热源吸热放给高温热源,这与Clausius的说法不符;(10)△...S=-R ∑n8 lnxR-|||-B恒大于△...S=-R ∑n8 lnxR-|||-B。[答](1)不正确,因为不可逆过程不一定是自发的例如 可逆压缩就不是自发过程,但自发过程一定是不可逆的;(2)不正确,因为熵增加过程不一定是自发过程,但自发过程都是熵增加的过程;所以必须在隔离体系中凡熵增加过程都是自发过程。=-26.36kJ(4)绝热可逆膨胀至压力减少一半;Q=0 △S=0△...S=-R ∑n8 lnxR-|||-B根据绝热过程方程△...S=-R ∑n8 lnxR-|||-B得△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B △...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B△A=△U-S△T=-824.58J-100J•K-1•mol-1×1mol×(206.9K-273K)=-5.787kJ△G=△H-S△T=-1374.3J-100J•K-1•mol-1×1mol×(206.9K-273K)=-5.33kJ(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。Q=0△...S=-R ∑n8 lnxR-|||-B即: △...S=-R ∑n8 lnxR-|||-B代入数据得:T2=218.4K所以 △...S=-R ∑n8 lnxR-|||-B=-680.92J△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B=-1.135kJ△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B=1.125J•K-1S2=△S+S1=1.125J•K-1+100J•K-1=101.125J•K-1△A=△U-△TS=△U-(T2S2-T1S1)=-680.92J-(218.4K×101.125J•K-1-273K×100J•K-1)=4.533kJ△G=△H-△TS=△H-(T2S2-T1S1)=-1135J-(218.4K×101.125J•K-1-273K×100J•K-1)=-26.36kJ=4.08kJ[17]将1molH2O(g)从373K,100kPa下,小心等温压缩,在没有灰尘等凝聚中心存在时,得到了373K,200kPa的介稳水蒸气,但不久介稳水蒸气全变成了液态水,即H2O(g,373K,200kPa)→H2O(l,373K,200kPa)求该过程的△H,△G和△S。已知在该条件下水的摩尔汽化焓为△...S=-R ∑n8 lnxR-|||-B,水的密度为1000kg•m-3.设气体为理想气体,液体体积受压力的影响可忽略不计。[解]设计可逆过程如下:=1mol×8.314J•K•mol×373Kln0.5=-2.15kJ△...S=-R ∑n8 lnxR-|||-B=(1mol×0.018kg•mol/1000kg•m)(200kPa-100kPa)=1.8J△G=△G+△G+△G=-2148.2J△...S=-R ∑n8 lnxR-|||-B[18]用合适的判据证明:(1)在373K和200kPa压力下,HO(l)比HO(g)更稳定;(2)在263K和100kPa压力下,H2O(s)比H2O(l)更稳定;[解](1)设计等温可逆过程如下△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B(等温等压无非体积功的可逆相变过程)△...S=-R ∑n8 lnxR-|||-B所以 △...S=-R ∑n8 lnxR-|||-B若水蒸气可看作理想气体,则所以,在373K和200kPa压力下,HO(l)比HO(g)更稳定。(2)设100kPa压力下设计如下可逆过程如下△...S=-R ∑n8 lnxR-|||-B△...S=-R ∑n8 lnxR-|||-B>0所以自发变化总是朝熵增加的方向进行,HO(s)比HO(l)更稳定。[19]在298K和100kPa压力下,已知C(金刚石)和C(石墨)的摩尔熵、摩尔燃烧焓和密度分别为:试求:(1)在298K及100kPa下,C(石墨)→C(金刚石)的;(2)在298K及100kPa时,哪个晶体更为稳定?(3)增加压力能否使不稳定晶体向稳定晶体转化?如有可能,至少要加多大压力,才能实现这种转化?[解] (1)根据△G=△H-T△S=-393.51kJ•mol-(-395.40kJ•mol)=1.89kJ•mol-1=2.45J•K•mol-5.71J•K•mol=-3.26J•K-1•mol-1=2.862kJ•mol(2)因为298K,100kPa下,>0,说明此反应在该条件下不能自发向右进行,亦即石墨比较稳定.(3)设298K下压力为p时石墨恰能变成金刚石△...S=-R ∑n8 lnxR-|||-B>0,解上式得:p>1.52×10Pa即需要加压至1.52×102Pa时,才能在298K时,使石墨转化为金刚石.[20]某实际气体的状态方程为,式中α为常数。设有1mol该气体,在温度为T的等温条件下,由p9可逆地变到p。试写出:Q,W,△U,△H,△S,△A及△G的计算表达式。
第三章 热力学第二定律
[复习题]
[1]指出下列公式的适用围。
(1)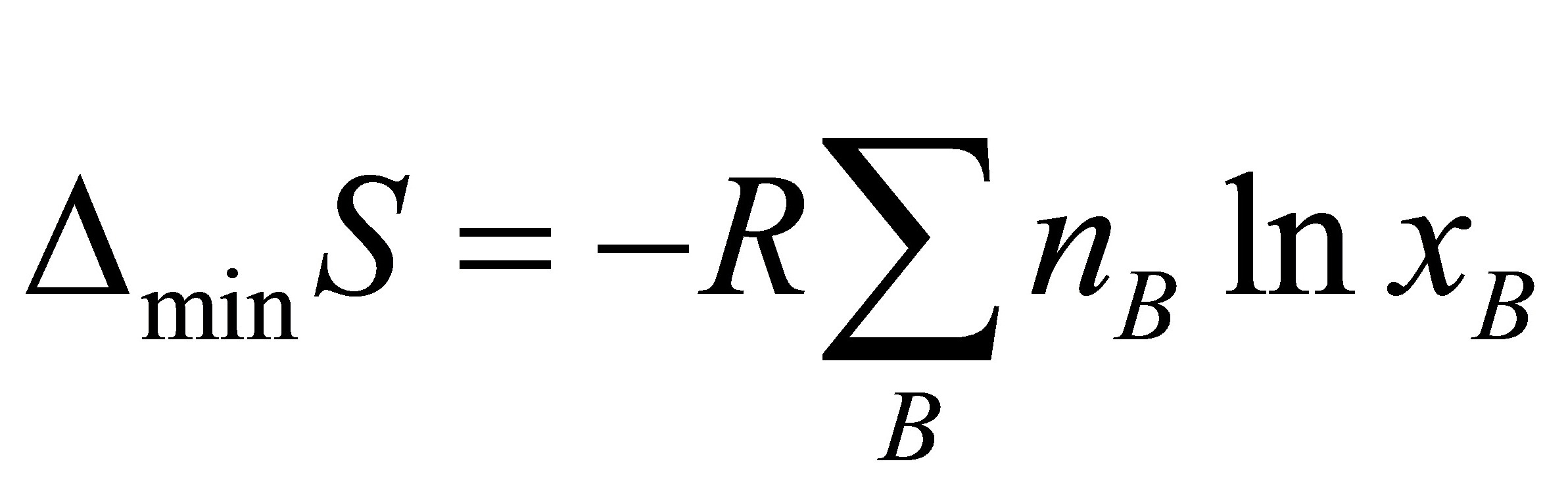 ;
;
(2)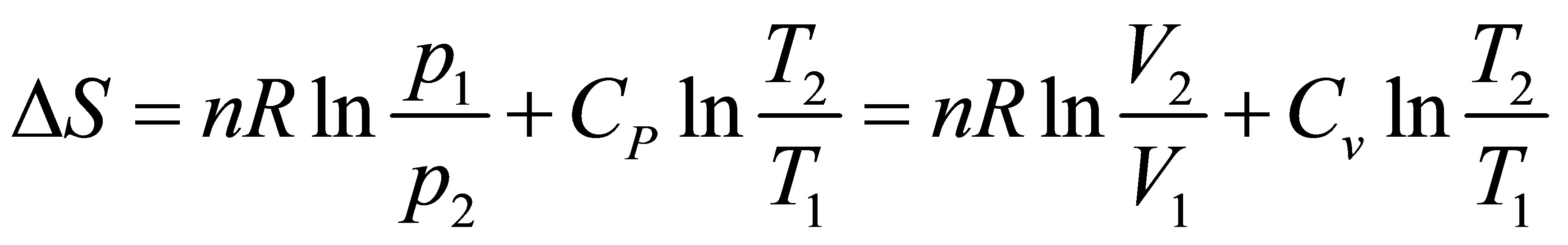 ;
;
(3)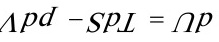 ;
;
(4)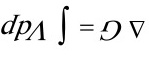
(5)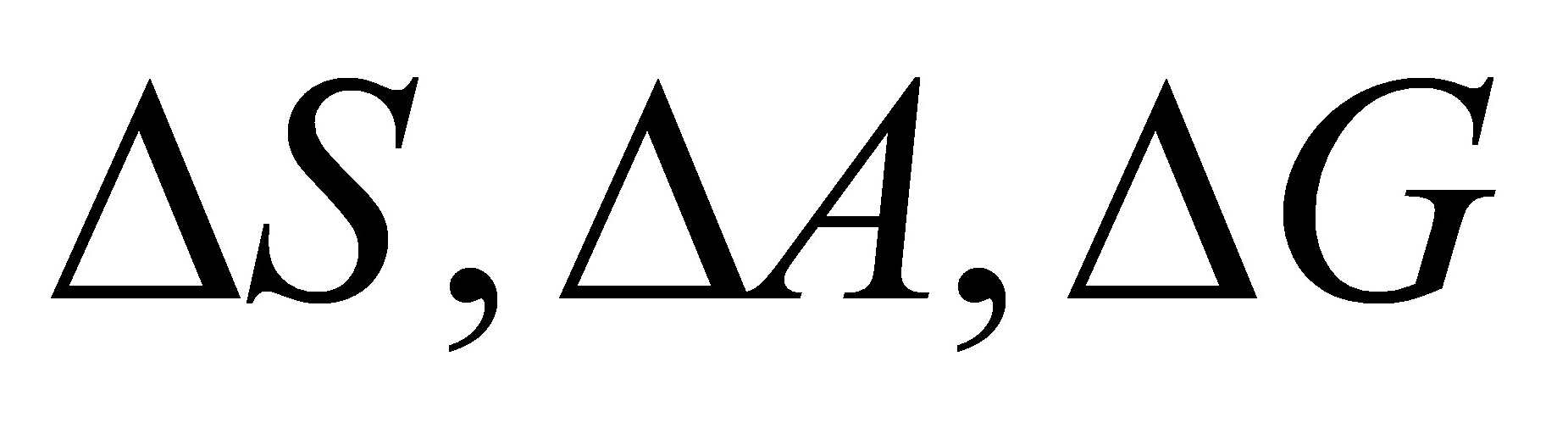 作为判据时必须满足的条件。
作为判据时必须满足的条件。
[解] (1)封闭体系平衡态,理想气体的等温混合,混合前后每种气体单独存在时的压力都相等,且等于混合后气体的总压力。
(2)非等温过程中熵的变化过程,对一定量的理想气体由状态A(P1、V1、T1)改变到状态A(P2、V2、T2)时,可由两种可逆过程的加和而求得。
(3)均相单组分(或组成一定的多组分)封闭体系,非体积功为0的任何过程;或组成可变的多相多组分封闭体系,非体积功为0的可逆过程。
(4)非体积功为0,组成不变的均相封闭体系的等温过程。
(5)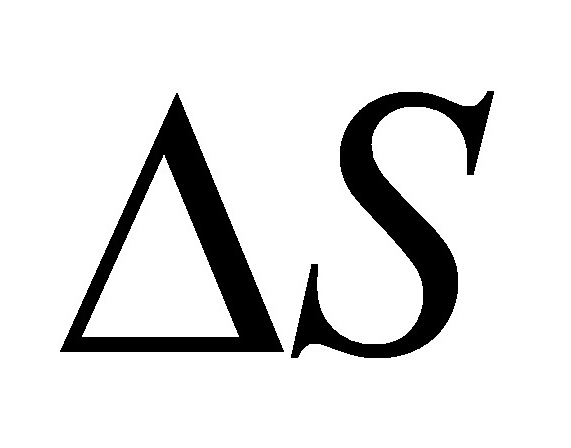 :封闭体系的绝热过程,可判定过程的可逆与否;
:封闭体系的绝热过程,可判定过程的可逆与否;
隔离体系,可判定过程的自发与平衡。
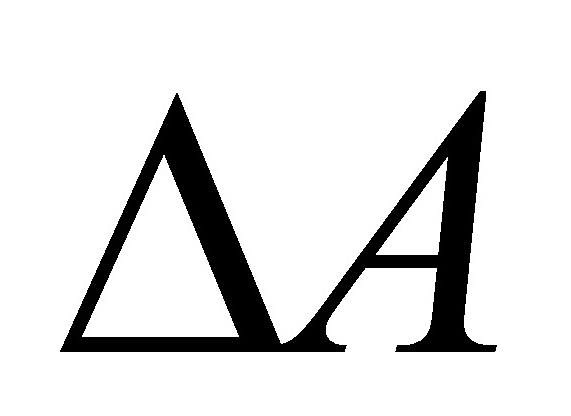 :封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否;
:封闭体系非体积功为0的等温等容过程,可判断过程的平衡与否;
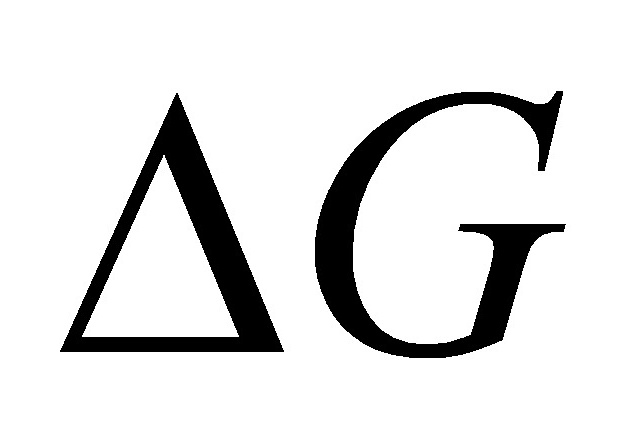 :封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;
:封闭体系非体积功为0的等温等压过程,可判断过程的平衡与否;
[2]判断下列说法是否正确,并说明原因。
(1)不可逆过程一定是自发的,而自发过程一定是不可逆的;
(2)凡熵增加过程都是自发过程;
(3)不可逆过程的熵永不减少;
(4)系统达平衡时,熵值最大,Gibbs自由能最小;
(5)当某系统的热力学能和体积恒定时,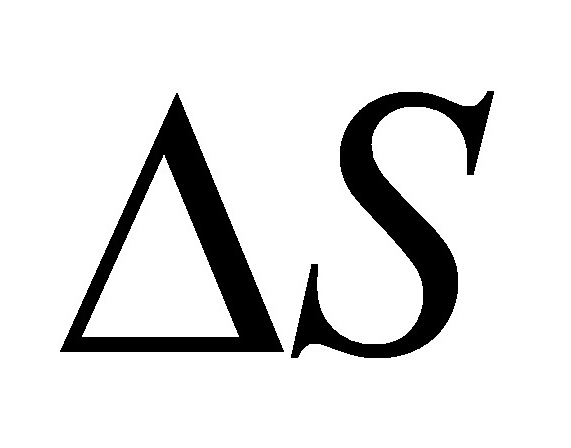 <0的过程不可能发生;
<0的过程不可能发生;
(6)某系统从始态经过一个绝热不可逆过程到达终态,先在要在相同的始、终态之间设计一个绝热可逆过程;
(7)在一个绝热系统中,发生了一个不可逆过程,系统从状态1变到了状态2,不论用什么方法,系统再也回不到原来状态了;
(8)理想气体的等温膨胀过程,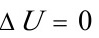 ,系统所吸的热全部变成了功,这与Kelvin的说法不符;
,系统所吸的热全部变成了功,这与Kelvin的说法不符;
(9)冷冻机可以从低温热源吸热放给高温热源,这与Clausius的说法不符;
(10)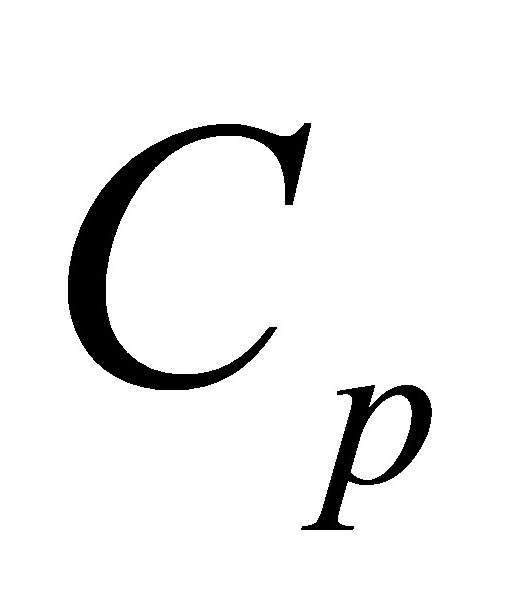 恒大于
恒大于 。
。
[答](1)不正确,因为不可逆过程不一定是自发的例如 可逆压缩就不是自发过程,但自发过程一定是不可逆的;
(2)不正确,因为熵增加过程不一定是自发过程,但自发过程都是熵增加的过程;所以必须在隔离体系中凡熵增加过程都是自发过程。
=-26.36kJ
(4)绝热可逆膨胀至压力减少一半;
Q=0 △S=0
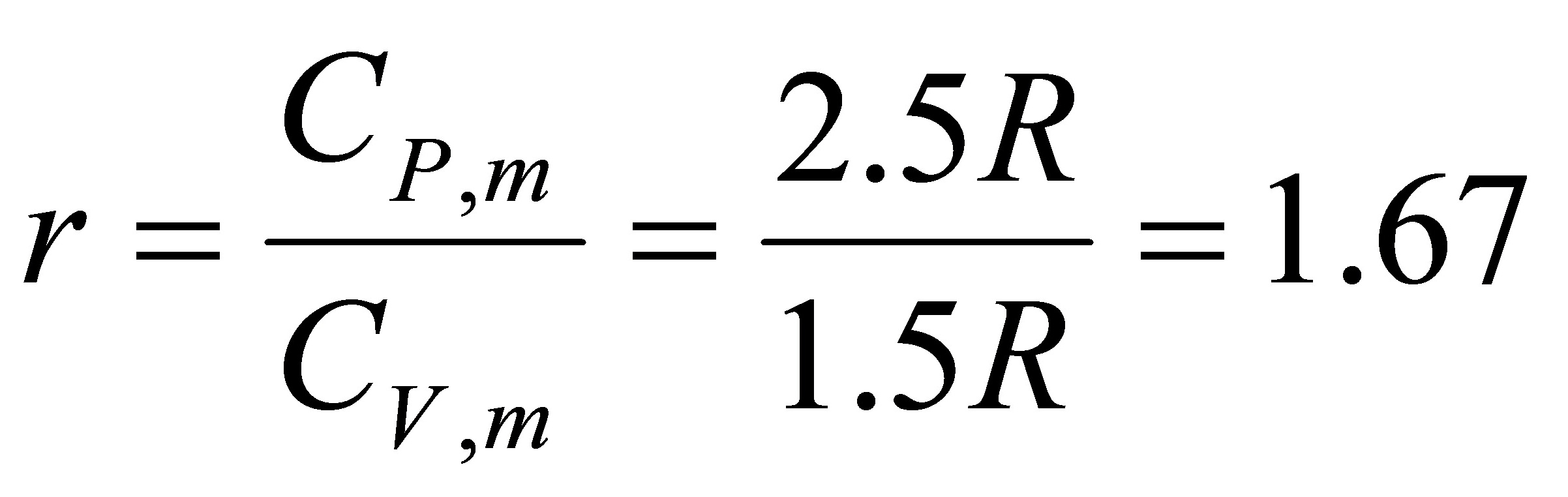
根据绝热过程方程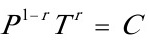 得
得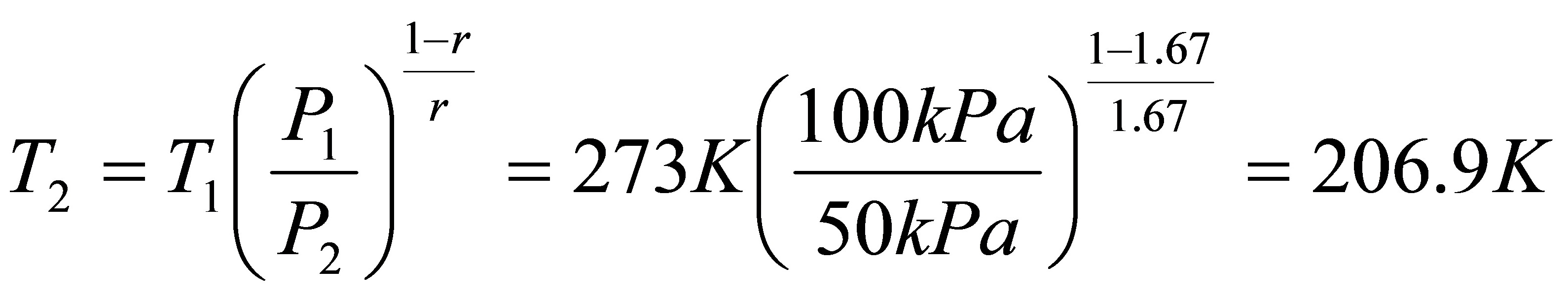
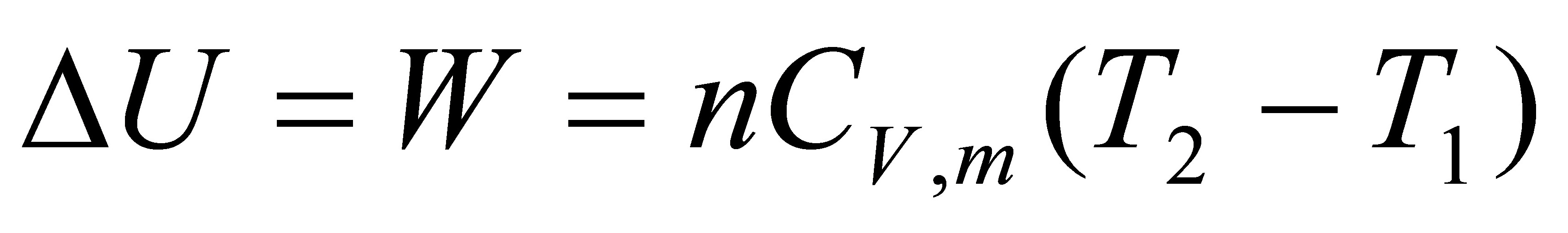
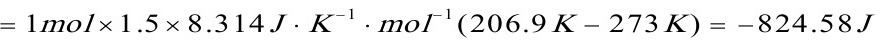
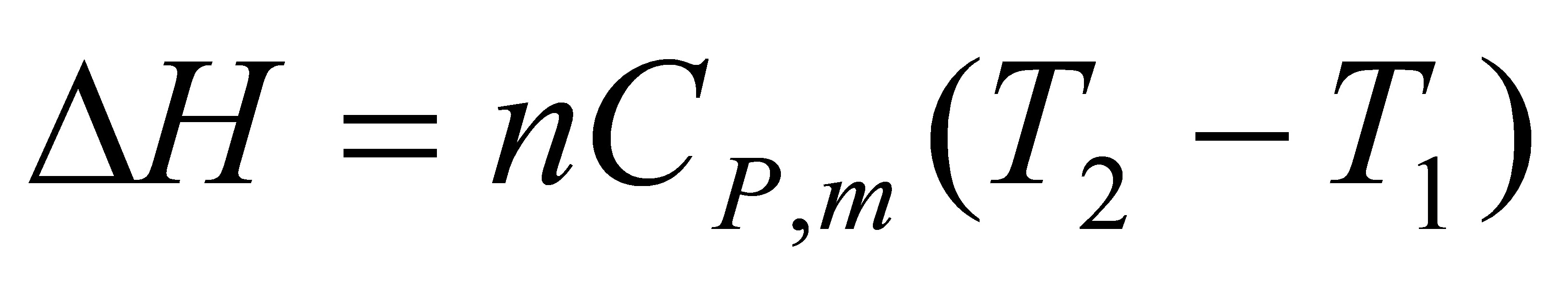
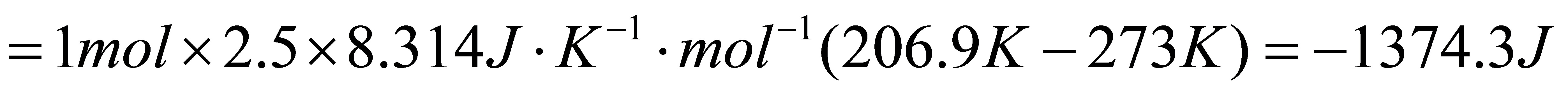
△A=△U-S△T
=-824.58J-100J•K-1•mol-1×1mol×(206.9K-273K)
=-5.787kJ
△G=△H-S△T
=-1374.3J-100J•K-1•mol-1×1mol×(206.9K-273K)
=-5.33kJ
(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。
Q=0
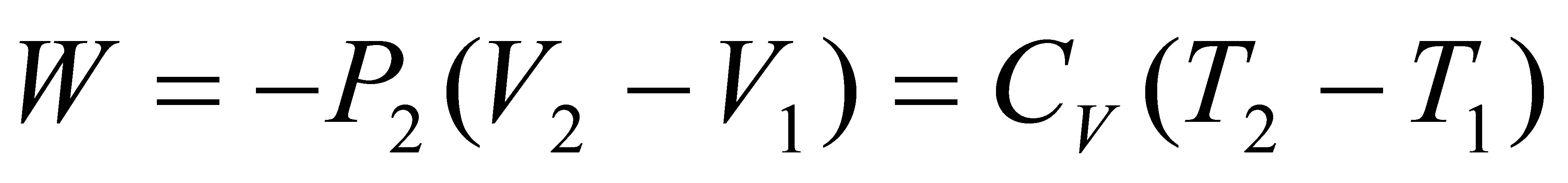
即: 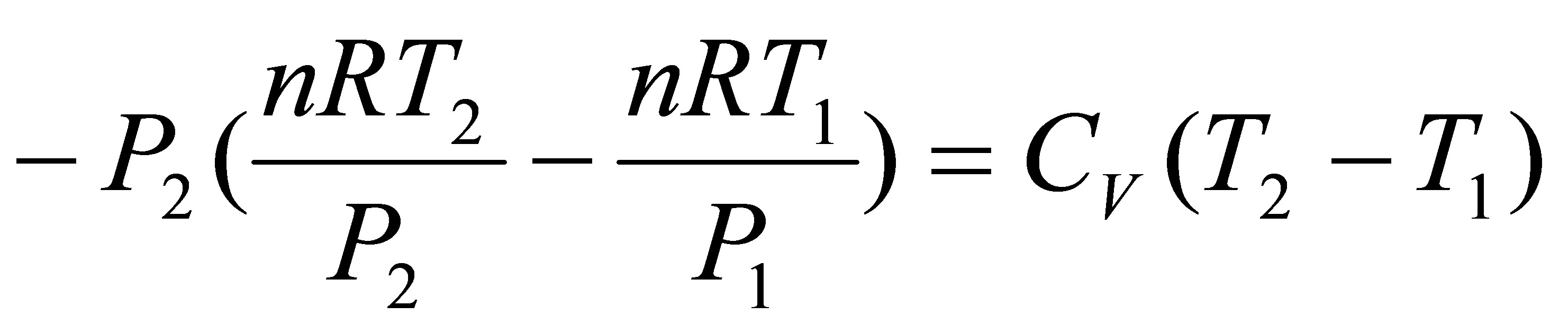
代入数据得:T2=218.4K
所以 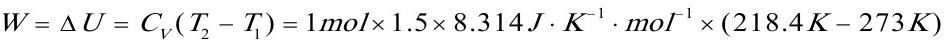
=-680.92J
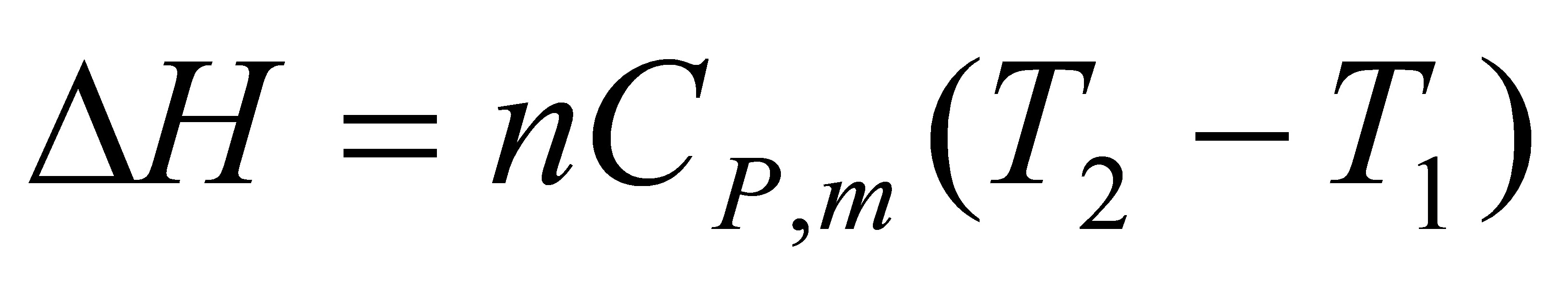
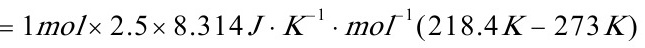
=-1.135kJ
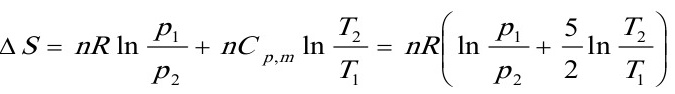
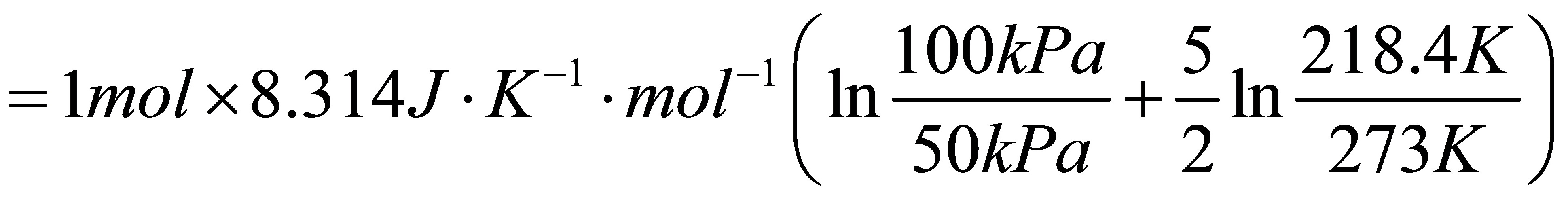
=1.125J•K-1
S2=△S+S1=1.125J•K-1+100J•K-1=101.125J•K-1
△A=△U-△TS=△U-(T2S2-T1S1)
=-680.92J-(218.4K×101.125J•K-1-273K×100J•K-1)
=4.533kJ
△G=△H-△TS=△H-(T2S2-T1S1)
=-1135J-(218.4K×101.125J•K-1-273K×100J•K-1)
=-26.36kJ
=4.08kJ
[17]将1molH2O(g)从373K,100kPa下,小心等温压缩,在没有灰尘等凝聚中心存在时,得到了373K,200kPa的介稳水蒸气,但不久介稳水蒸气全变成了液态水,即
H2O(g,373K,200kPa)→H2O(l,373K,200kPa)
求该过程的△H,△G和△S。已知在该条件下水的摩尔汽化焓为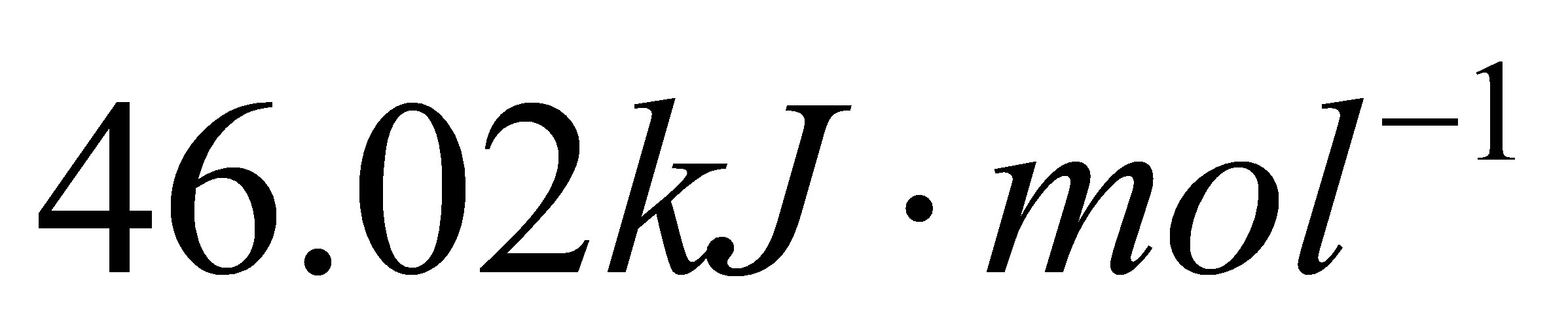 ,水的密度为1000kg•m-3.设气体为理想气体,液体体积受压力的影响可忽略不计。
,水的密度为1000kg•m-3.设气体为理想气体,液体体积受压力的影响可忽略不计。
[解]设计可逆过程如下:
=1mol×8.314J•K•mol×373Kln0.5
=-2.15kJ
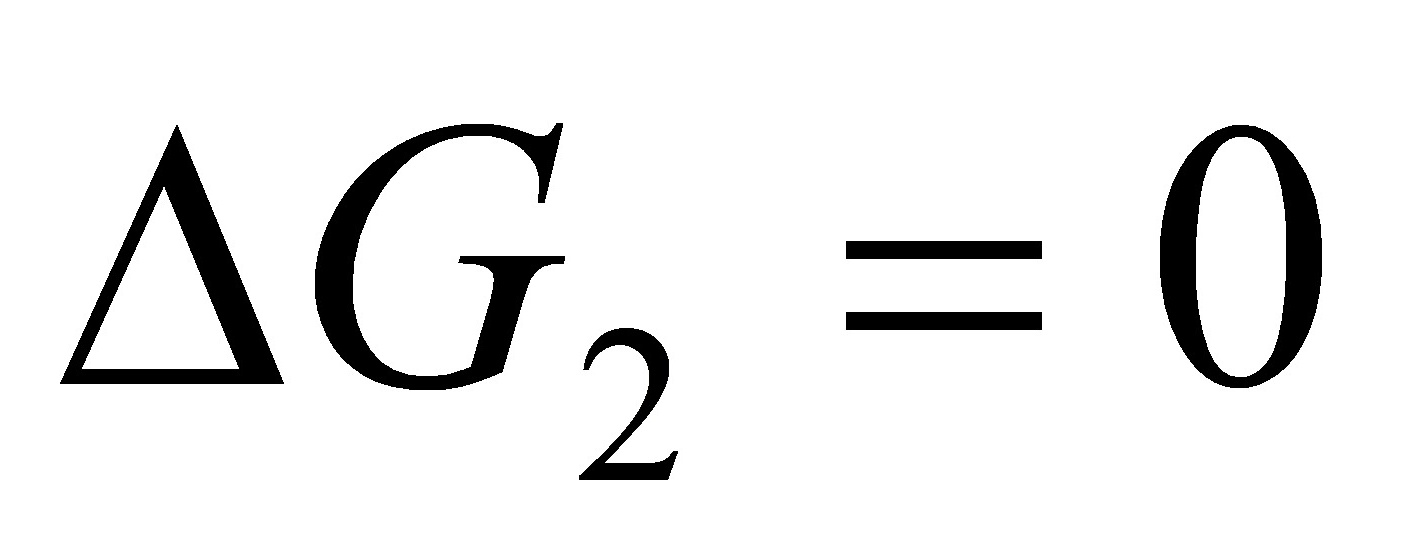
=(1mol×0.018kg•mol/1000kg•m)(200kPa-100kPa)
=1.8J
△G=△G+△G+△G=-2148.2J
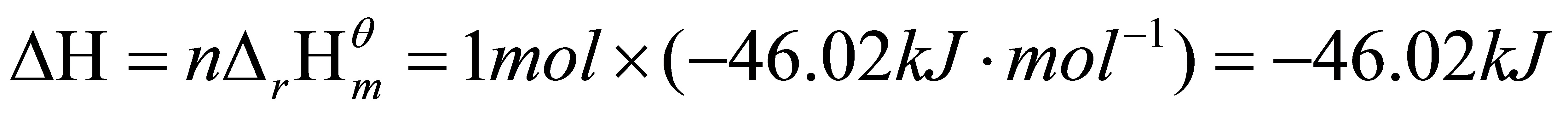
[18]用合适的判据证明:
(1)在373K和200kPa压力下,HO(l)比HO(g)更稳定;
(2)在263K和100kPa压力下,H2O(s)比H2O(l)更稳定;
[解](1)设计等温可逆过程如下
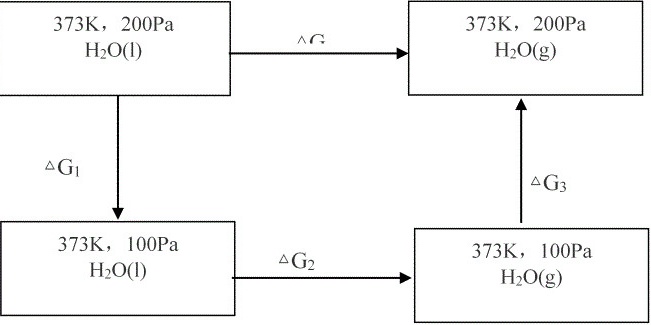
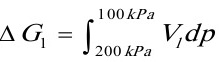 (等温等压无非体积功的可逆相变过程)
(等温等压无非体积功的可逆相变过程)
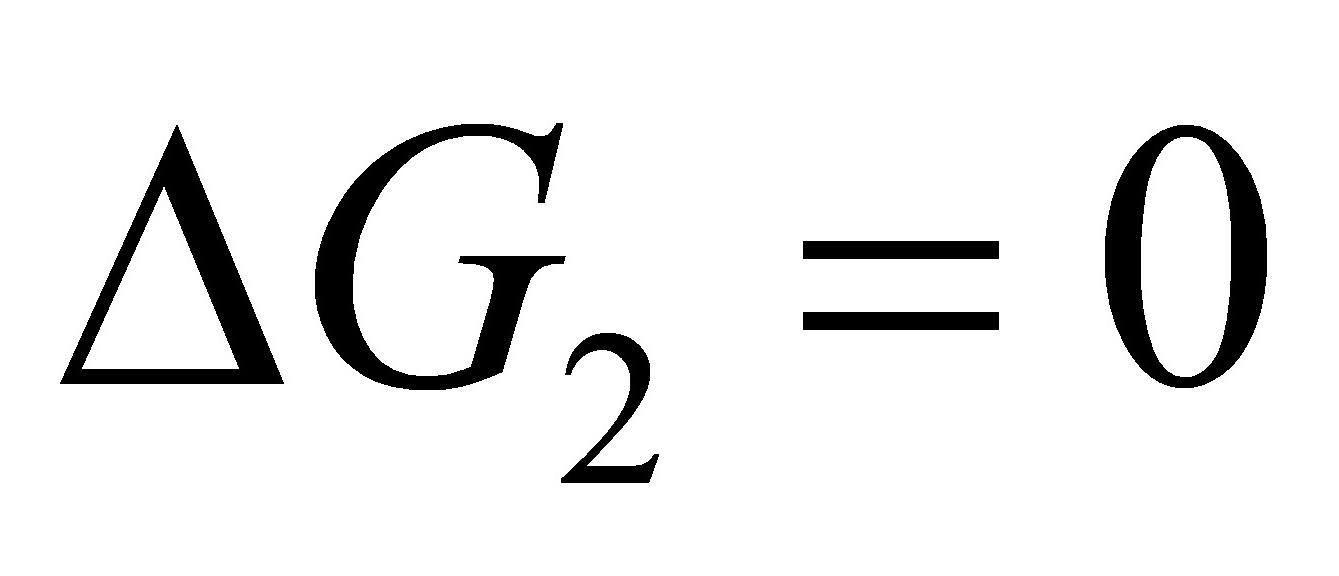
所以 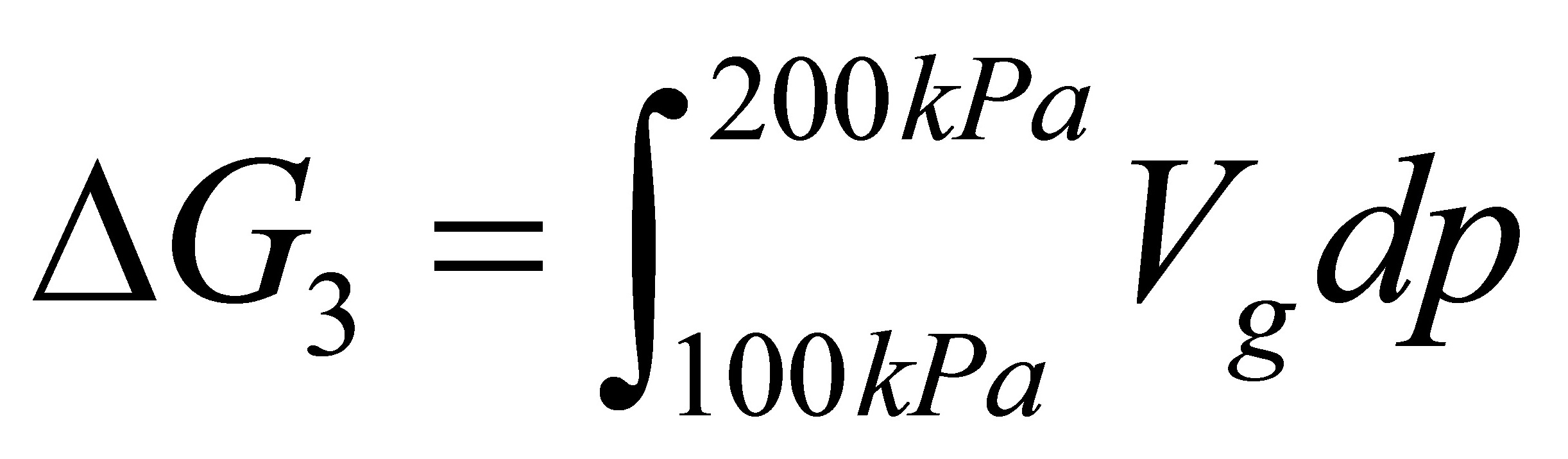
若水蒸气可看作理想气体,则
所以,在373K和200kPa压力下,HO(l)比HO(g)更稳定。
(2)设100kPa压力下设计如下可逆过程如下
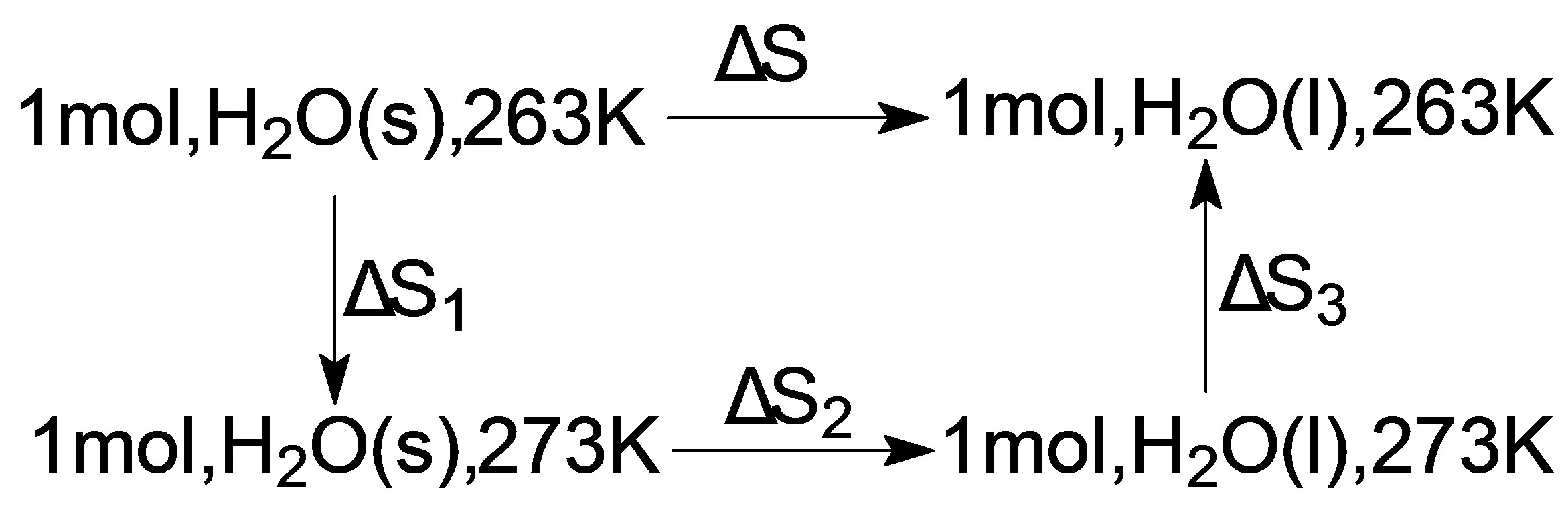
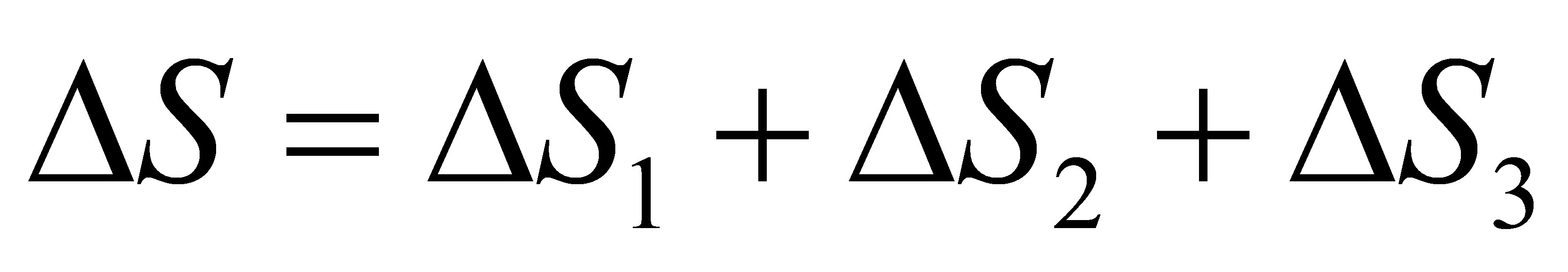 >0所以自发变化总是朝熵增加的方向进行,HO(s)比HO(l)更稳定。
>0所以自发变化总是朝熵增加的方向进行,HO(s)比HO(l)更稳定。
[19]在298K和100kPa压力下,已知C(金刚石)和C(石墨)的摩尔熵、摩尔燃烧焓和密度分别为:
试求:
(1)在298K及100kPa下,C(石墨)→C(金刚石)的;
(2)在298K及100kPa时,哪个晶体更为稳定?
(3)增加压力能否使不稳定晶体向稳定晶体转化?如有可能,至少要加多大压力,才能实现这种转化?
[解] (1)根据△G=△H-T△S
=-393.51kJ•mol-(-395.40kJ•mol)
=1.89kJ•mol-1
=2.45J•K•mol-5.71J•K•mol
=-3.26J•K-1•mol-1
=2.862kJ•mol
(2)因为298K,100kPa下,>0,说明此反应在该条件下不能自发向右进行,亦即石墨比较稳定.
(3)设298K下压力为p时石墨恰能变成金刚石
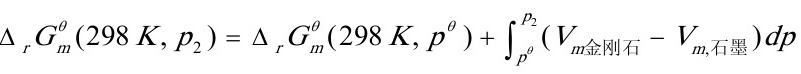 >0,解上式得:
>0,解上式得:
p>1.52×10Pa
即需要加压至1.52×102Pa时,才能在298K时,使石墨转化为金刚石.
[20]某实际气体的状态方程为,式中α为常数。设有1mol该气体,在温度为T的等温条件下,由p9可逆地变到p。试写出:Q,W,△U,△H,△S,△A及△G的计算表达式。
题目解答
答案
解: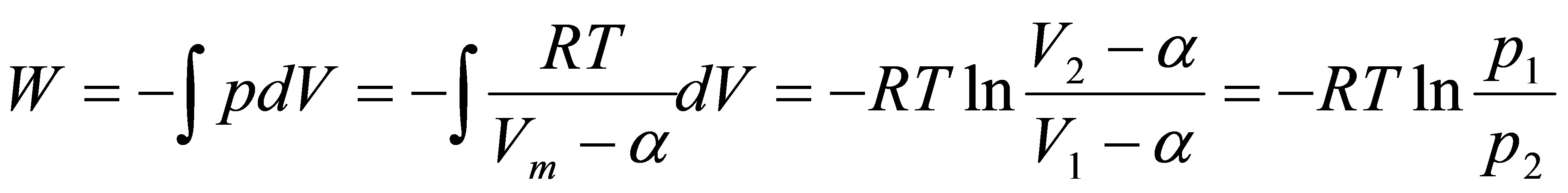
因为 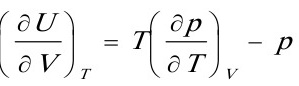 而
而 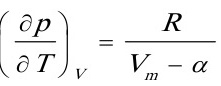
所以 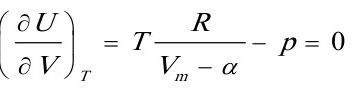
即该气体的等温过程 △U=0
Q=-W=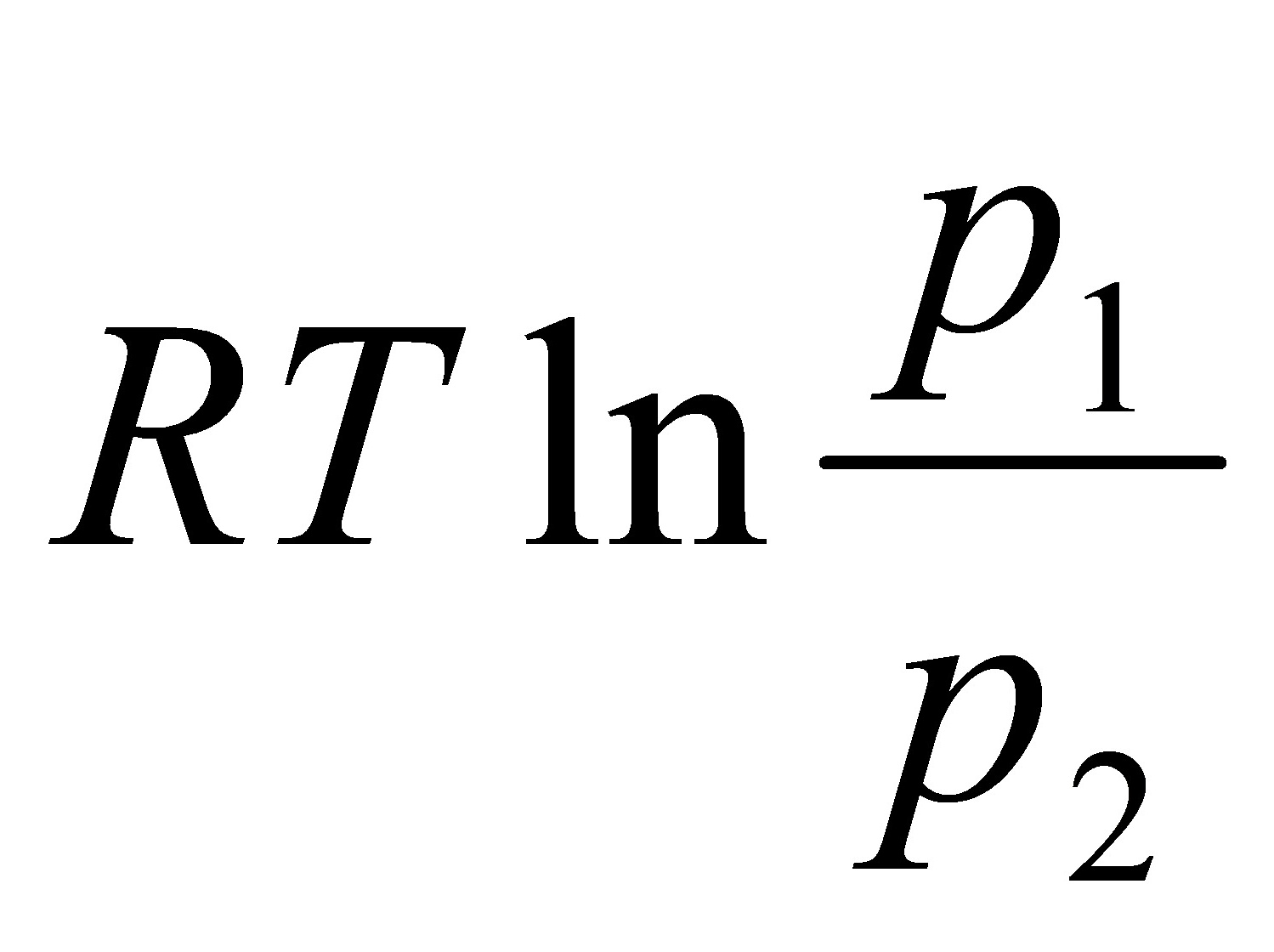
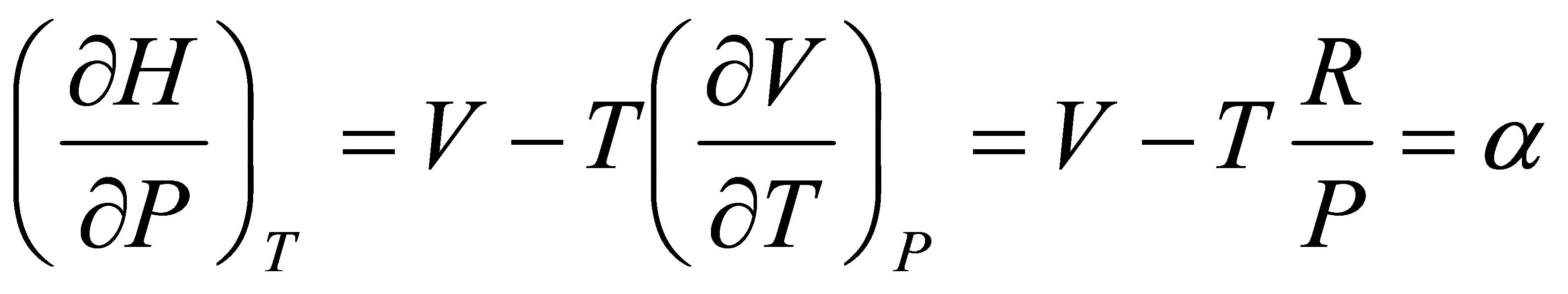
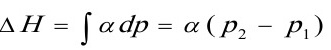
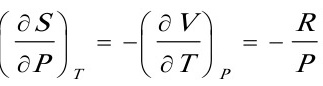
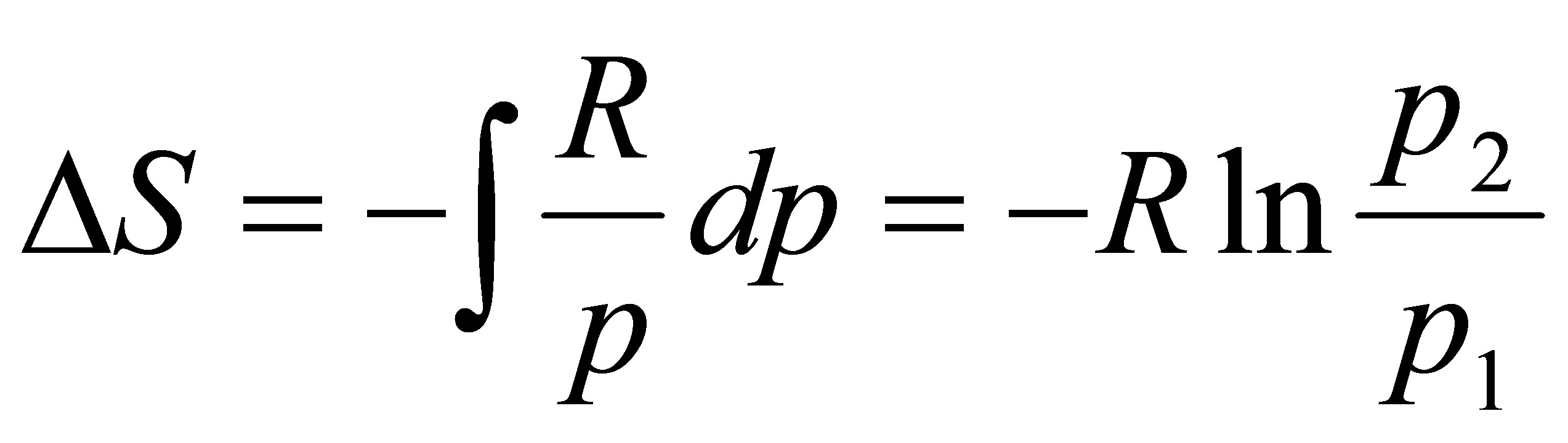
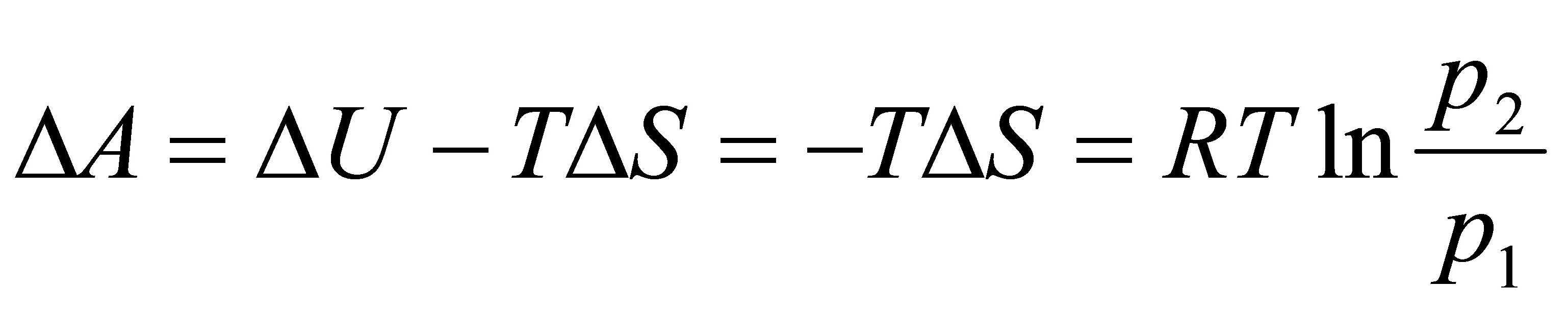
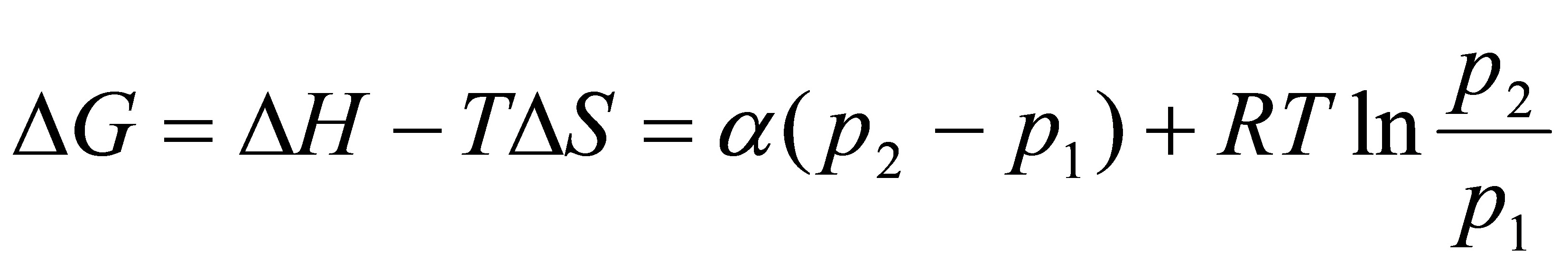
[21]在标准压力和298K时,计算如下反应的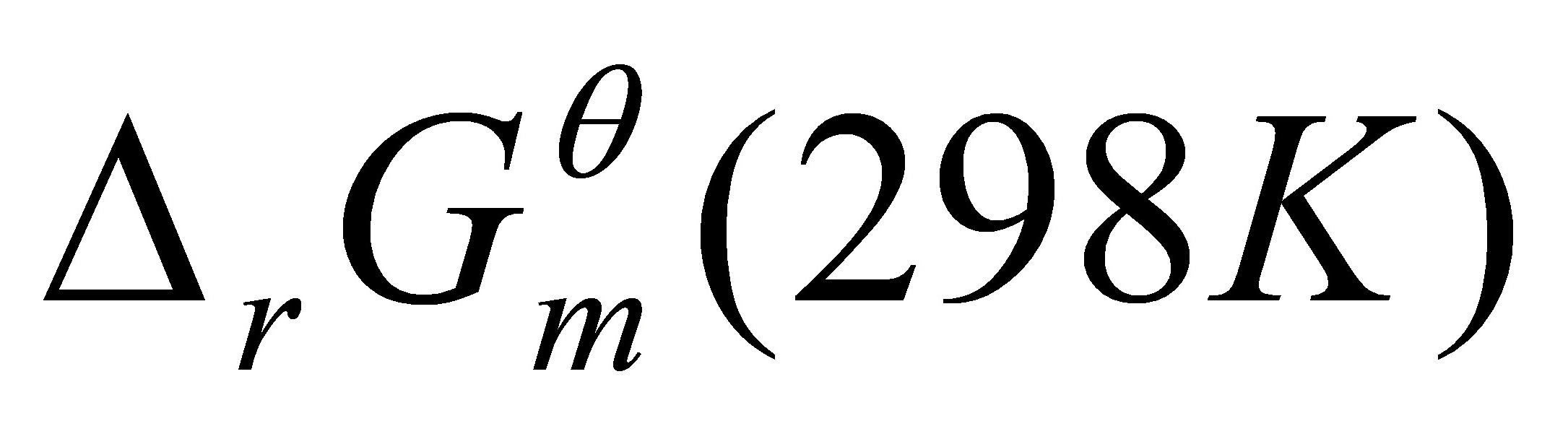 ,从所得数据值判断反应的可能性。
,从所得数据值判断反应的可能性。
(1) CH4(g)+1/2O2(g) →CH3OH(l)
(2) C(石墨)+2H2(g)+ 1/2O2(g)→CH3OH(l)
所需数据自己从热力学数据表上查阅。
[解]所查热力学数据如下:
物质 | CH4(g) | O2(g) | CH3OH(l) | H2(g) | C(石墨) |
-50.72 | -166.27 |
(1)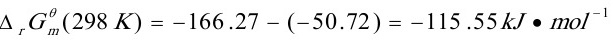
可见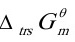 <0,说明此反应在该条件下能自发向右进行.
<0,说明此反应在该条件下能自发向右进行.
(2)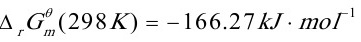
可见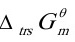 <0,说明此反应在该条件下能自发向右进行.
<0,说明此反应在该条件下能自发向右进行.
[22]计算下述催化加氢反应,在298K和标准压力下的熵变。
C2 H2 (g) + 2H2 (g) → C2 H6 (g)
已知C2 H2 (g),H2 (g),C2 H6 (g)在298K和标准压力下的标准摩尔熵分别为:200.8J•K-1•mol-1,,130.6J•K-1•mol-1,,229.5J•K-1•mol-1,.
[解] 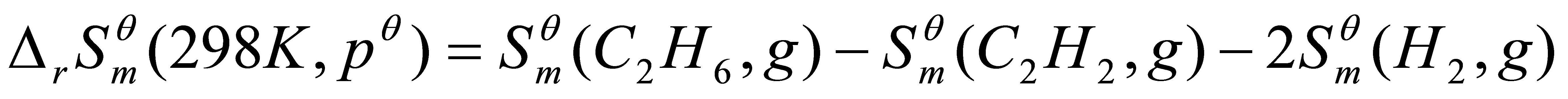
=229.5J•K-1•mol-1-200.8J•K-1•mol-1-2×130.6J•K-1•mol-1,
=-232.5J•K-1•mol-1
[23]若令膨胀系数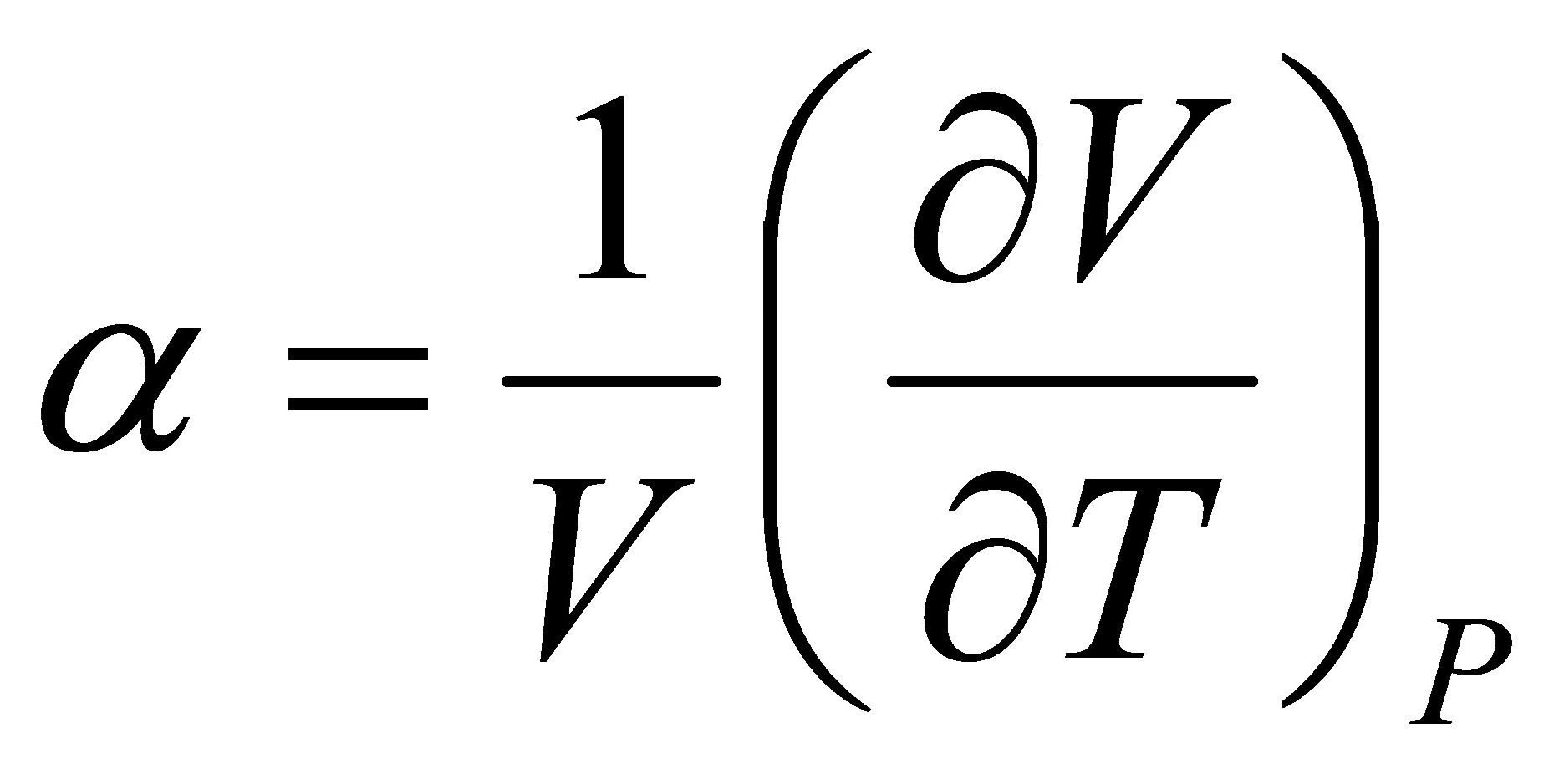 ,压缩系数
,压缩系数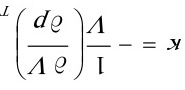 。试证明:
。试证明:
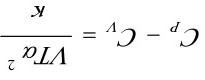
[证明]根据 的定义,及H=U+P V
的定义,及H=U+P V
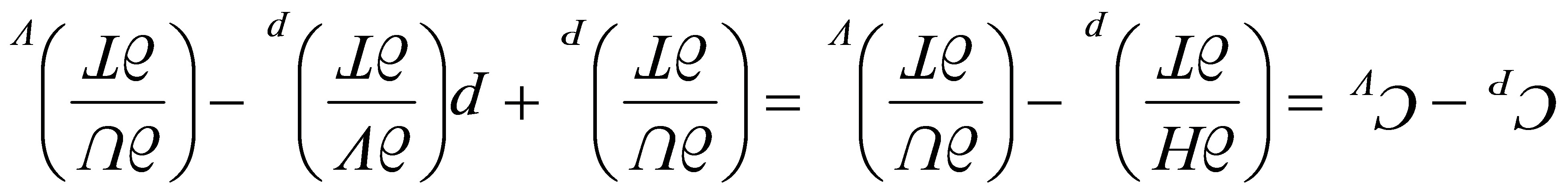
由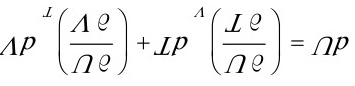
在恒压下对T求偏导得: 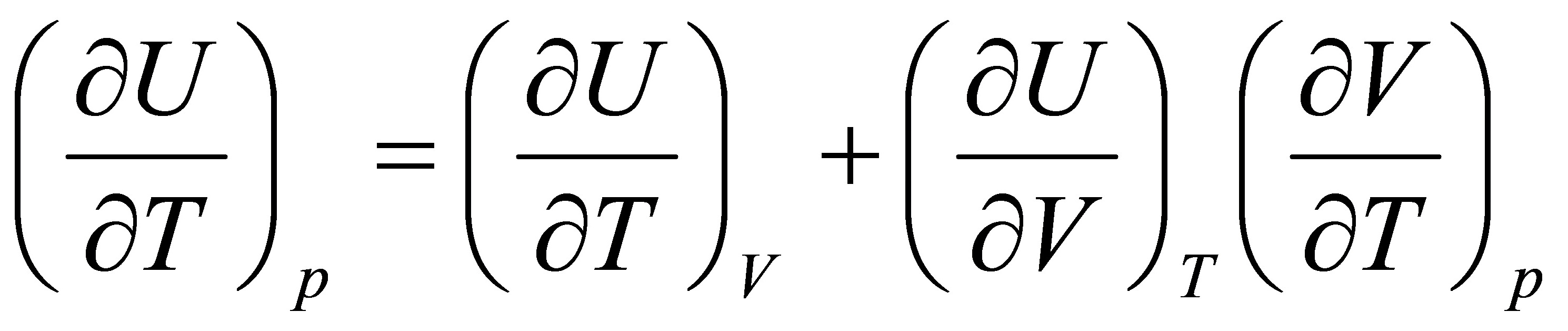
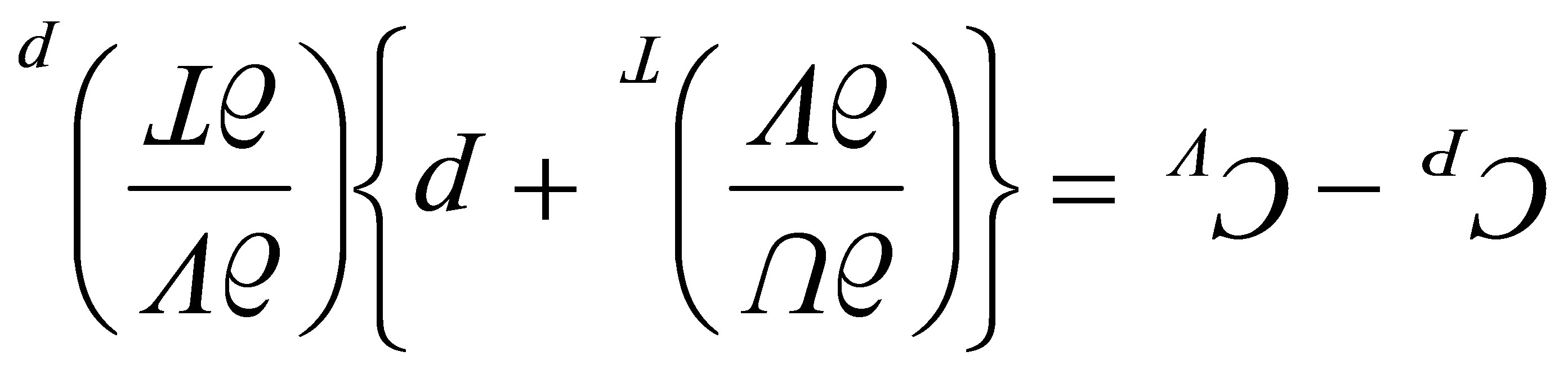 (1)
(1)
又因为 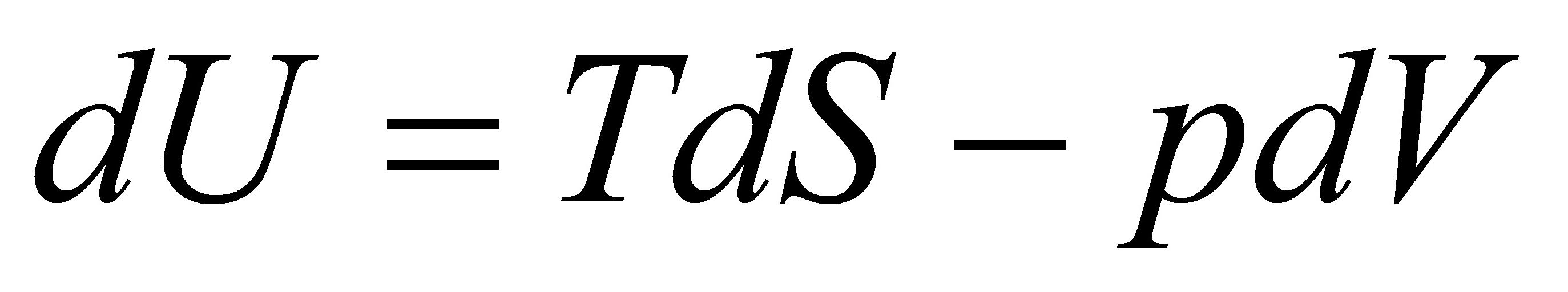
在恒温下对V求偏导得: 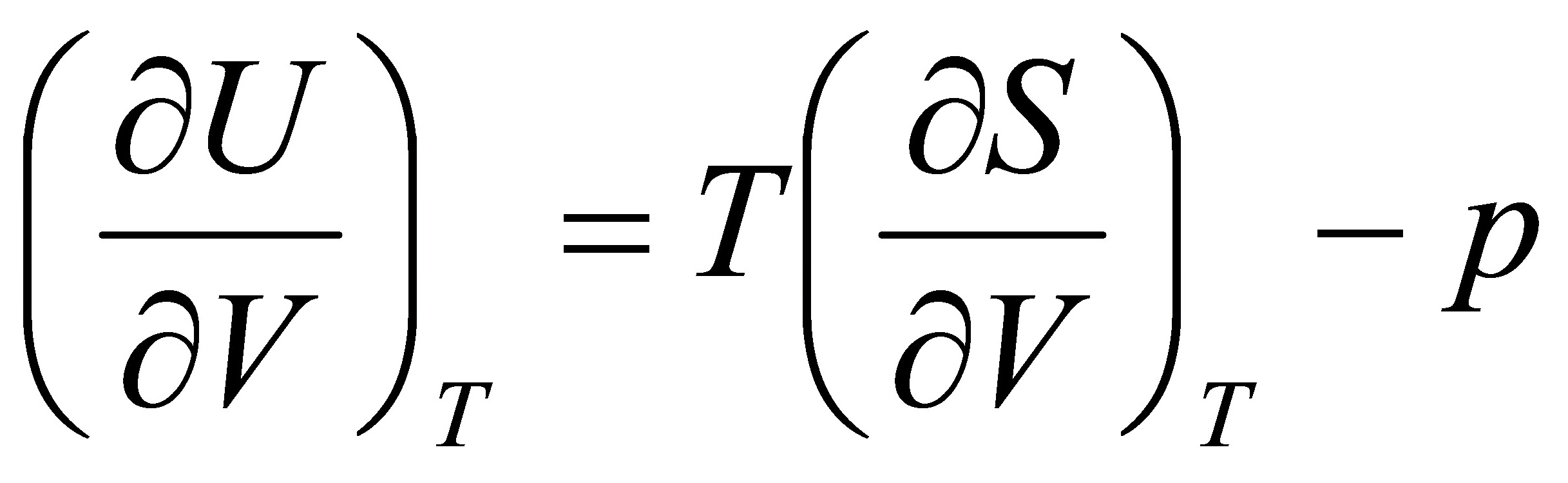 (2)
(2)
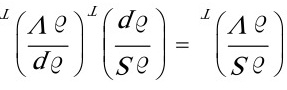
将麦克斯韦关系式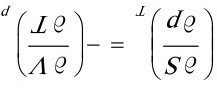 代入上式
代入上式
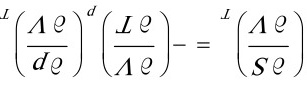 (3)
(3)
将(3)代入(2)得: 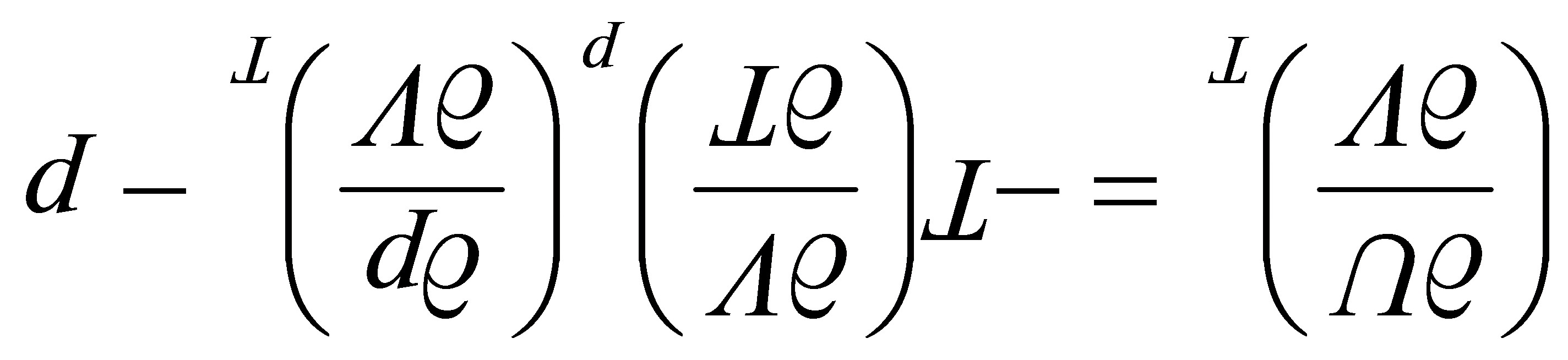 (4)
(4)
将(4)代入(1)得: 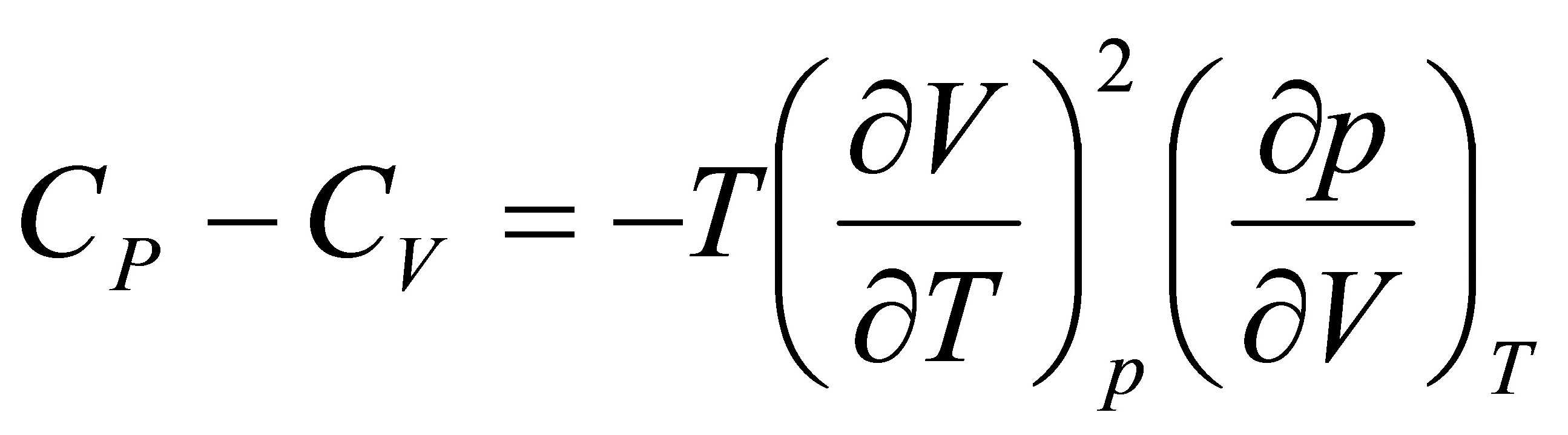
再将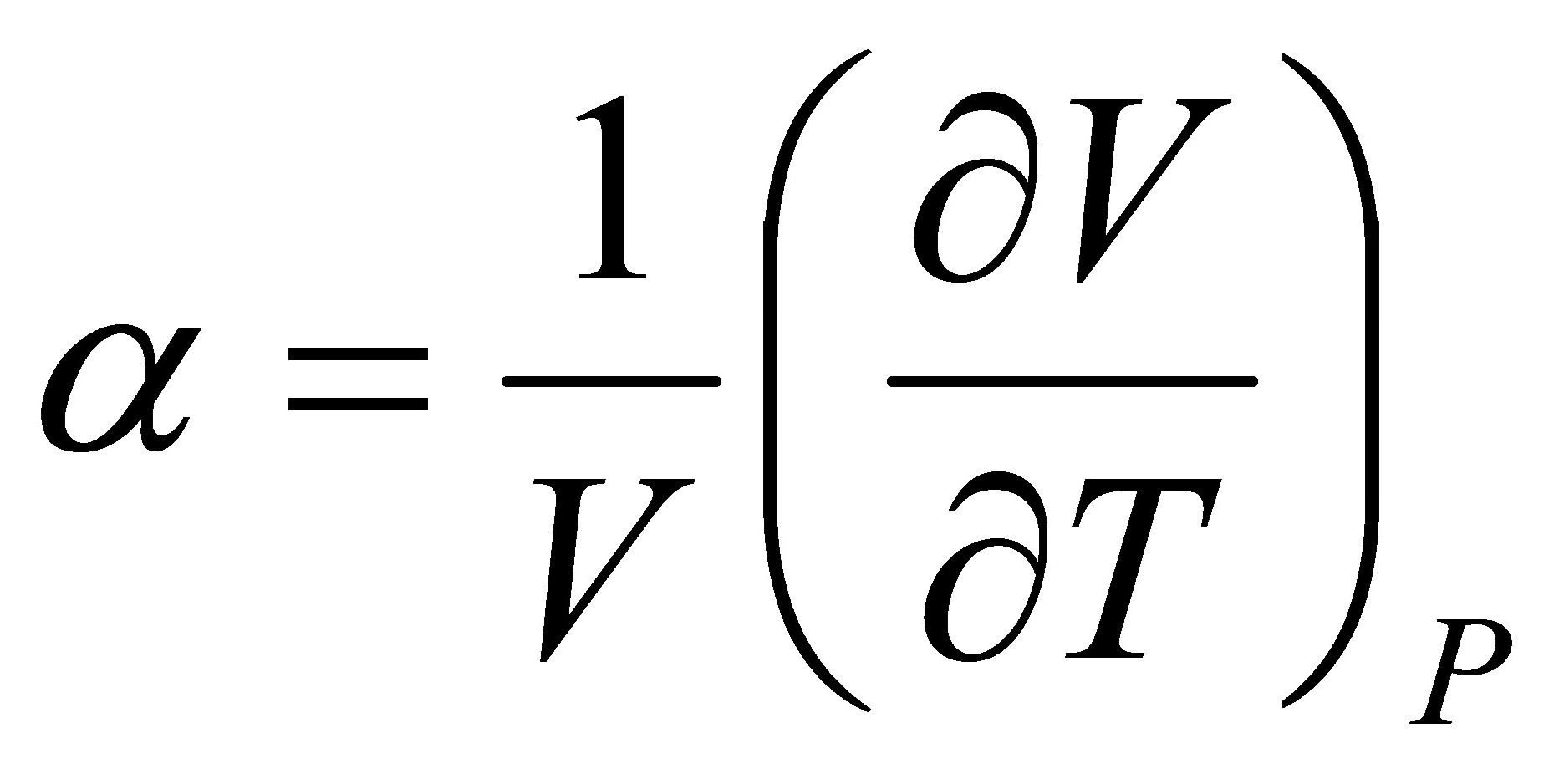 ,
, 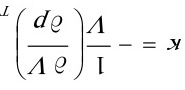 代入得:
代入得:
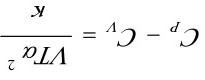
[24]对van der Waals实际气体,试证明: 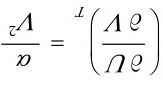
证明: van der Waals实际气体的状态方程式为
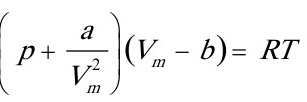
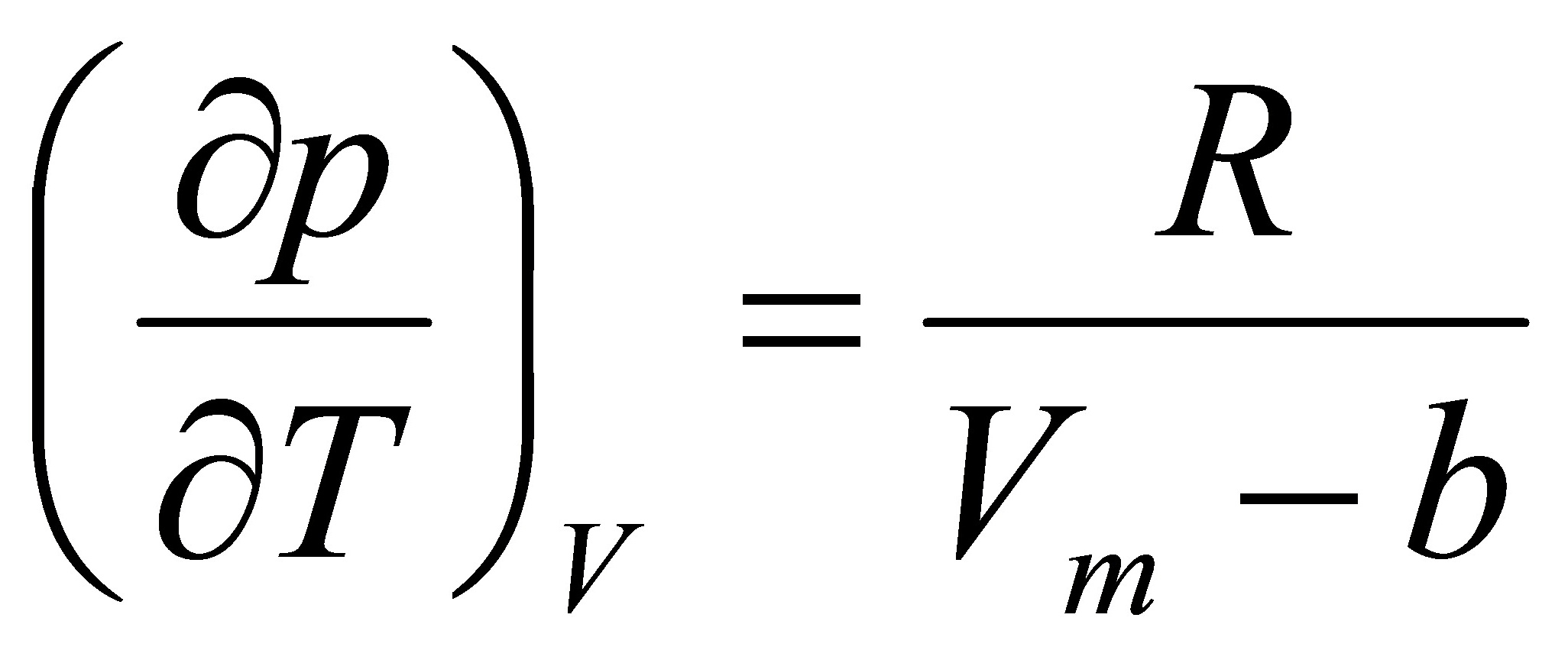
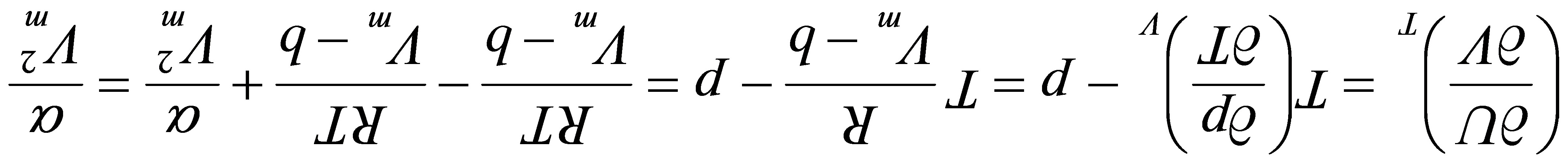
[25]对理想气体,试证明: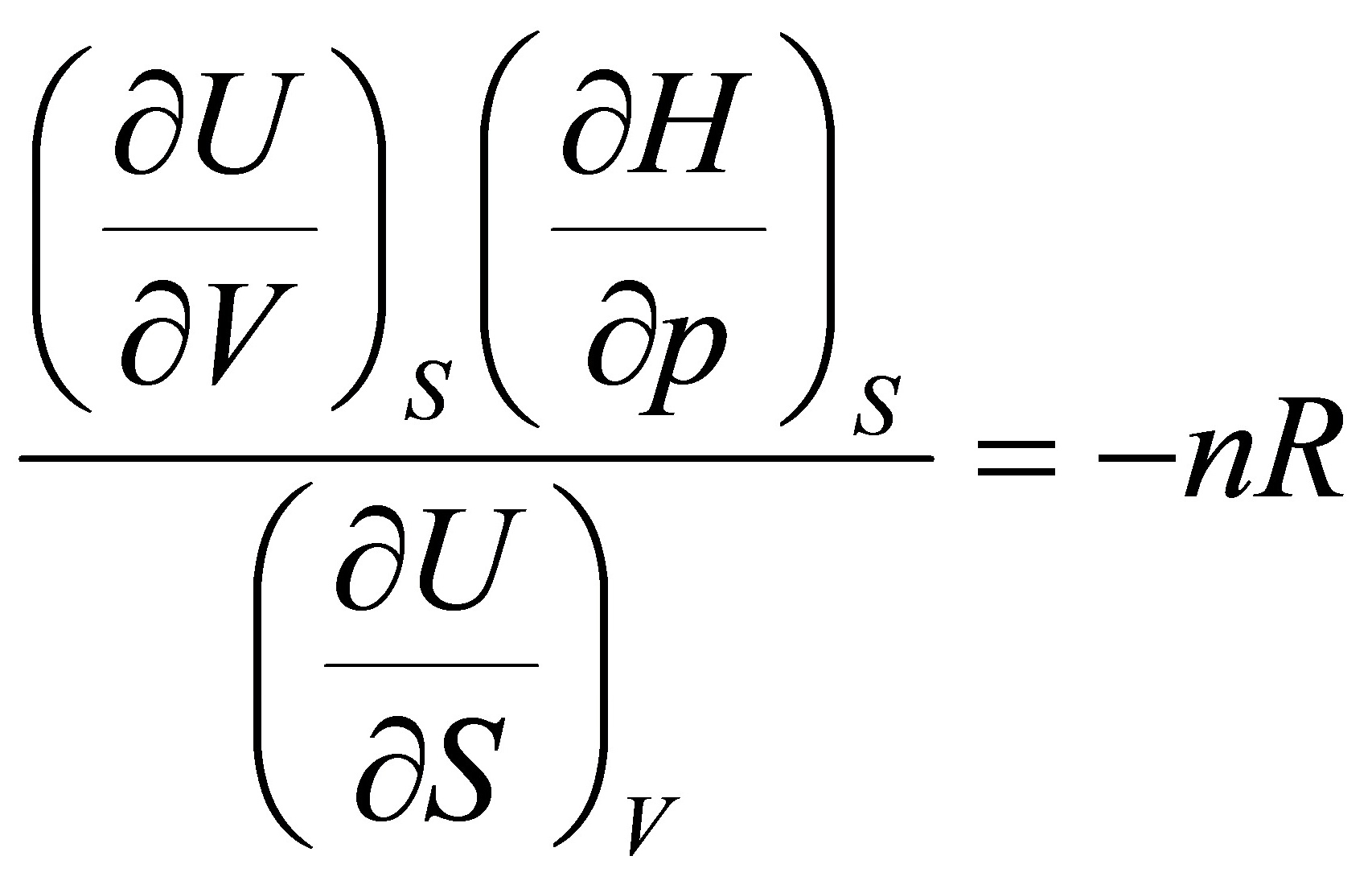
[证明] 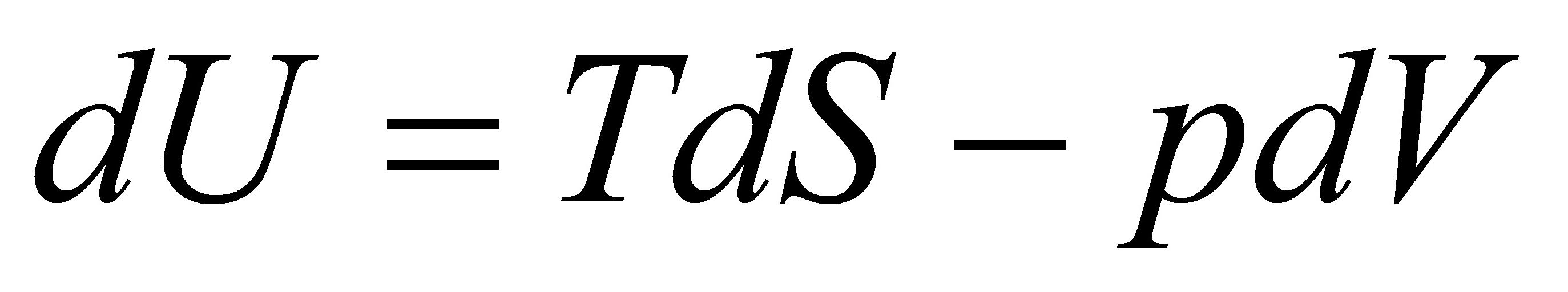
则 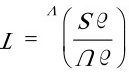
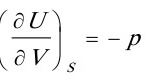
又 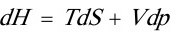
则 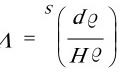
那么 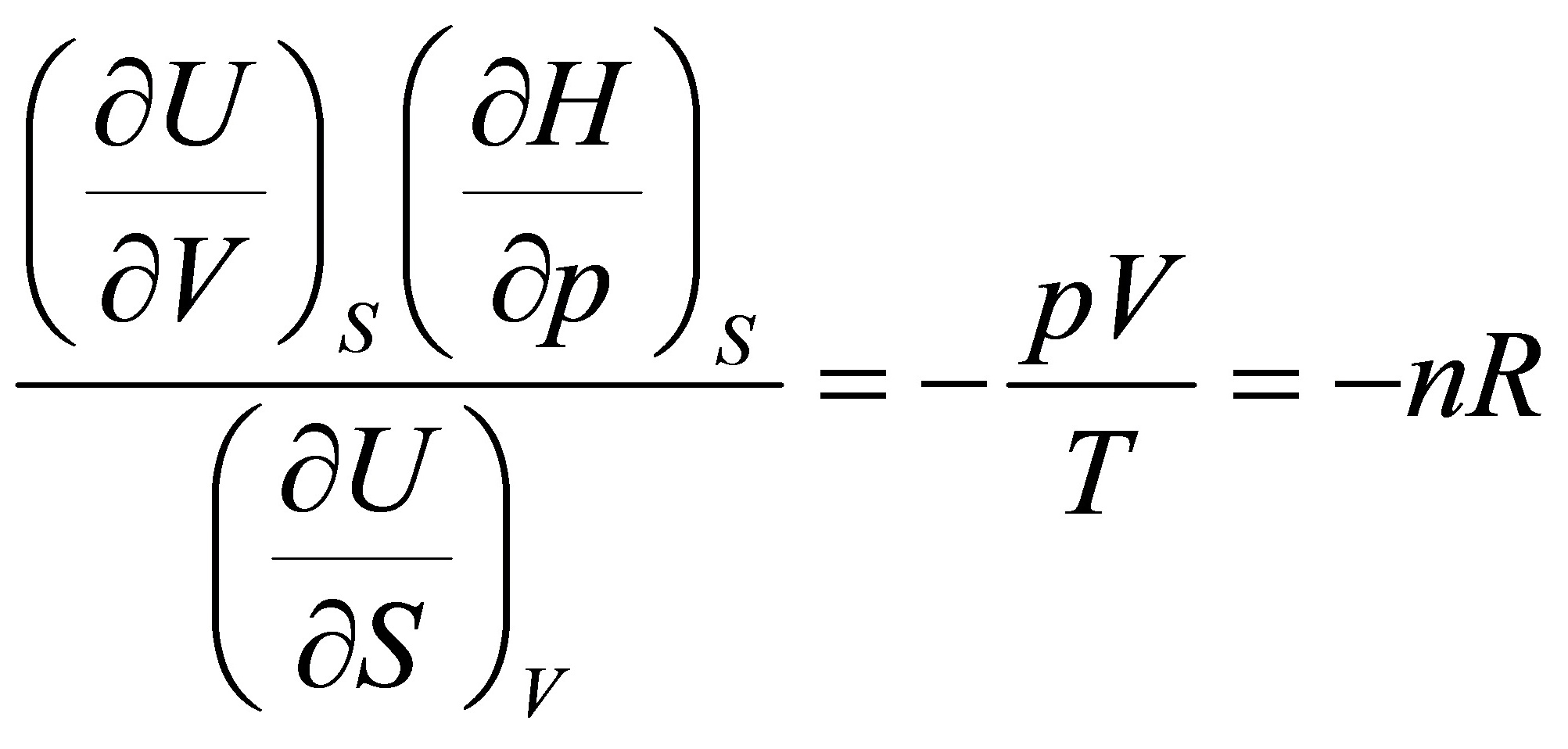
[26]在600K,100kPa压力下,生石膏的脱水反应为
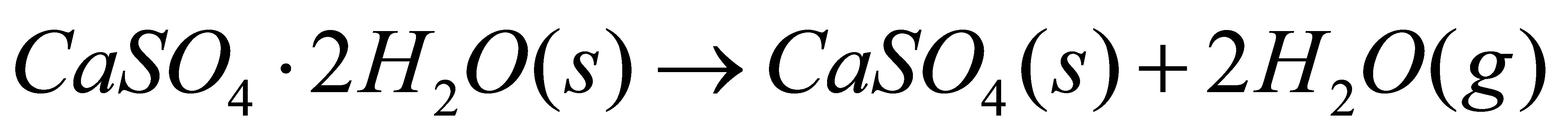
试计算:该反应进度为1mol时的Q,W,△Um,△Hm,△Sm,△Am及△Gm。已知各物质在298K,100kPa的热力学数据为:
物质 | |||
-2021.12 | 193.97 | 186.20 | |
-1432.68 | 106.70 | 99.60 | |
-241.82 | 188.83 | 33.58 |
[解]W=-P△V=-PV水=-2RT=-2×8.314J•K-1•mol-1×600K=-9.98kJ
在298K,100kPa时:
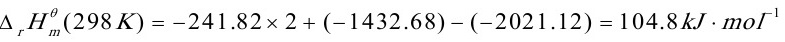
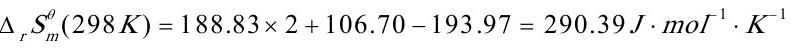
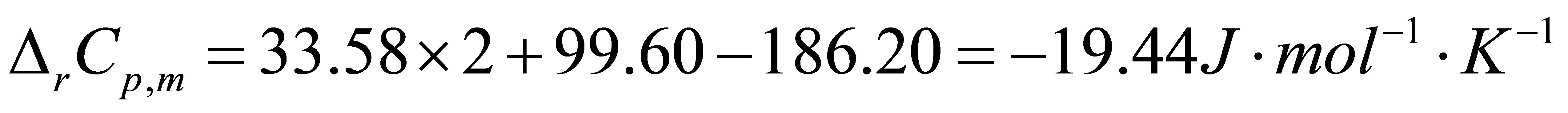
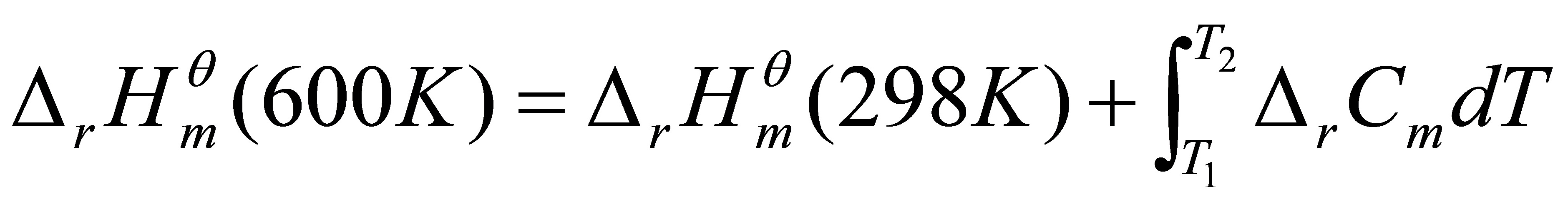
=104.8kJ•mol-1+(-19.44J•K-1•mol-1)(600K-298K)
=98.93kJ•mol-
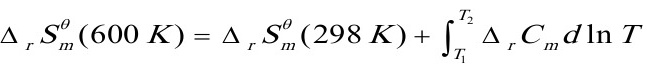
=290.39J•K-1•mol-1+(-19.44J•K-1•mol-1)ln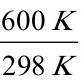
=276.79J•K-1•mol-1
△Um=△Hm+W=98.93kJ•mol--9.98kJ•mol-=88.95kJ•mol-
Q=△U-W=98.93kJ•mol-
△Am=△U-T△S=88.95kJ•mol-1-600K×276.79J•K-1•mol-1
=-77.124kJ•mol-1
△Gm=△H-T△S=98.93kJ•mol-1-600K×276.79J•K-1•mol-1
=-67.14kJ•mol-1
[27]将1mol固体碘I2(s)从298K,100kPa的始态,转变成457K,100kPa的I2(g),计算在457K时I2(g)的标准摩尔熵和过程的熵变。已知I2(s)在298K,100kPa时的标准摩尔熵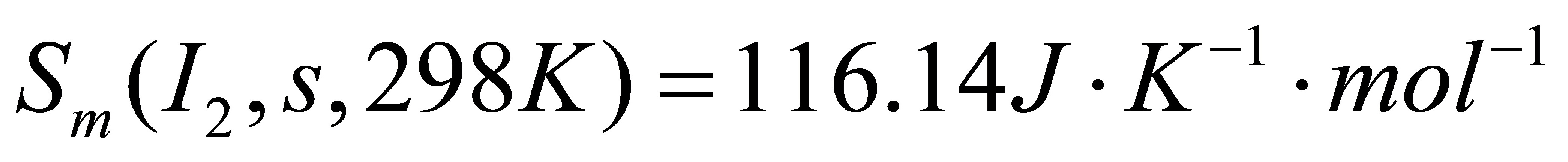 ,熔点为387K,标准摩尔熔化焓
,熔点为387K,标准摩尔熔化焓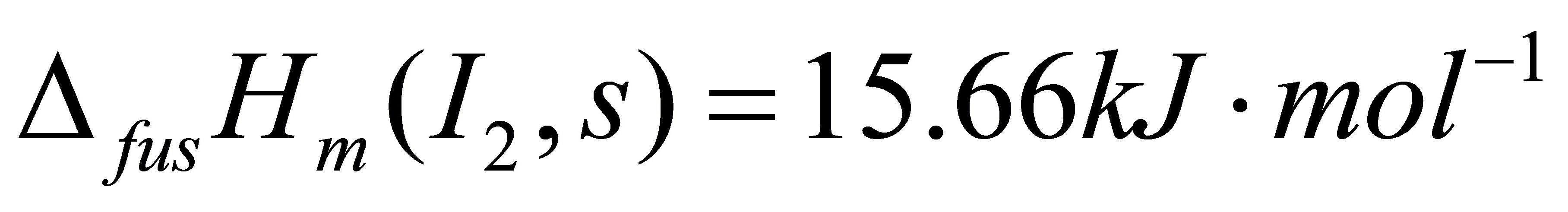 。设在298-378K的温度区间,固体与液体碘的摩尔比定压热容分别为
。设在298-378K的温度区间,固体与液体碘的摩尔比定压热容分别为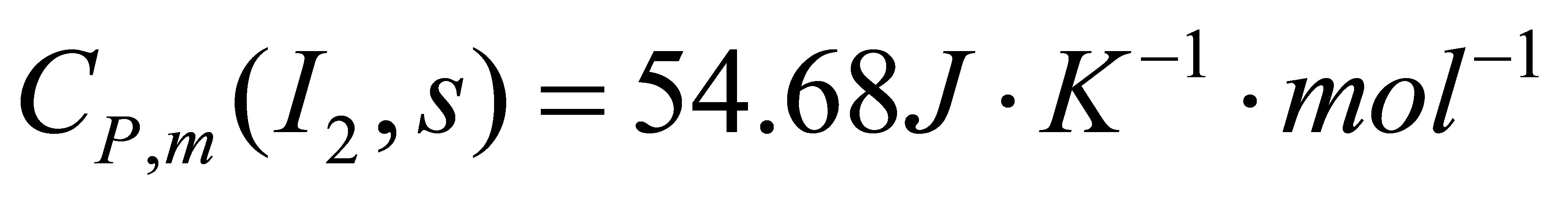 ,
,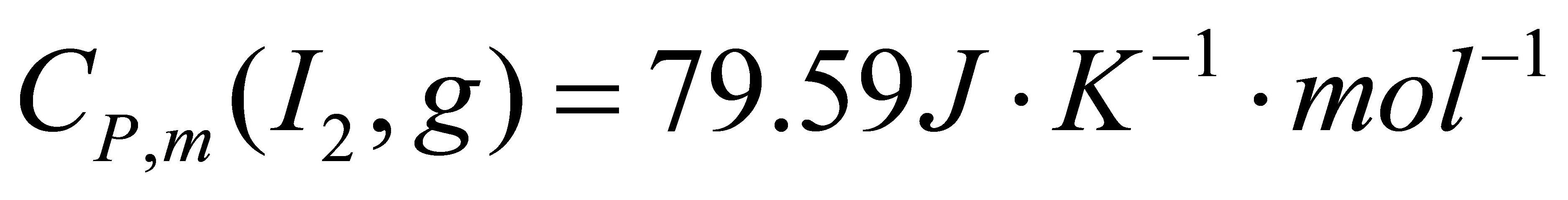 ,碘在沸点457K时的摩尔汽化焓为
,碘在沸点457K时的摩尔汽化焓为
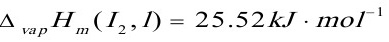 。
。
[解]设计可逆过程如下:
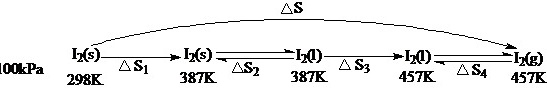
△S=△S1+△S2+△S3+△S4
=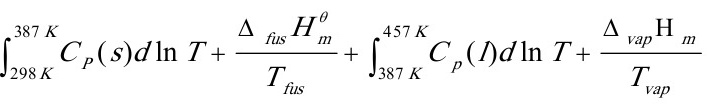
=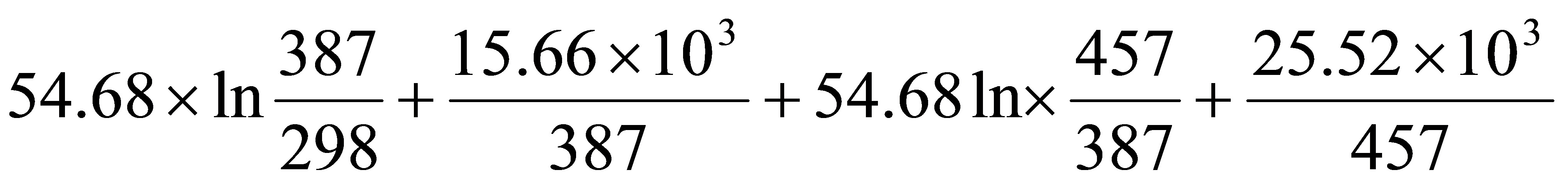
=123.82J•K-1•mol-1
又因为 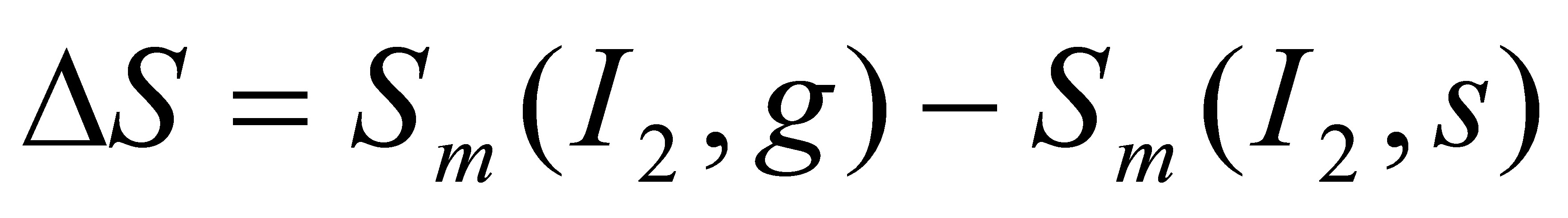
123.82J•K-1•mol-1=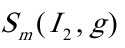 -116.14 J•K-1•mol-1
-116.14 J•K-1•mol-1
得: 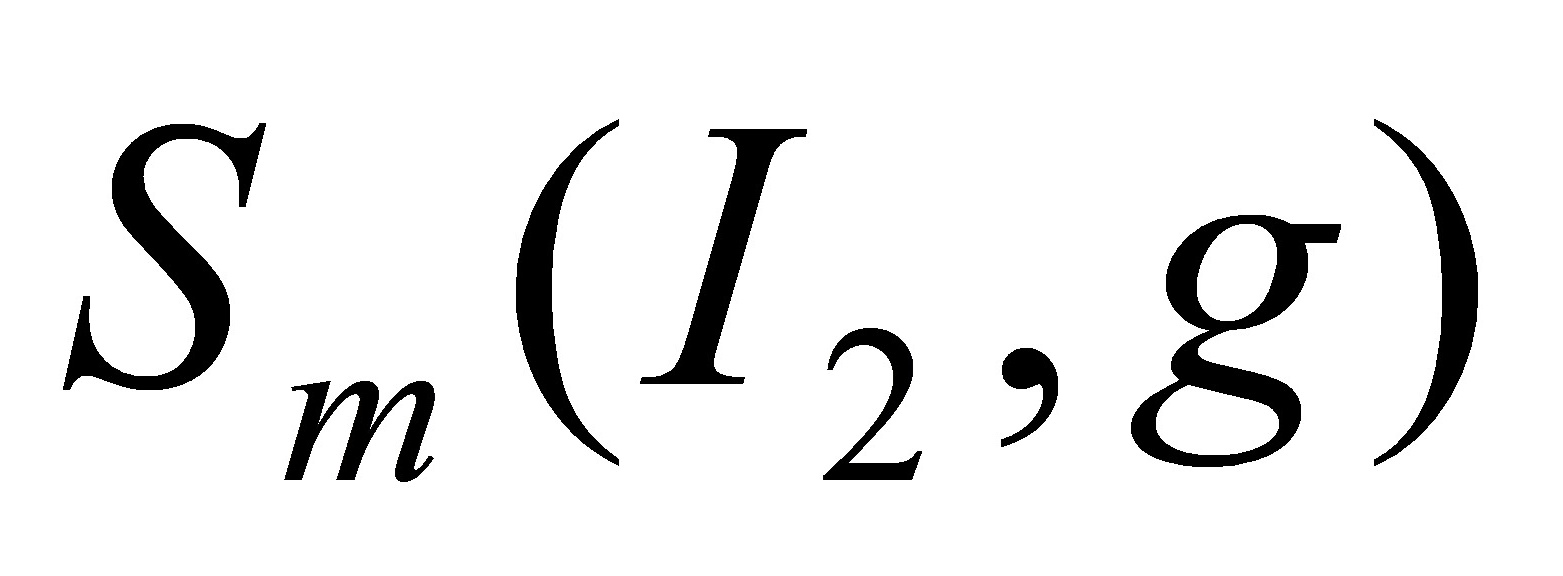 =239.96J•K-1•mol-1
=239.96J•K-1•mol-1
[28]保持压力为标准压力,计算丙酮蒸气在1000K时的标准摩尔熵值。已知在298K时丙酮蒸气的标准摩尔熵值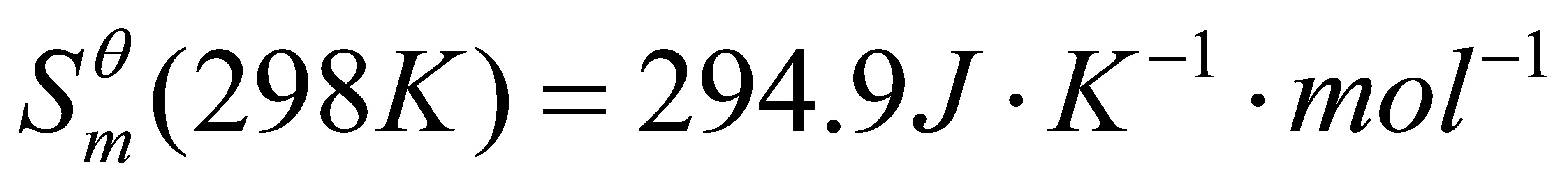 在273-1500K的温度区间,丙酮蒸气的定压摩尔热容
在273-1500K的温度区间,丙酮蒸气的定压摩尔热容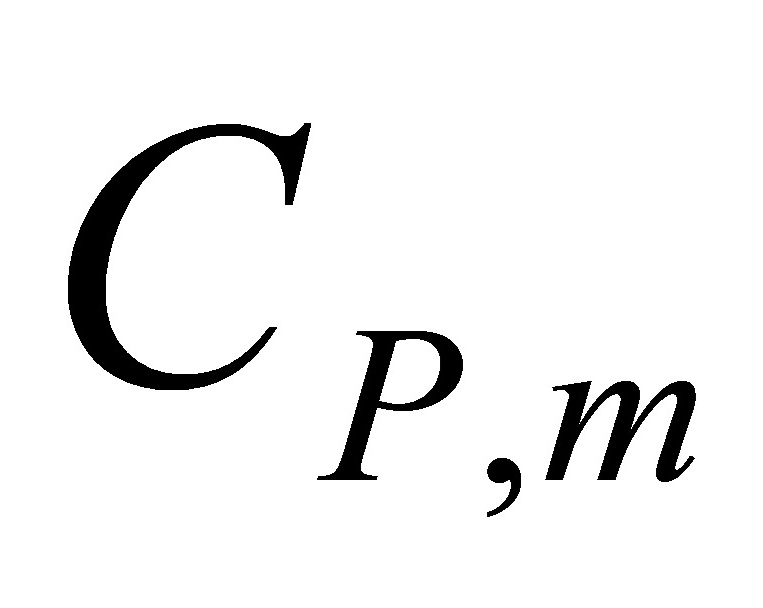 与温度的关系式为:
与温度的关系式为:
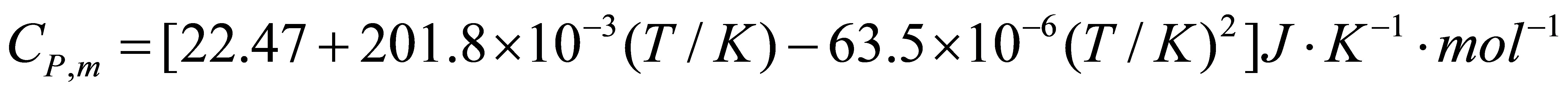
解:由于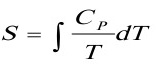
故 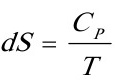
即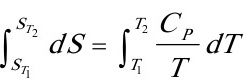
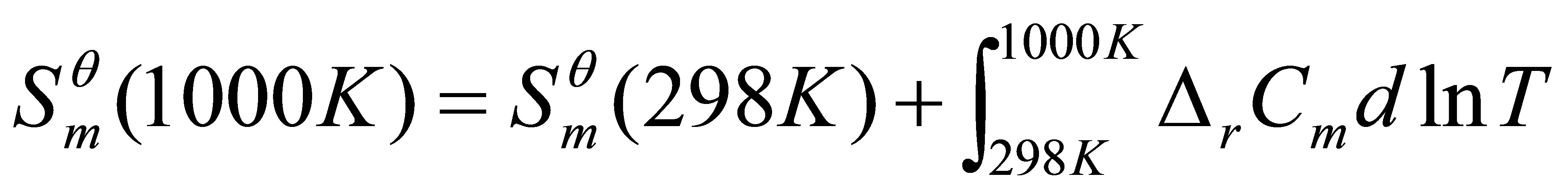
=434.8J•K-1•mol-1
(3)不正确,因为不可逆过程不一定是自发的,而自发过程的熵永不减少;所以必须在隔离体系中。不可逆过程的熵永不减少
(4)不正确。绝热体系或隔离体系达平衡时熵最大,等温等压不作非体积功的条件下,体系达平衡时Gibbs自由能最小。
(5)不正确,因为只有当系统的U和V恒定非体积功为0时,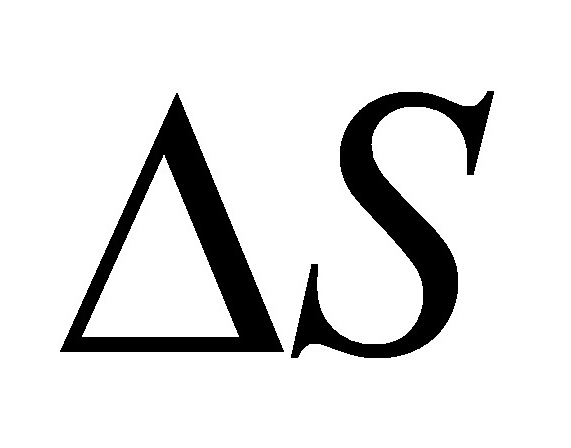 <0和
<0和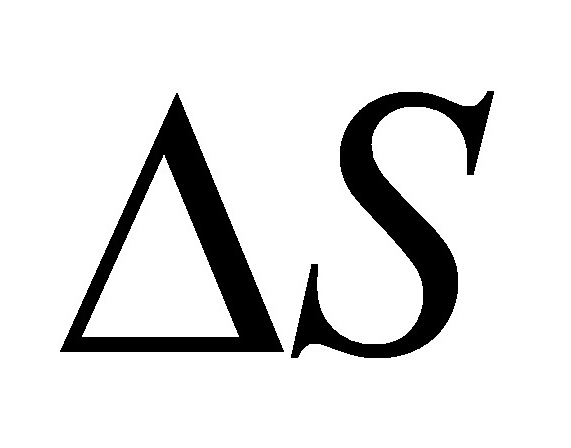 =0的过程不可能发生;
=0的过程不可能发生;
(6)不正确,根据熵增加原理,绝热不可逆过程的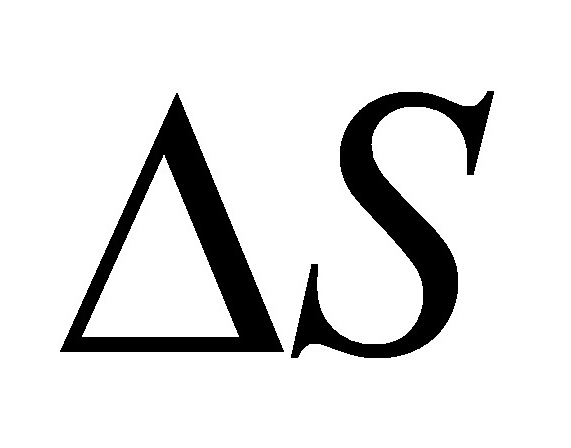 >0,而绝热可逆过程的
>0,而绝热可逆过程的 =0,从同一始态出发经历一个绝热不可逆过程的熵值和经历一个绝热可逆过程的熵值永不相等,不可能达到同一终态。
=0,从同一始态出发经历一个绝热不可逆过程的熵值和经历一个绝热可逆过程的熵值永不相等,不可能达到同一终态。
(7)正确,在绝热系统中,发生了一个不可逆过程,从状态1变到了状态2, >0,S2>S1,仍然在绝热系统中,从状态2出发,无论经历什么过程,体系的熵值有增无减,所以永远回不到原来状态了。
>0,S2>S1,仍然在绝热系统中,从状态2出发,无论经历什么过程,体系的熵值有增无减,所以永远回不到原来状态了。
(8)不正确,Kelvin的说法是不可能从单一的热源取出热使之变为功而不留下其它变化。关键是不留下其它变化,理想气体的等温膨胀时热全部变成了功,,体积增大了,环境的体积缩小的,留下了变化,故原来的说法不违反Kelvin的说法。
(9)不正确,Clausius的说法是不可能把热从低温热源传到高温热源而不引起其它变化。冷冻机可以从低温热源吸热放给高温热源时环境失去了功,得到了热引起了变化,故原来的说法不违反Clausius的说法。
(10)不正确,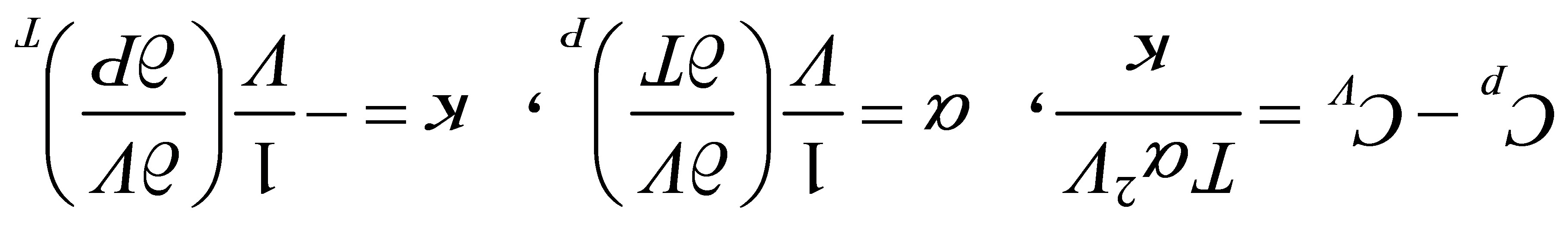 因为
因为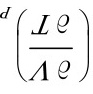 >0,
>0,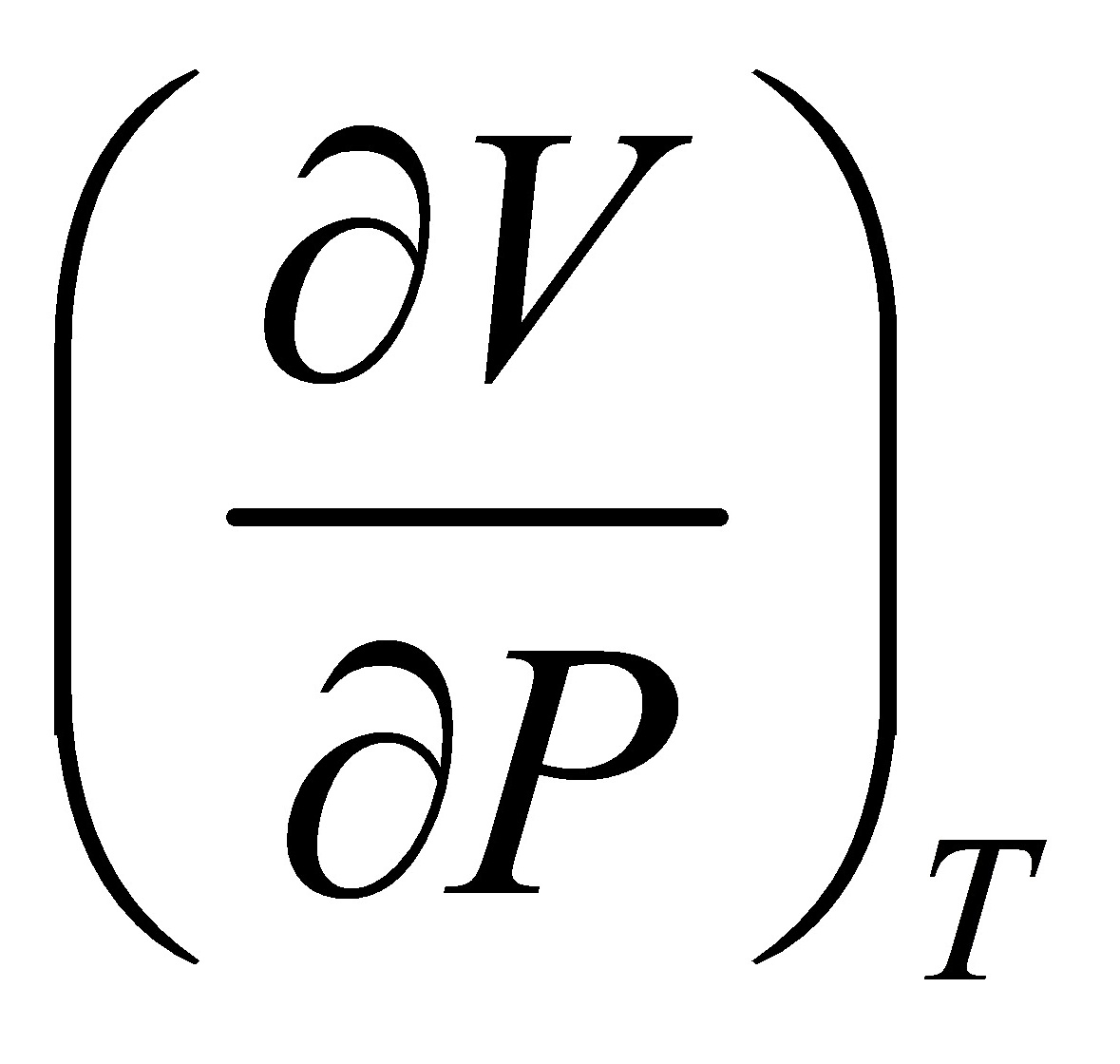 <0,即
<0,即 >0,
>0, >0,则
>0,则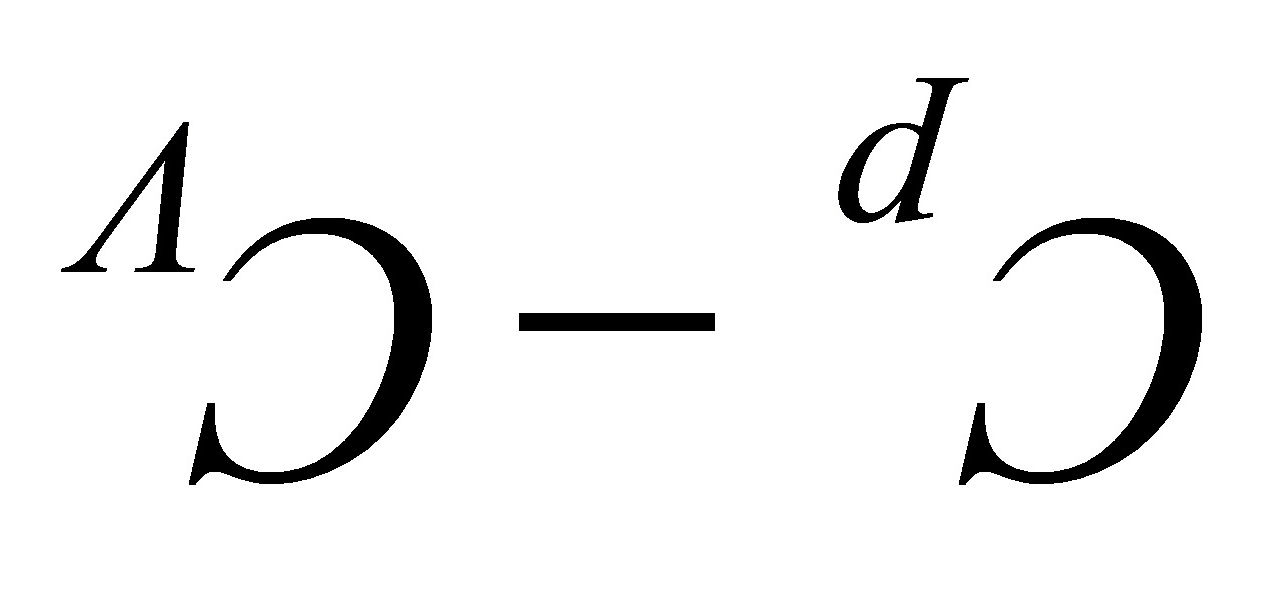 >0,
>0,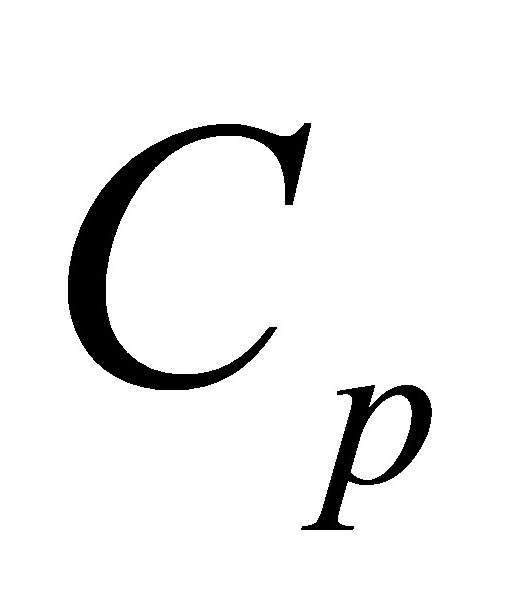 恒大于
恒大于 。但有例外,如对277.15K的水,
。但有例外,如对277.15K的水,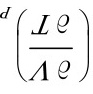 =0,此时
=0,此时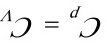 。
。
[3]指出下列各过程中,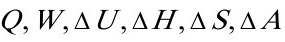 和
和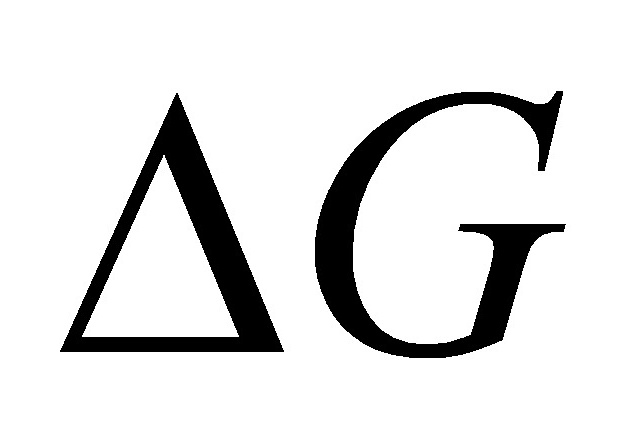 等热力学函数的变量哪些为零,哪些绝对值相等?
等热力学函数的变量哪些为零,哪些绝对值相等?
(1)理想气体真空膨胀;
(2)理想气体等温可逆膨胀;
(3)理想气体绝热节流膨胀;
(4)实际气体绝热可逆膨胀;
(5)实际气体绝热节流膨胀;
(6)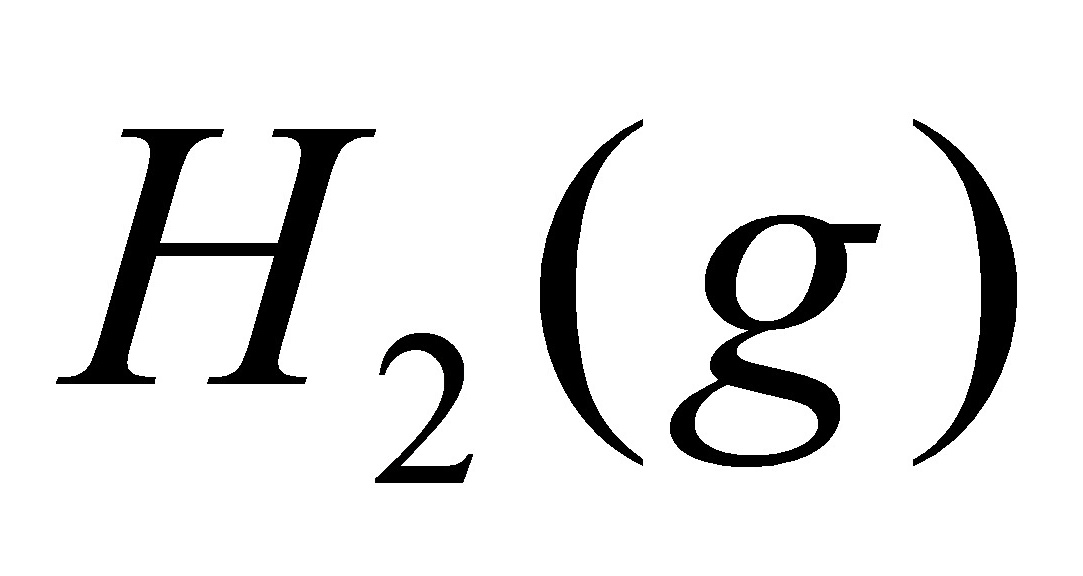 和
和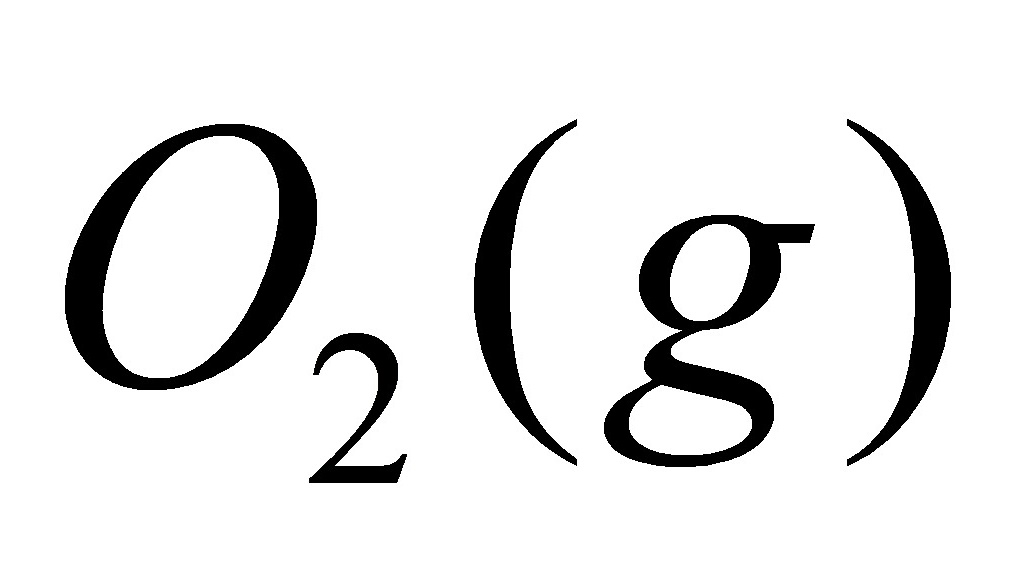 在绝热钢瓶中发生反应生成水;
在绝热钢瓶中发生反应生成水;
(7)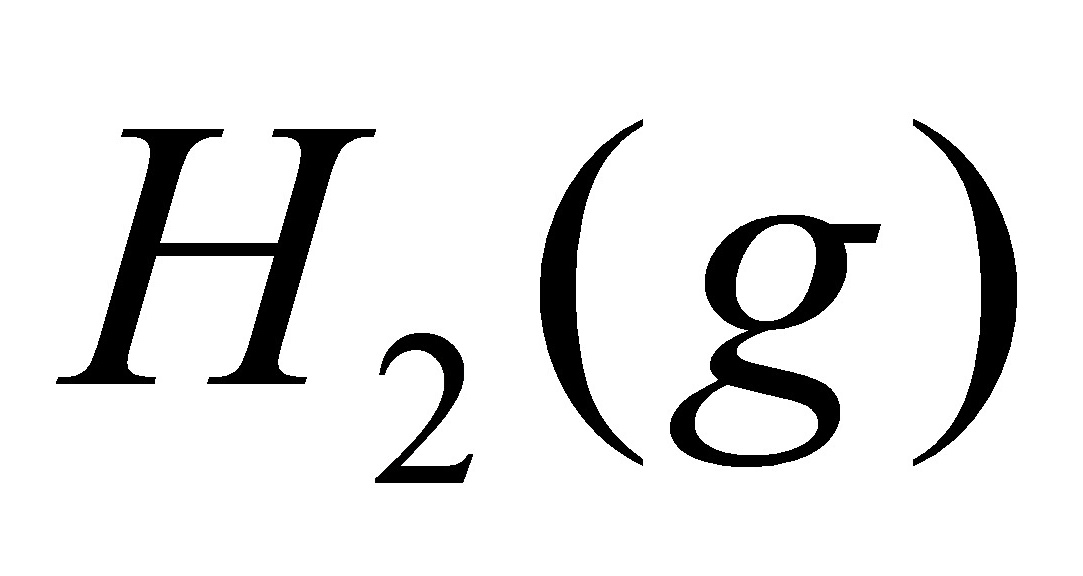 和
和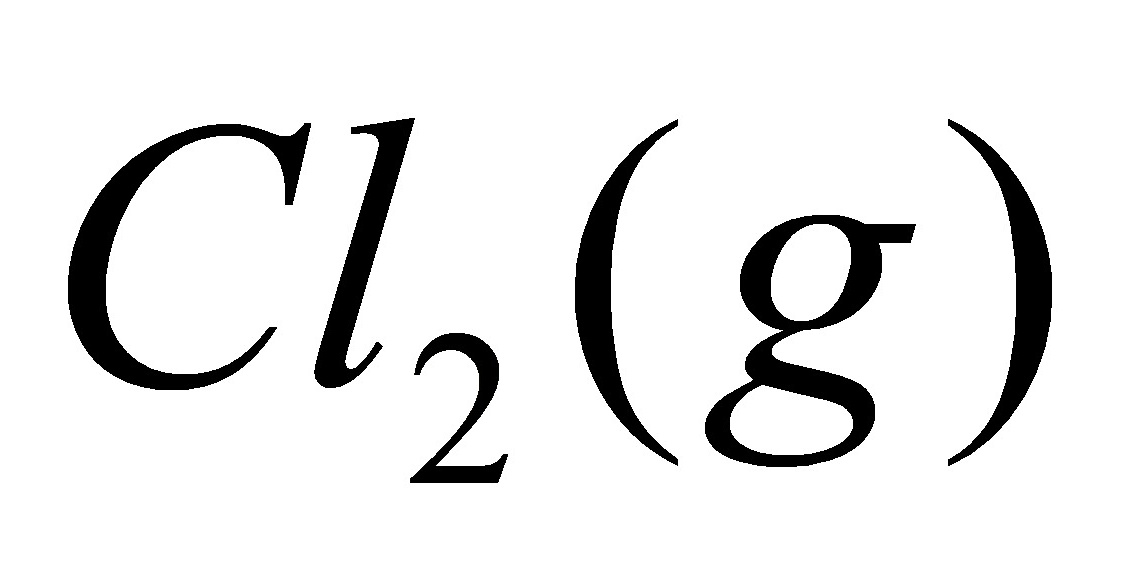 在绝热钢瓶中发生反应生成
在绝热钢瓶中发生反应生成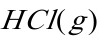 ;
;
(8)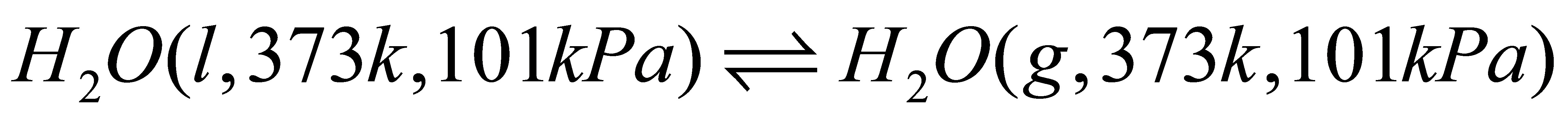 ;
;
(9)在等温、等压、不作非膨胀功的条件下,下列反应达到平衡
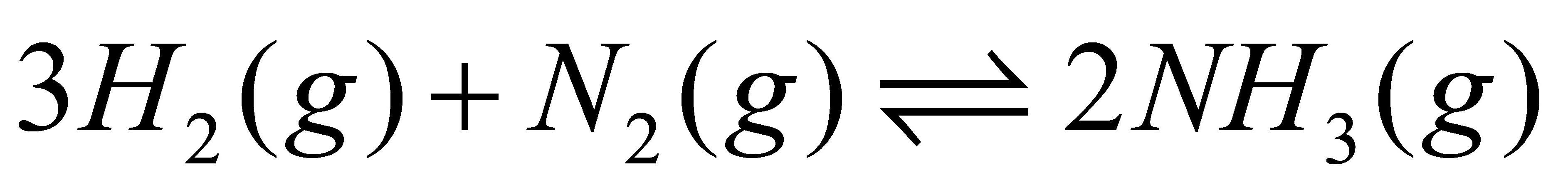
(10)绝热、恒压、不作非膨胀功的条件下,发生了一个化学反应。
[解](1)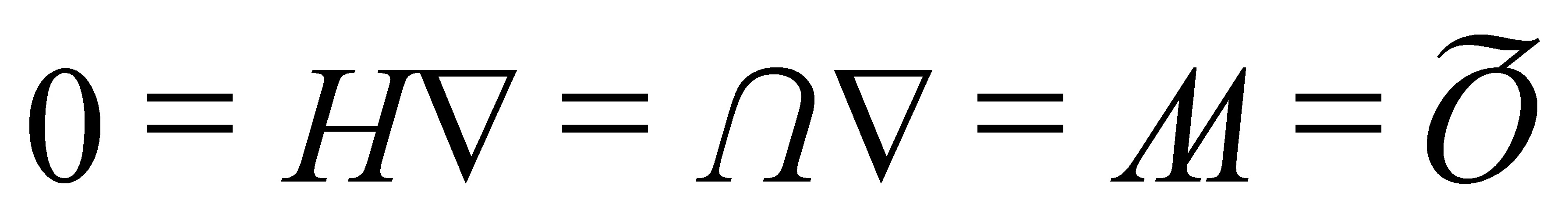
(2)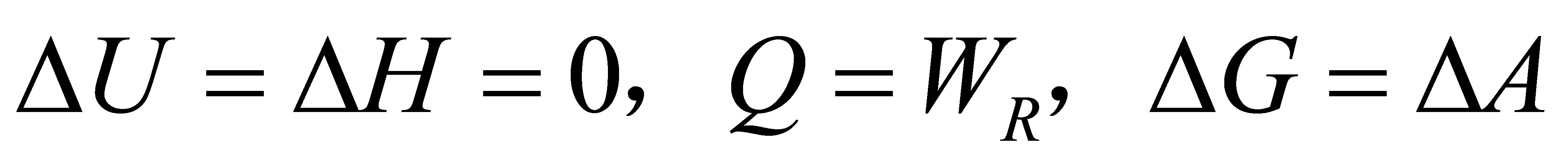 ,
,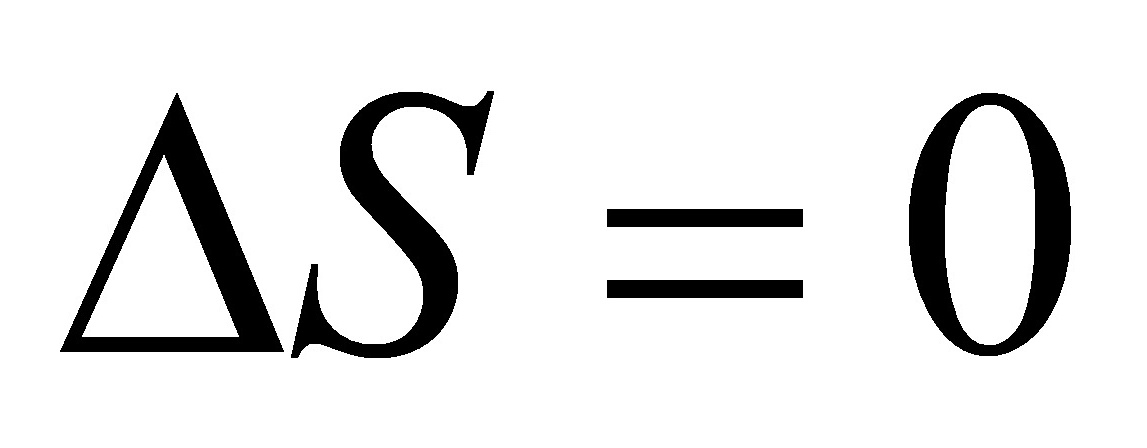
(3)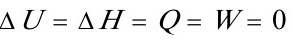
(4)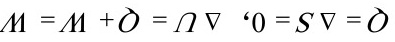
(5)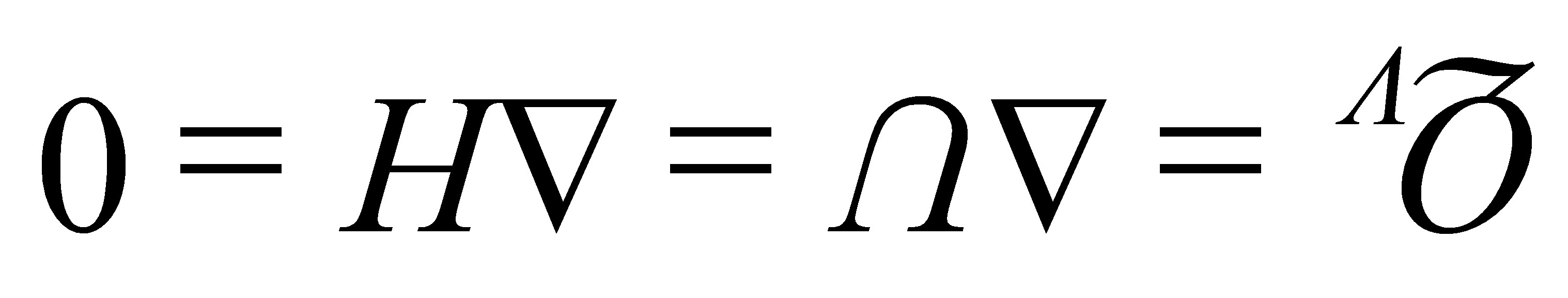
(6)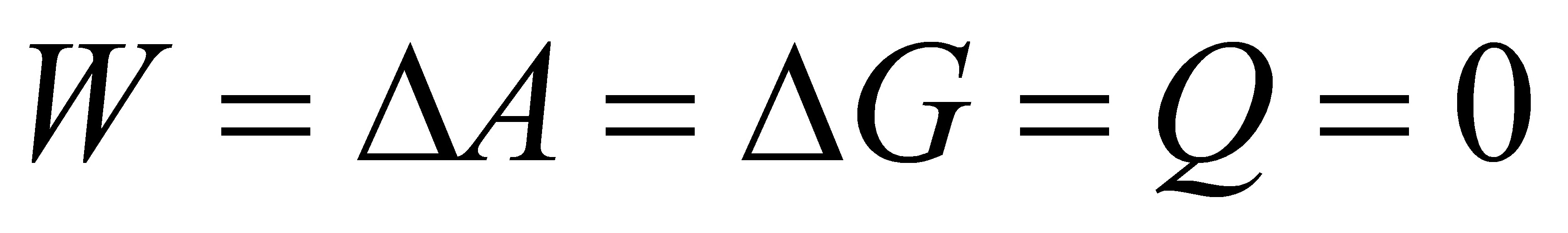
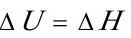
(7)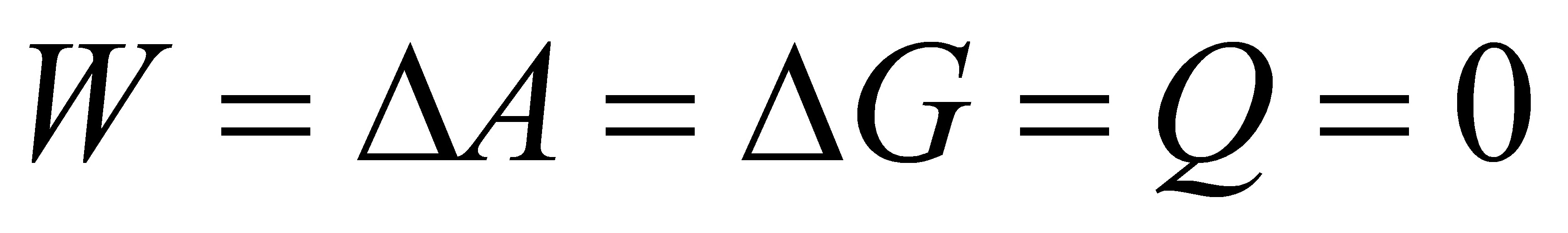
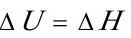
(8)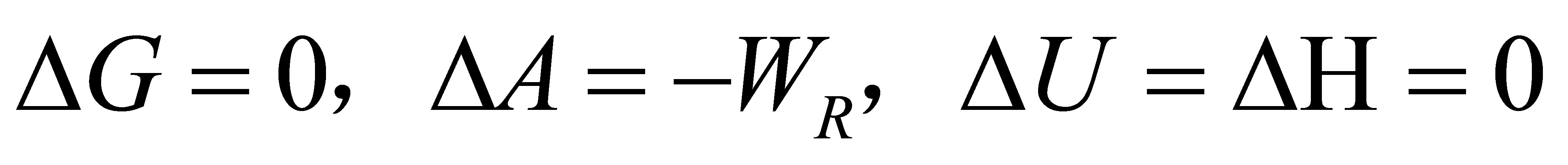 ;
;
(9)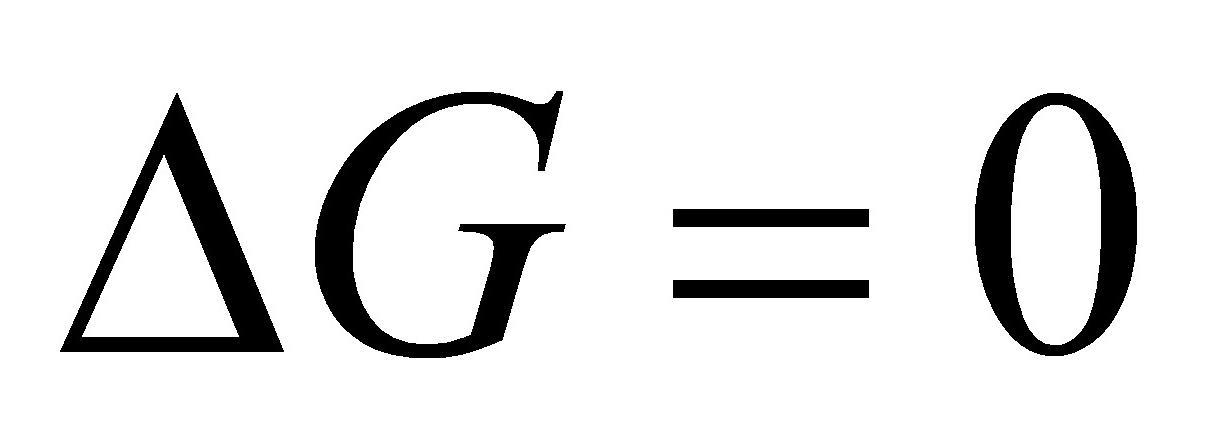 ;
;
(10)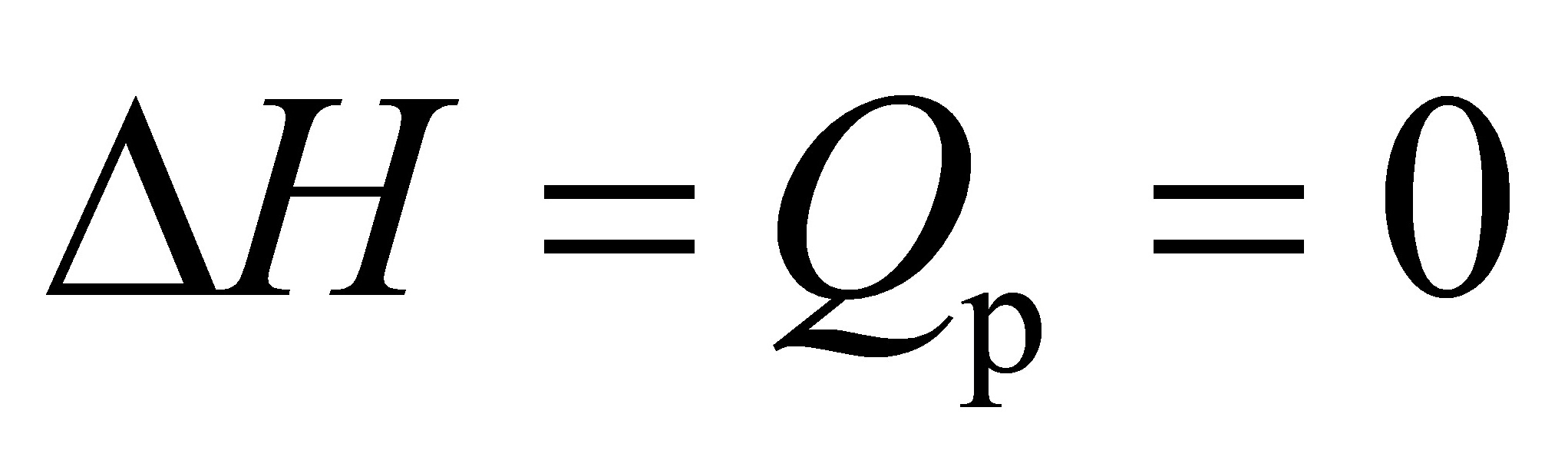
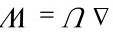
[4]将不可逆过程设计为可逆过程。
(1)理想气体从压力为p1向真空膨胀为p2;
(2)将两块温度分别为T1,T2的铁块(T1>T2)相接触,最后终态温度为T
(3)水真空蒸发为同温、同压的气,设水在该温度时的饱和蒸气压为p,
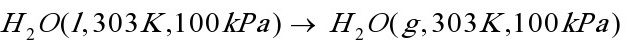
(4)理想气体从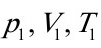 经不可逆过程到达
经不可逆过程到达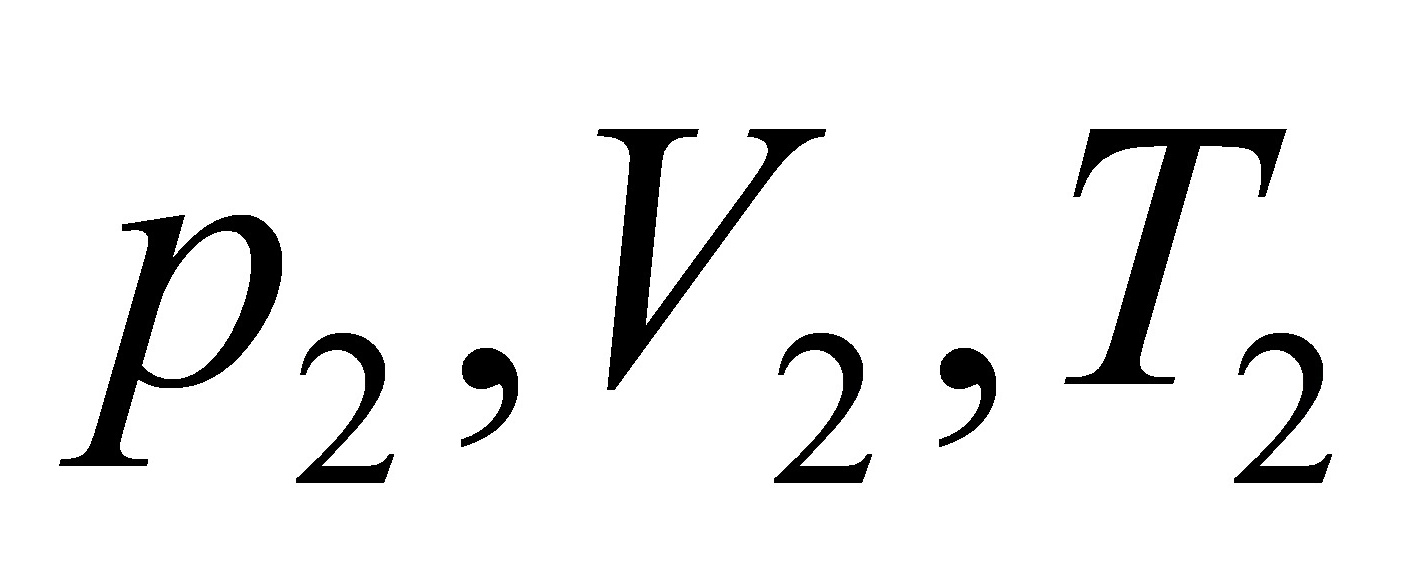 ,可设计几条可逆路线,画出示意图。
,可设计几条可逆路线,画出示意图。
[答](1)设计等温可逆膨胀
(2)在T1和T2之间设置无数个温差为dT的热源,使铁块T1和T1-dT,T1-2dT,…的无数热源接触,无限缓慢地达到终态温度T,使铁块T2和T2-dT,T2-2dT,…的热源接触,无限缓慢地达到终态温度T。
(3)可以设计两条可逆途径:一是等压可逆,另一条是等温可逆。
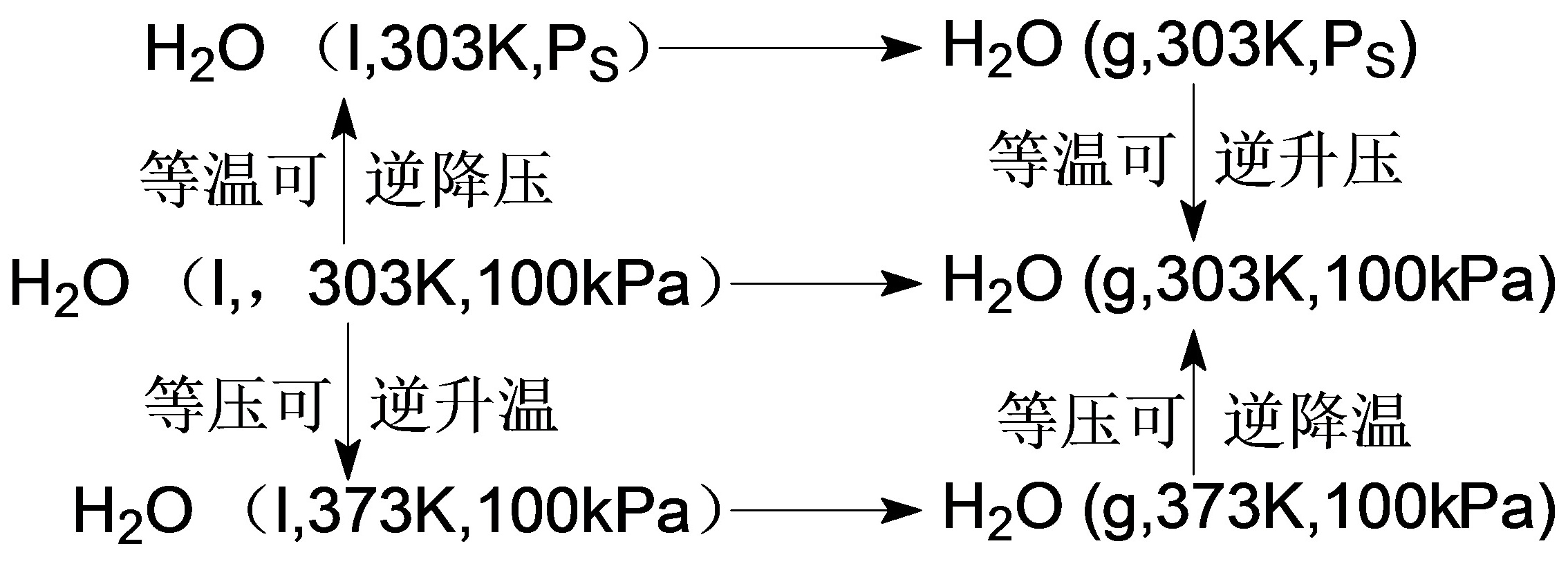
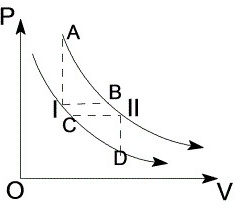 (4)可设计下列四条途径,从
(4)可设计下列四条途径,从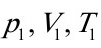 变化到
变化到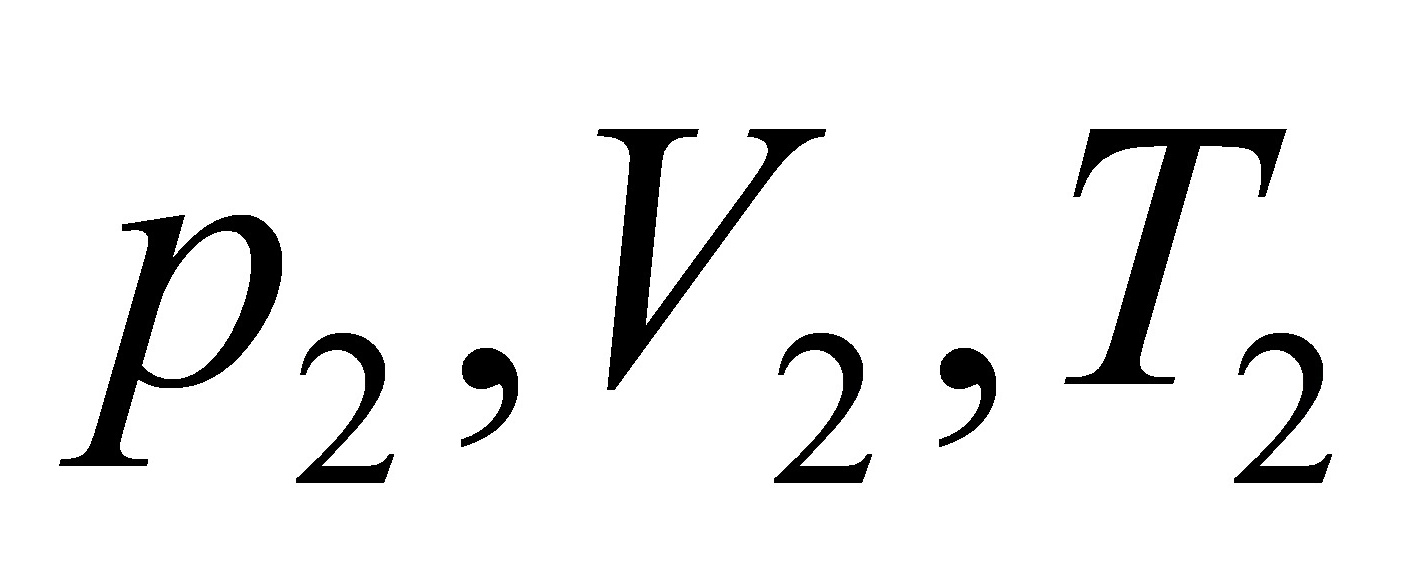 。
。
(a)等容可逆升压到状态A后再等温可逆膨胀终态Ⅱ;
(b)等压可逆膨胀到状态B后再等温可逆膨胀到终态Ⅱ;
(c) 等温可逆膨胀到状态C后再等压可逆膨胀到终态Ⅱ;
(d) 等温可逆膨胀到状态D后再等容可逆升压到终态Ⅱ。
[5]判断下列恒温、恒压过程中,熵值的变化,是大于零,小于零还是等于零,为什么?
(1)将食盐放入水中;
(2)HCl(g)溶于水中生成盐酸溶液;
(3)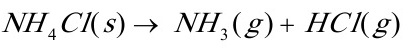 ;
;
(4)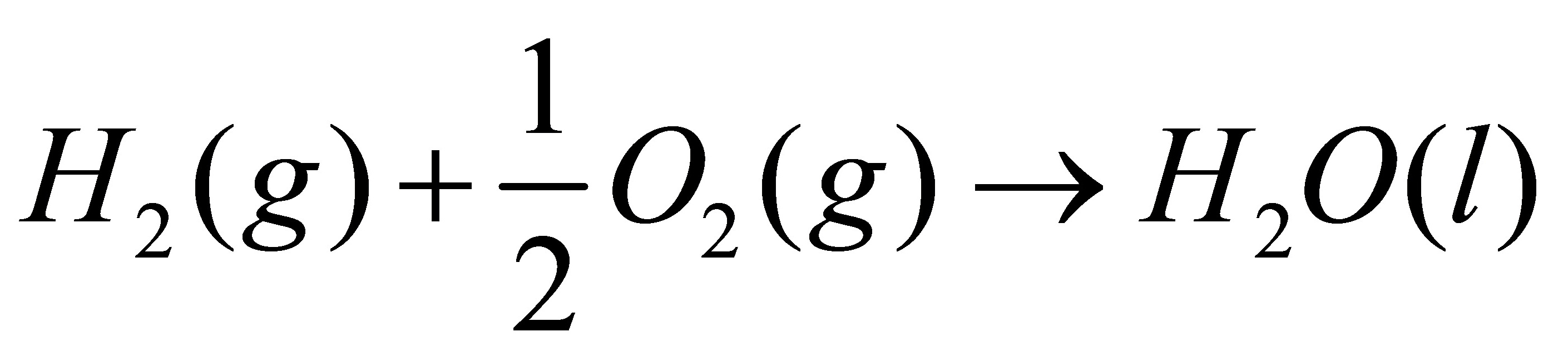 ;
;
(5)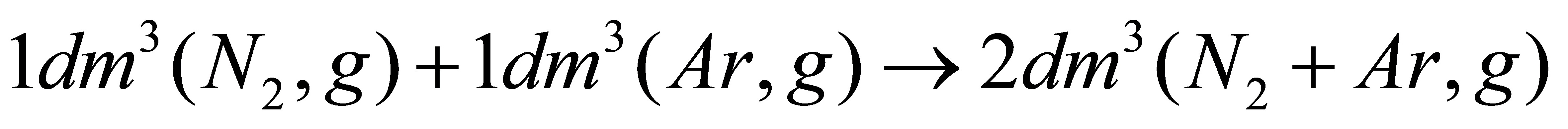 ;
;
(6)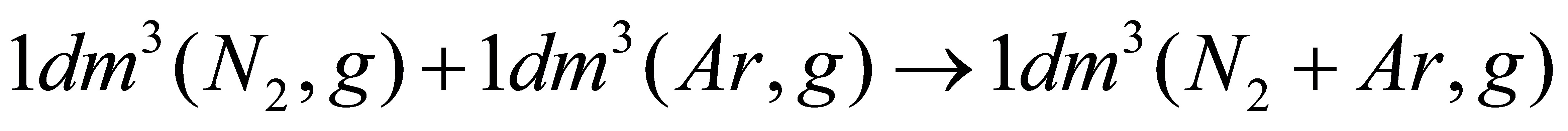 ;
;
(7)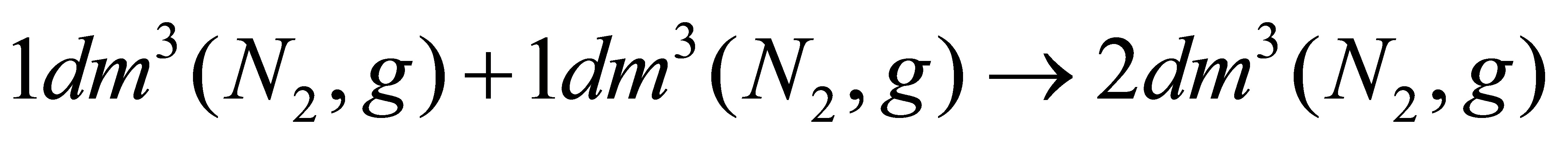 ;
;
(8)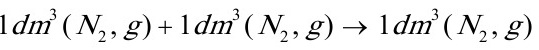 。
。
[解](1)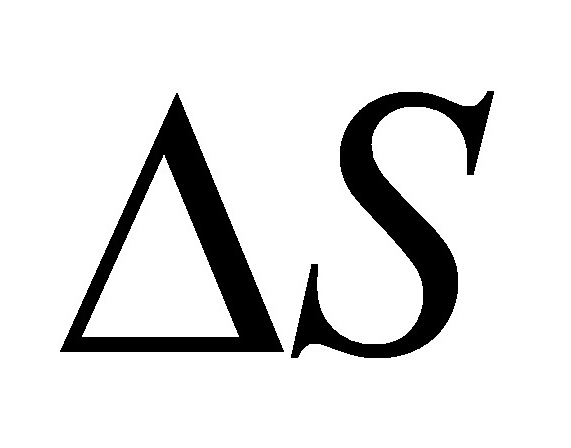 <0,因为将食盐放入水中为放热过程,Q<0,
<0,因为将食盐放入水中为放热过程,Q<0,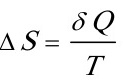 ,所以
,所以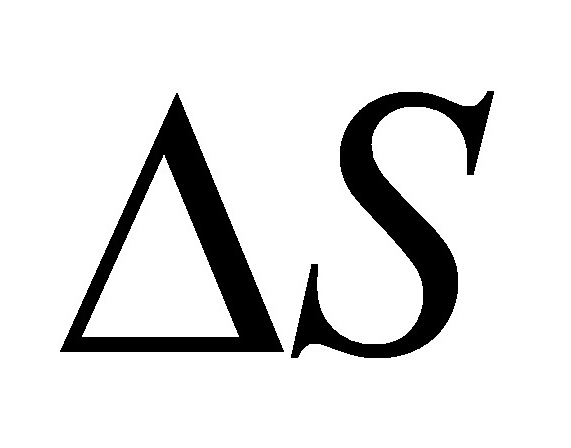 <0;
<0;
(2)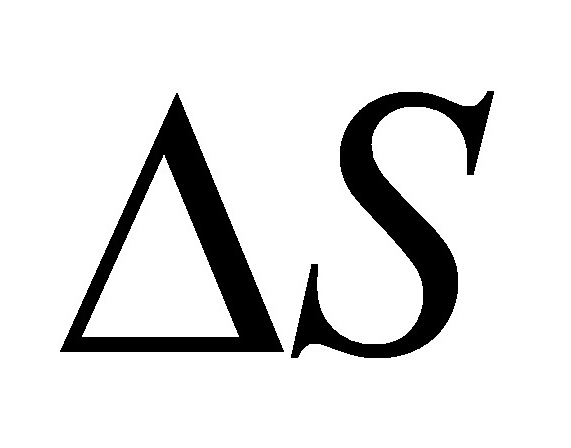 <0,同理,HCl(g)溶于水中Q<0,
<0,同理,HCl(g)溶于水中Q<0,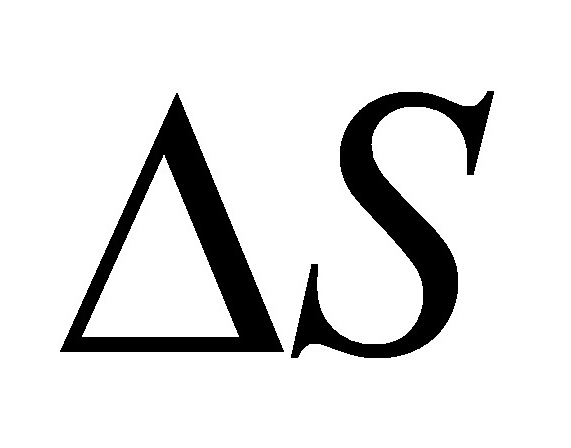 <0;
<0;
(3)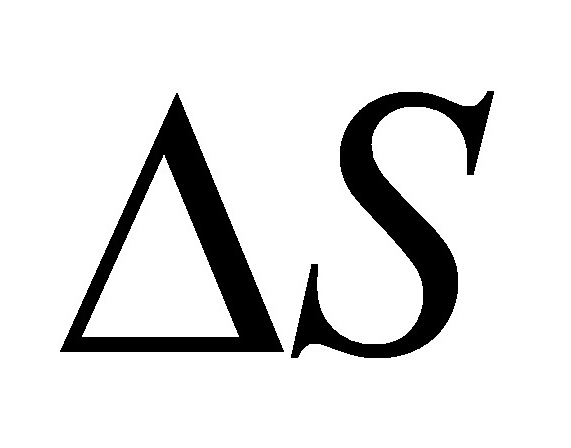 >0,因为该过程为吸热反应,Q>0,
>0,因为该过程为吸热反应,Q>0,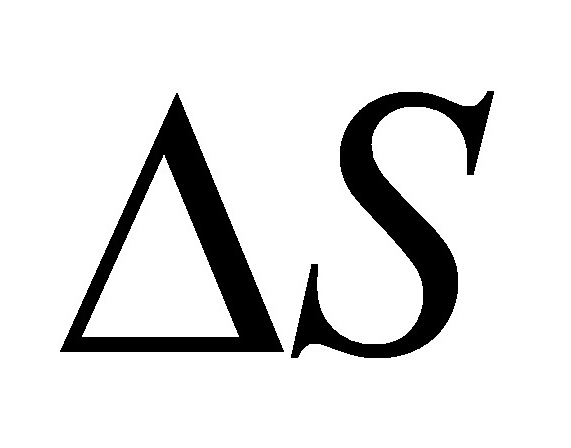 >0;或因为混乱度增加;
>0;或因为混乱度增加;
(4)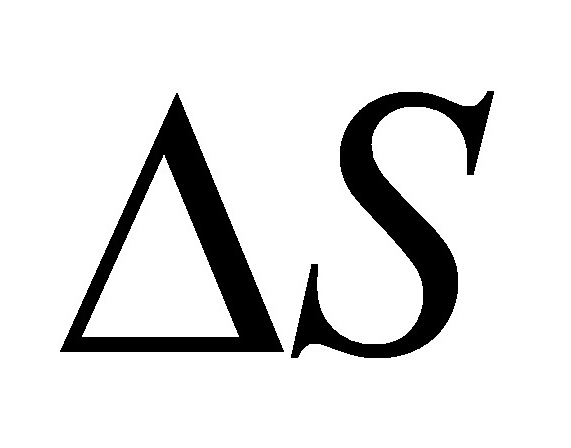 <0,因为该过程为放热反应,Q<0,
<0,因为该过程为放热反应,Q<0,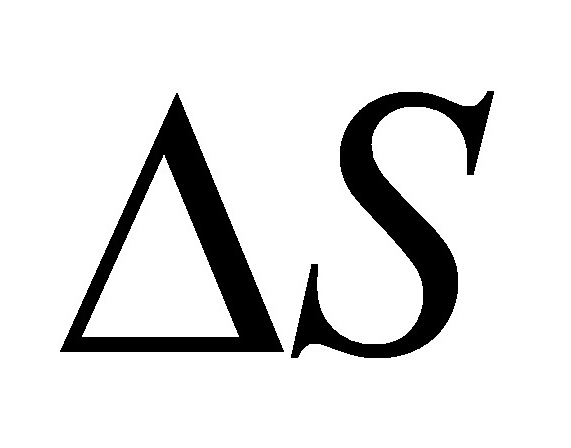 <0;或因为混乱度减小;
<0;或因为混乱度减小;
(5)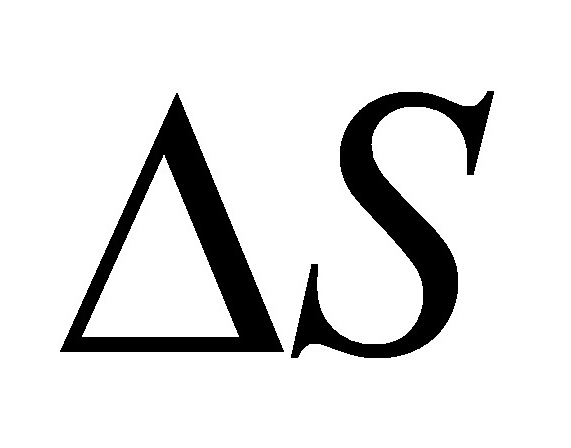 >0,根据
>0,根据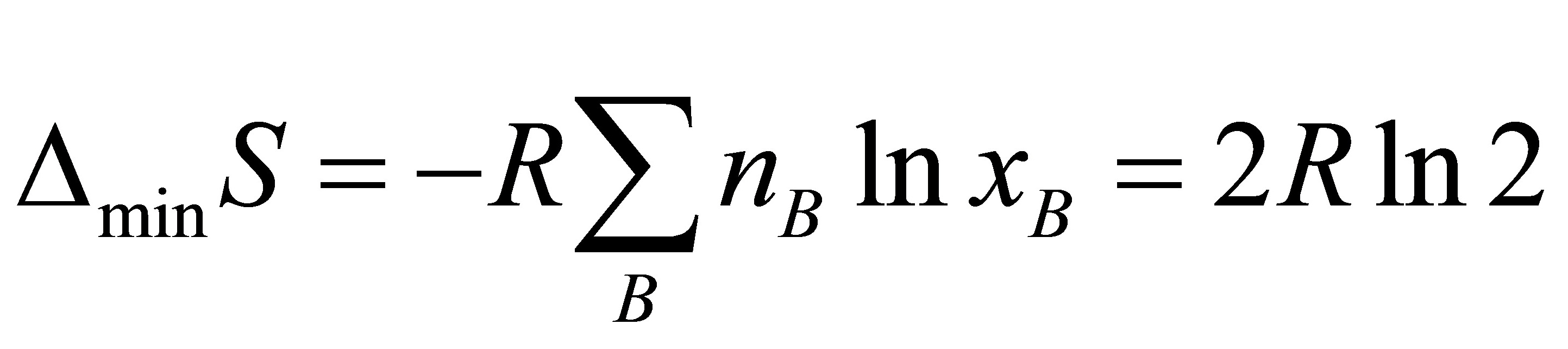 >0,或因为混乱度增加;
>0,或因为混乱度增加;
(6)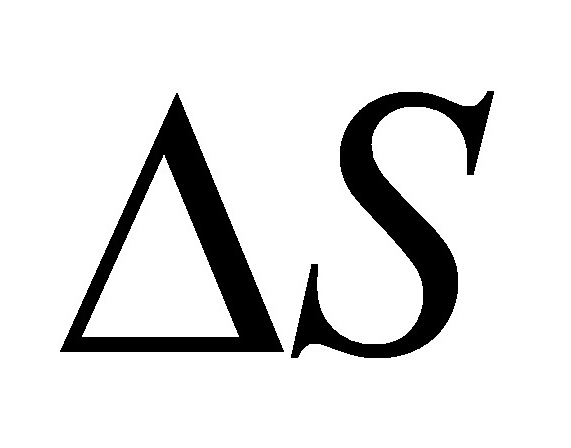 =0,根据
=0,根据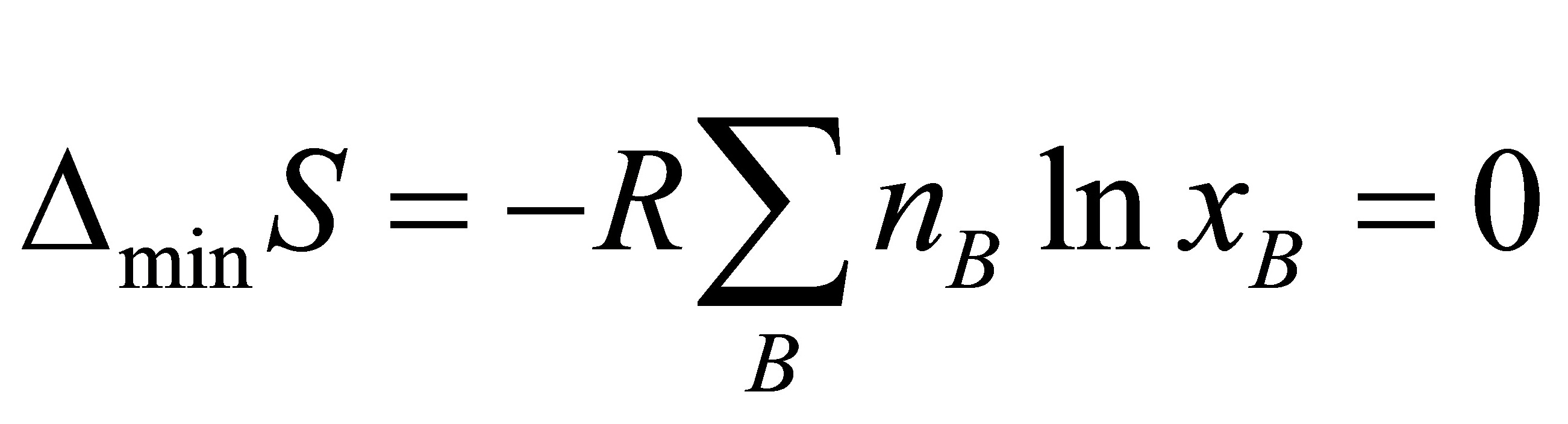 ;
;
(7)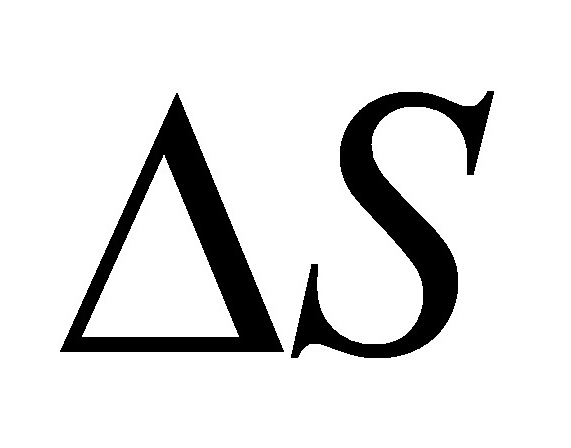 =0,根据
=0,根据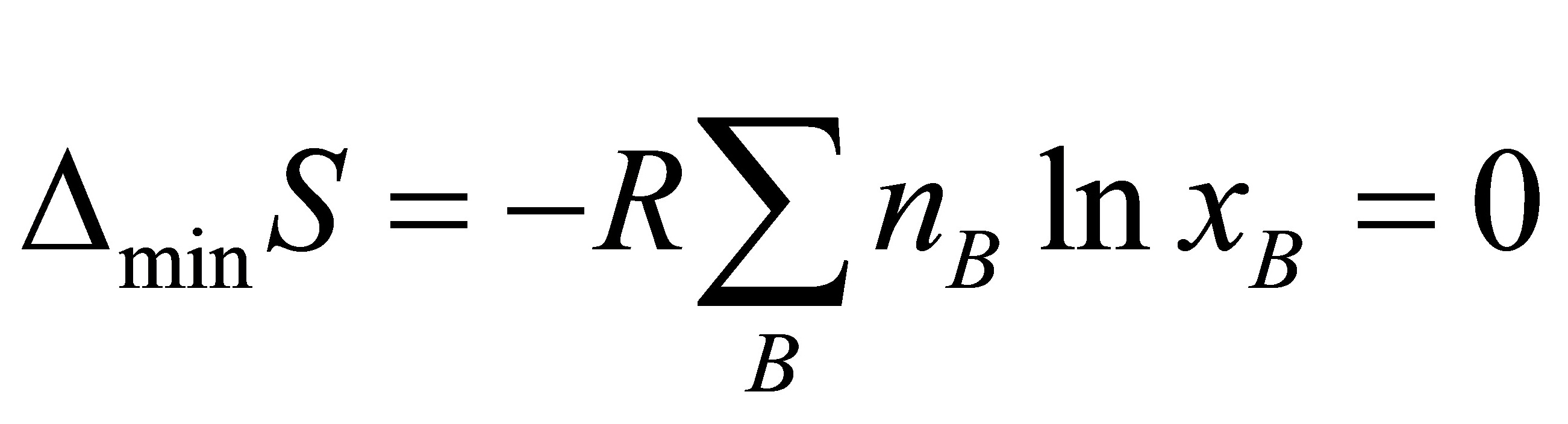 ;
;
(8)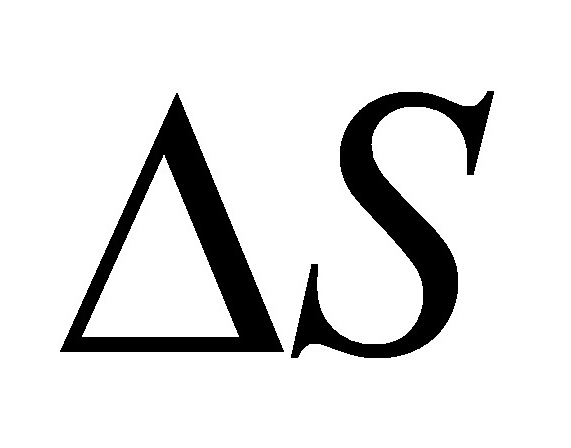 <0,根据
<0,根据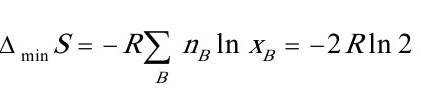 <0
<0
[6](1)在298K和100kPa时,反应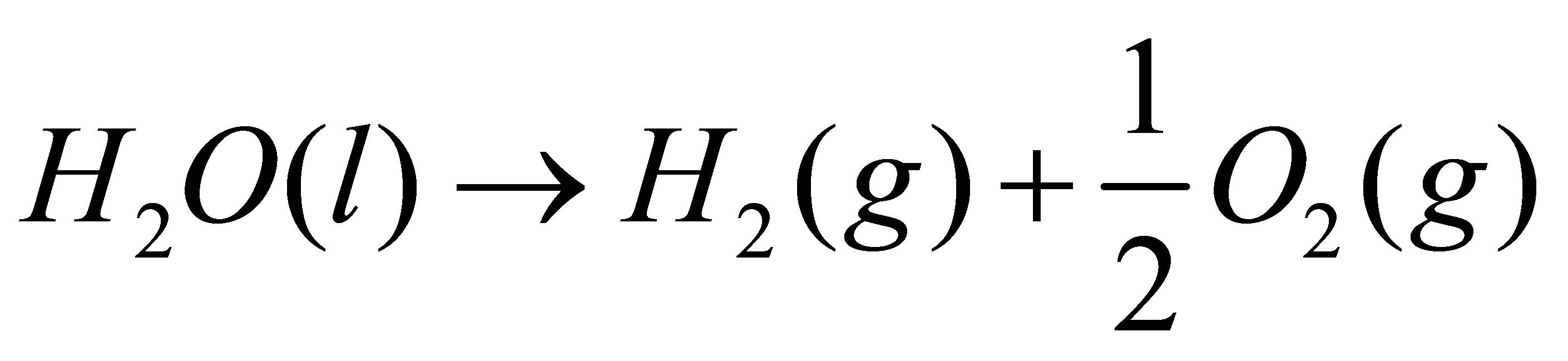 的
的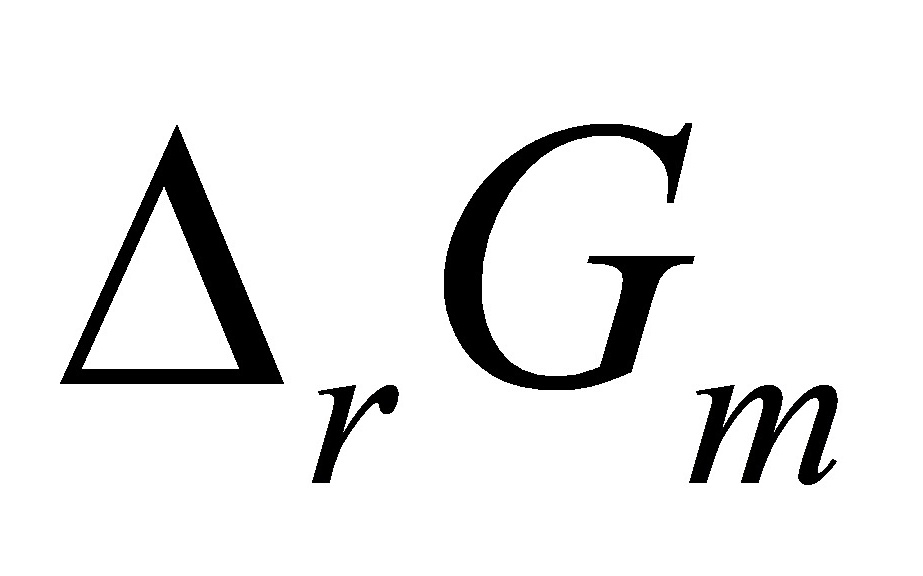 >0,说明该反应不能自发进行。但在实验室常用电解水的方法制备氢气,这两者有无矛盾?
>0,说明该反应不能自发进行。但在实验室常用电解水的方法制备氢气,这两者有无矛盾?
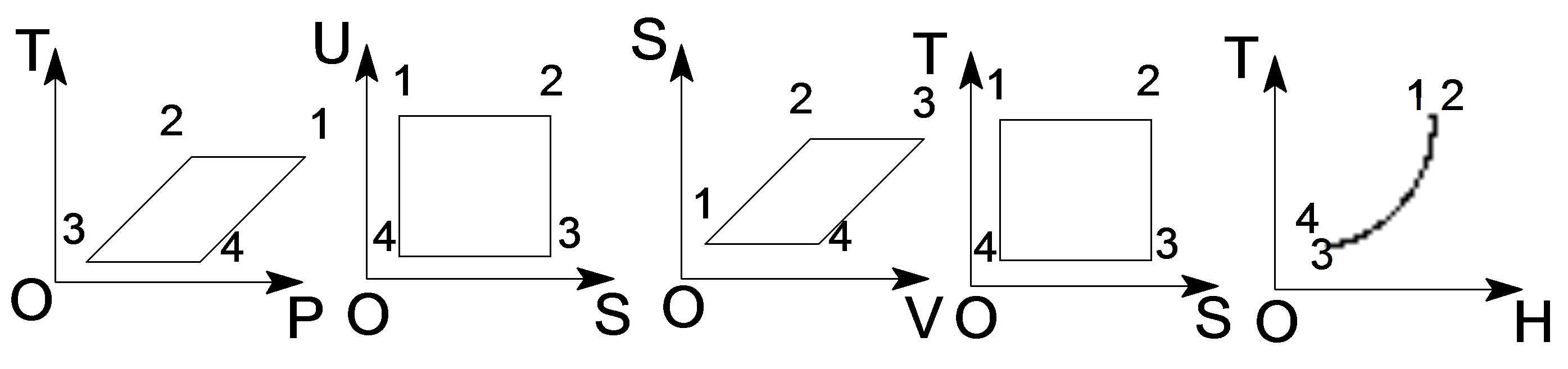
(2)请将Carnot循环分别表达在以如下坐标表示的图上:
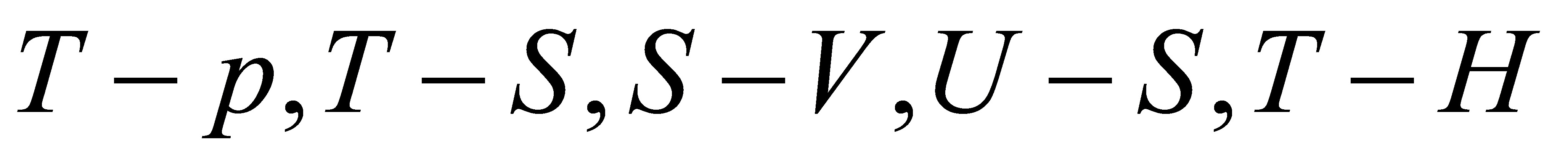
[解] (1)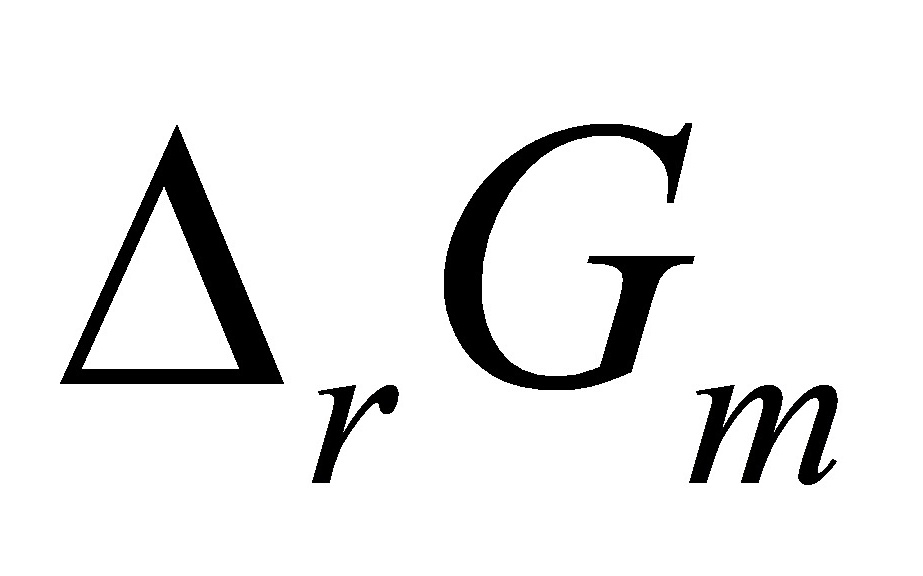 >0的判据是在等温等压非体积功为0的条件下,所以在298K和100kPa时,反应
>0的判据是在等温等压非体积功为0的条件下,所以在298K和100kPa时,反应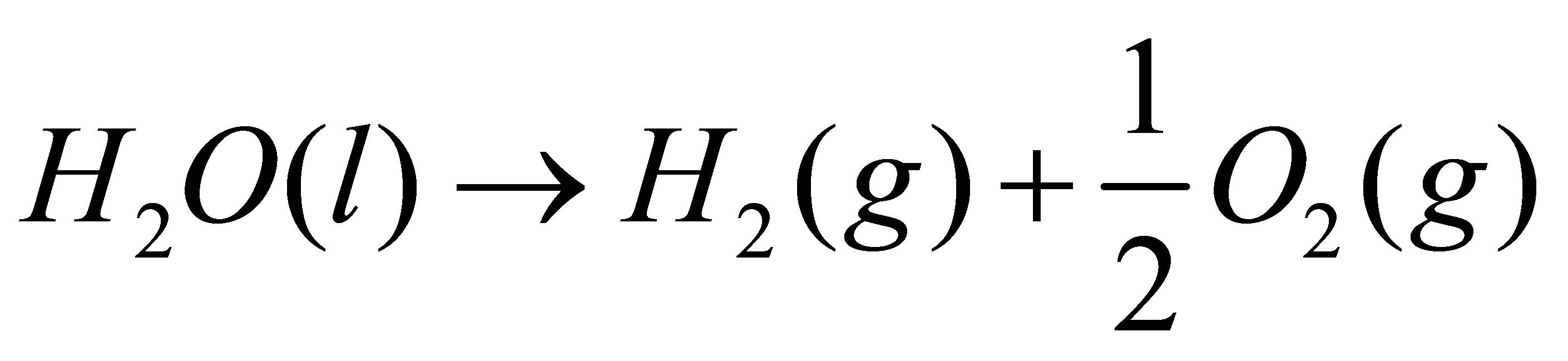 的
的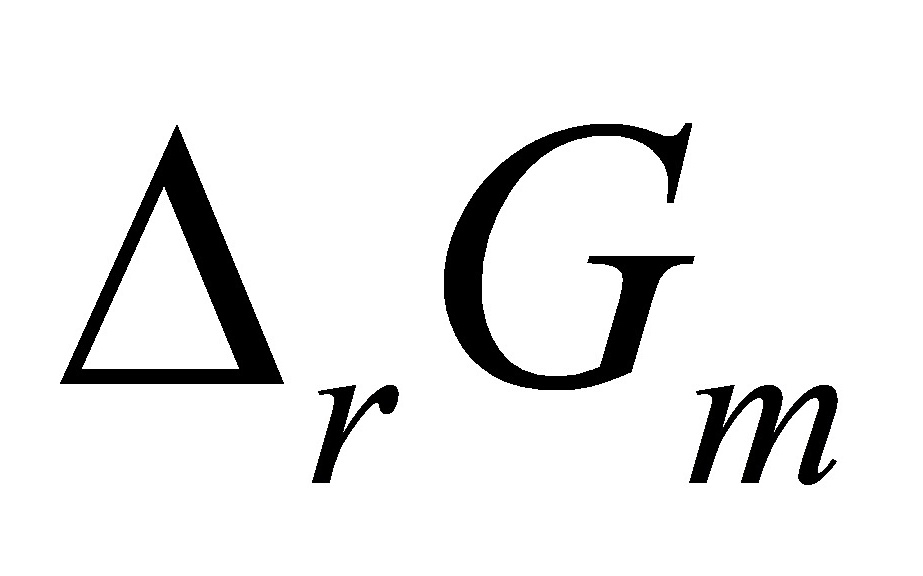 >0,说明该反应在等温等压非体积功为0的条件下不能自发进行。而在实验室常用电解水的方法制备氢气,是在电功对体系作功,所以并不矛盾。
>0,说明该反应在等温等压非体积功为0的条件下不能自发进行。而在实验室常用电解水的方法制备氢气,是在电功对体系作功,所以并不矛盾。
(2)
[习题]
[01]有5mol某双原子理想气体,已知其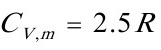 ,从始态400K,200kPa,经绝热可逆压缩至400kPa后,再真空膨胀至200kPa,求整个过程的Q,W,△U,△H和△S.
,从始态400K,200kPa,经绝热可逆压缩至400kPa后,再真空膨胀至200kPa,求整个过程的Q,W,△U,△H和△S.
[解]第一步绝热可逆压缩 Q1=0 △S1=0
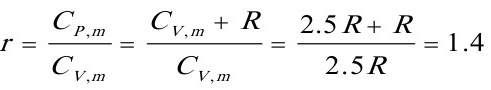
根据绝热过程方程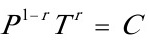 得
得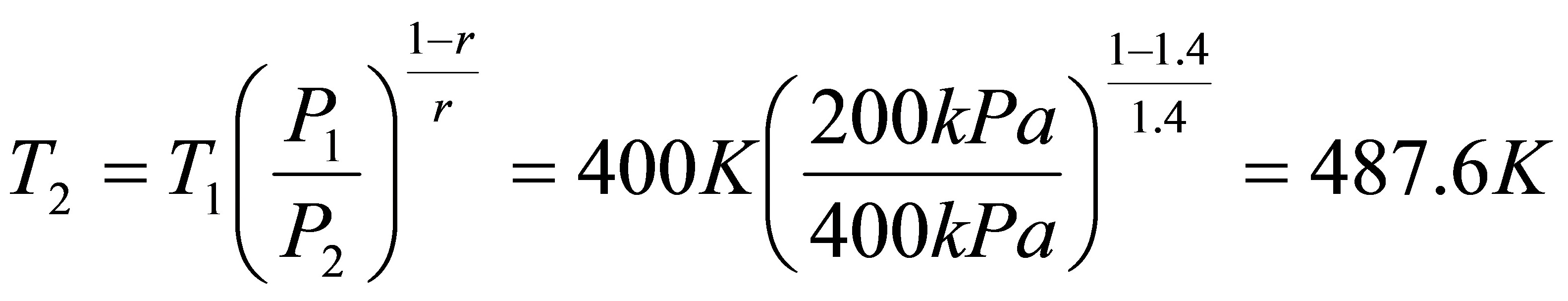
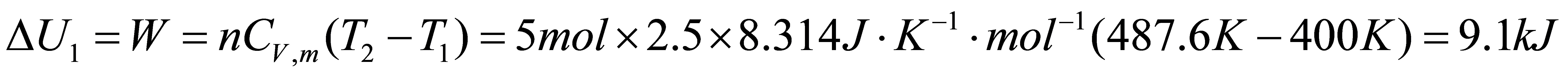
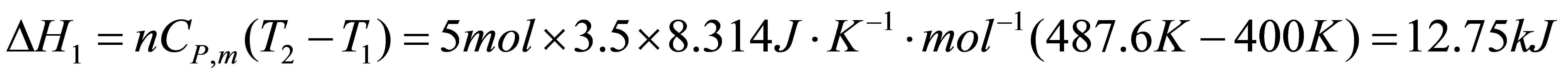
第二步等温向真空膨胀 W2=0 △U2=△H2=0 Q2=0
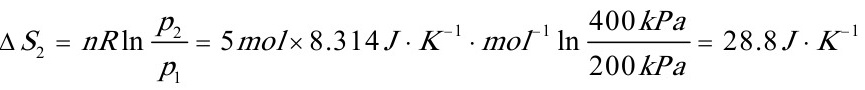
所以整个过程的
Q=0,W=9.1kJ,△U=9.1kJ,△H=12.75kJ,△S=28.8J•K-1
[2]有5molHe(g)可看作理想气体, 已知其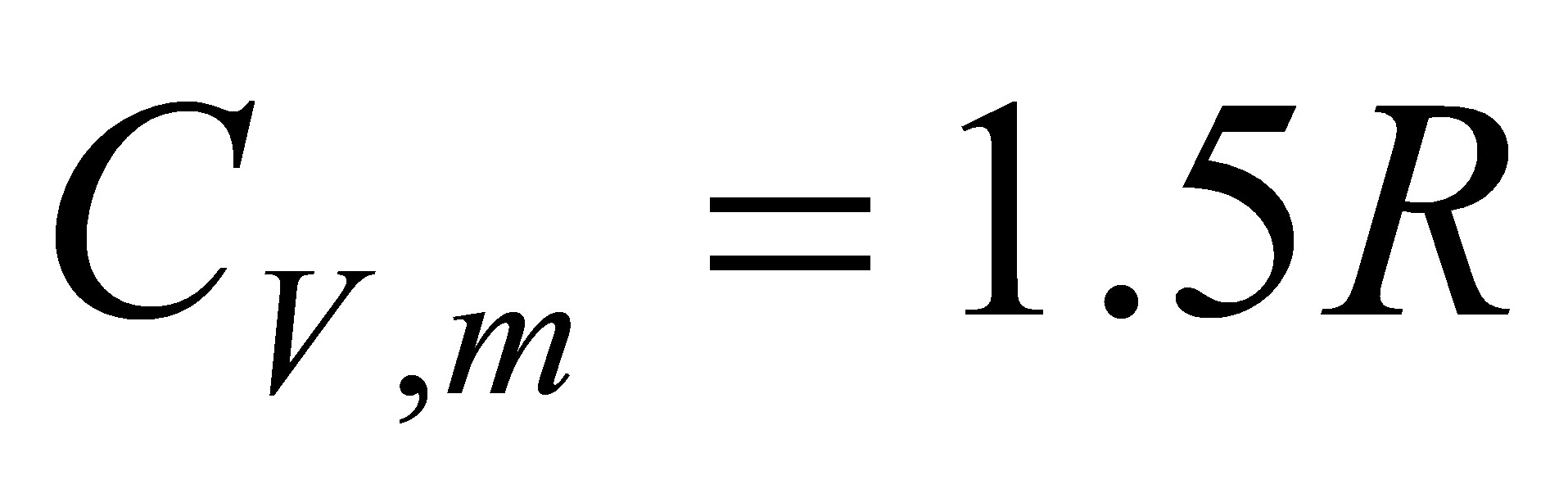 ,从始态273K,100kPa,变到终态298K,1000kPa,计算该过程的熵变.
,从始态273K,100kPa,变到终态298K,1000kPa,计算该过程的熵变.
[解]根据理想气体从状态p1,V1,T1到终态p2,V2,T2的熵变公式:
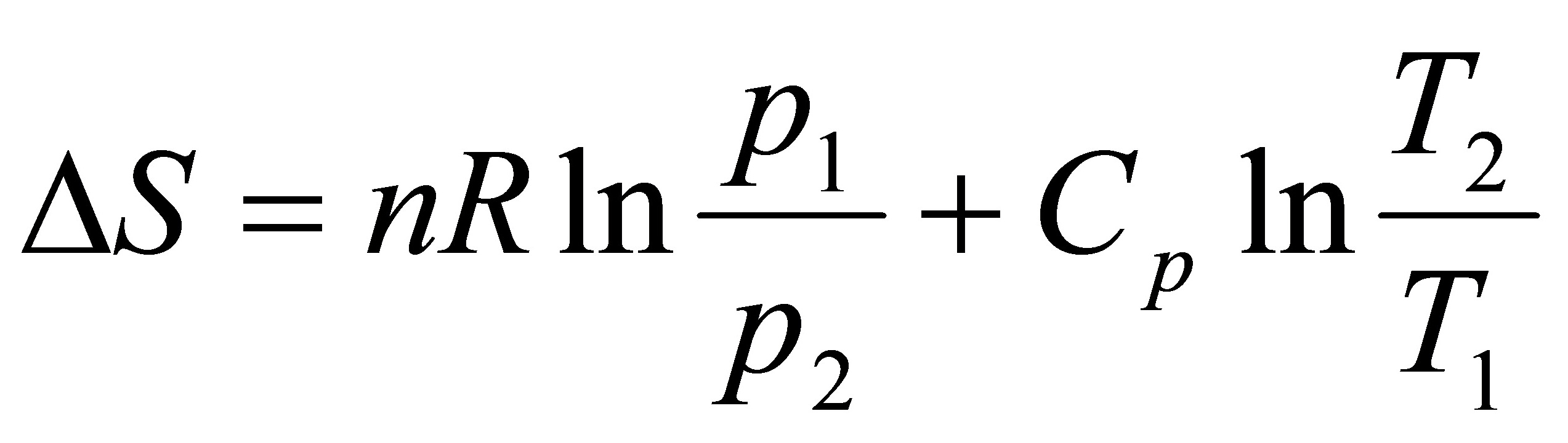 得:
得: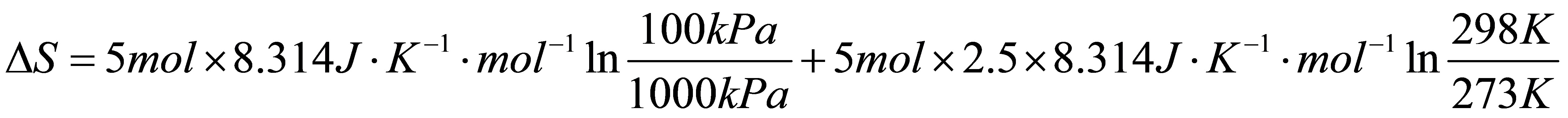
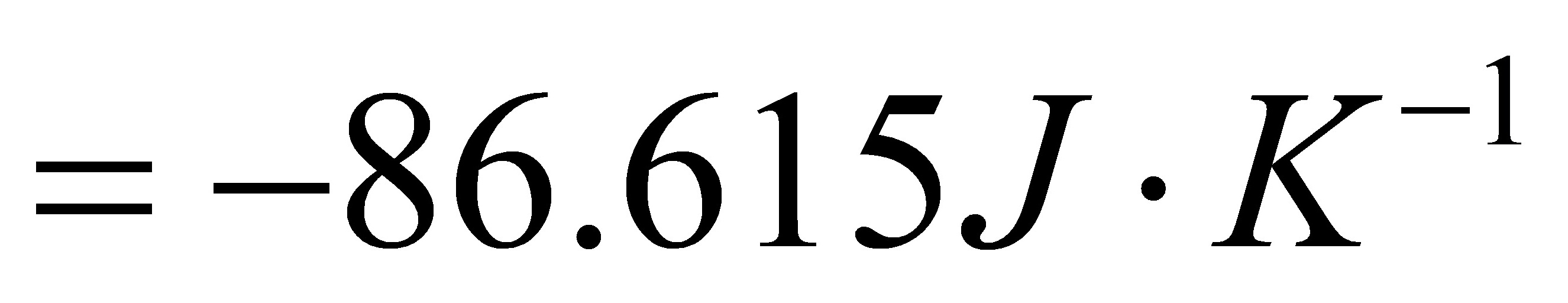
[03]在绝热容器中,将0.10kg、283K的水与0.20kg、313K的水混合,求混合过程的熵变。设水的平均比热为4.184kJ•K-1•kg-1.
[解]设混合后的平衡温度为T,则
0.10kg、283K的水吸热为
Q1=CP(T-T1)=4.184kJ•K-1•kg-1×0.10kg×(T-283K)
0.20kg、313K的水放热为
Q2=CP(T1-T)=4.184kJ•K-1•kg-1×0.20kg×(313K-T)
平衡时Q1=Q2得 T=303K
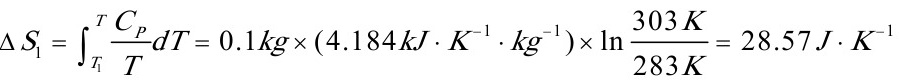
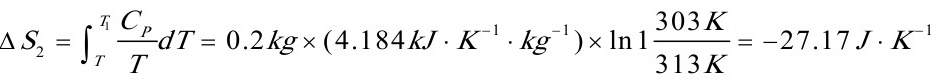 △S=△S1+△S2=1.40J•K-1
△S=△S1+△S2=1.40J•K-1
[04]在298K的等温情况下,在一个中间有导热隔板分开的盒子中,一边放0.2molO2(g),压力为20kPa,另一边放0.8molN2(g),压力为80kPa,抽去隔板使两种气体混合,试求
(1)混合后盒子中的压力;
(2)混合过程的Q,W,△U,△S和△G;
(3)如果假设在等温情况下,使混合后的气体再可逆地回到始态,计算该过程的Q和W的值。
[解](1)混合前O2(g)和N2(g)的体积V相等,混合后是1mol气体占全部容积的体积2V。
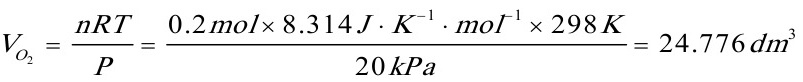
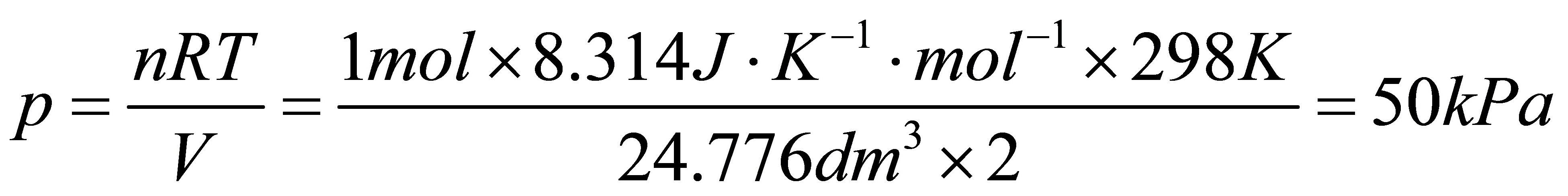
(2)由于是等温过程 △U=0
O2(g)和N2(g)都相当于在等温下从V膨胀到2V
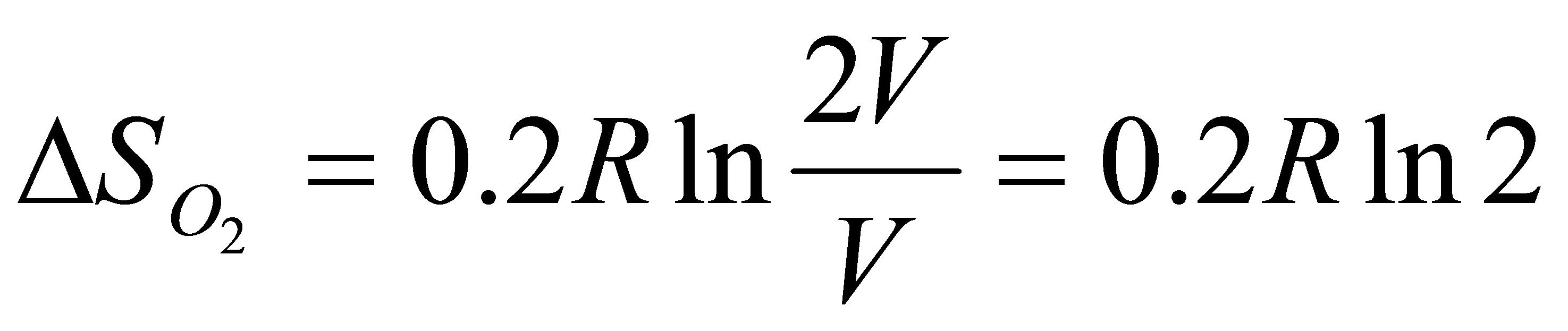
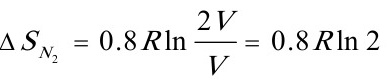
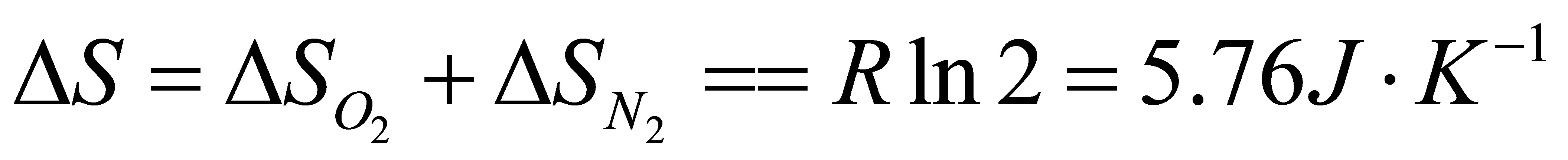
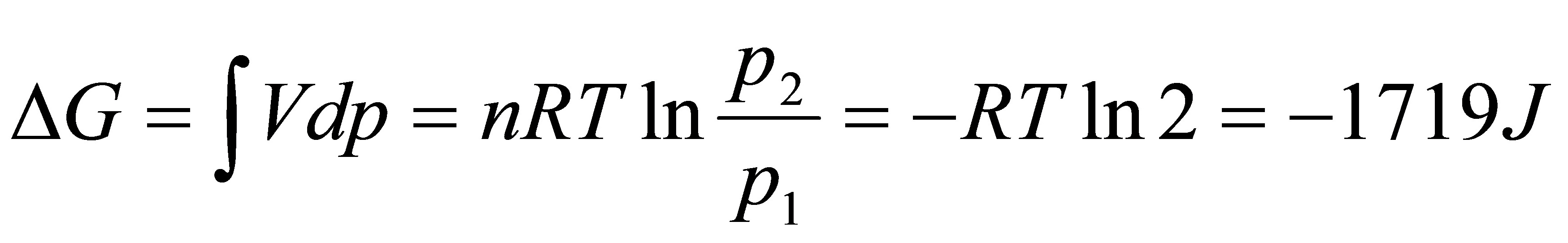
(3)因为△U′=0,Qr=-Wr=T△S′
所以 Qr=-Wr=T△S′=298K×(-5.76J•K-1)=-1.716J
[05]有一绝热箱子,中间用绝热隔板把箱子的容积一分为二,一边放1mol 300K,100kPa的单原子理想气体Ar(g),另一边放2mol 400K,200kPa的双原子理想气体N2(g),如果把绝热隔板抽去,让两种气体混合达平衡,求混合过程的熵变。
[解]起初Ar(g)和N2(g)的体积分别为
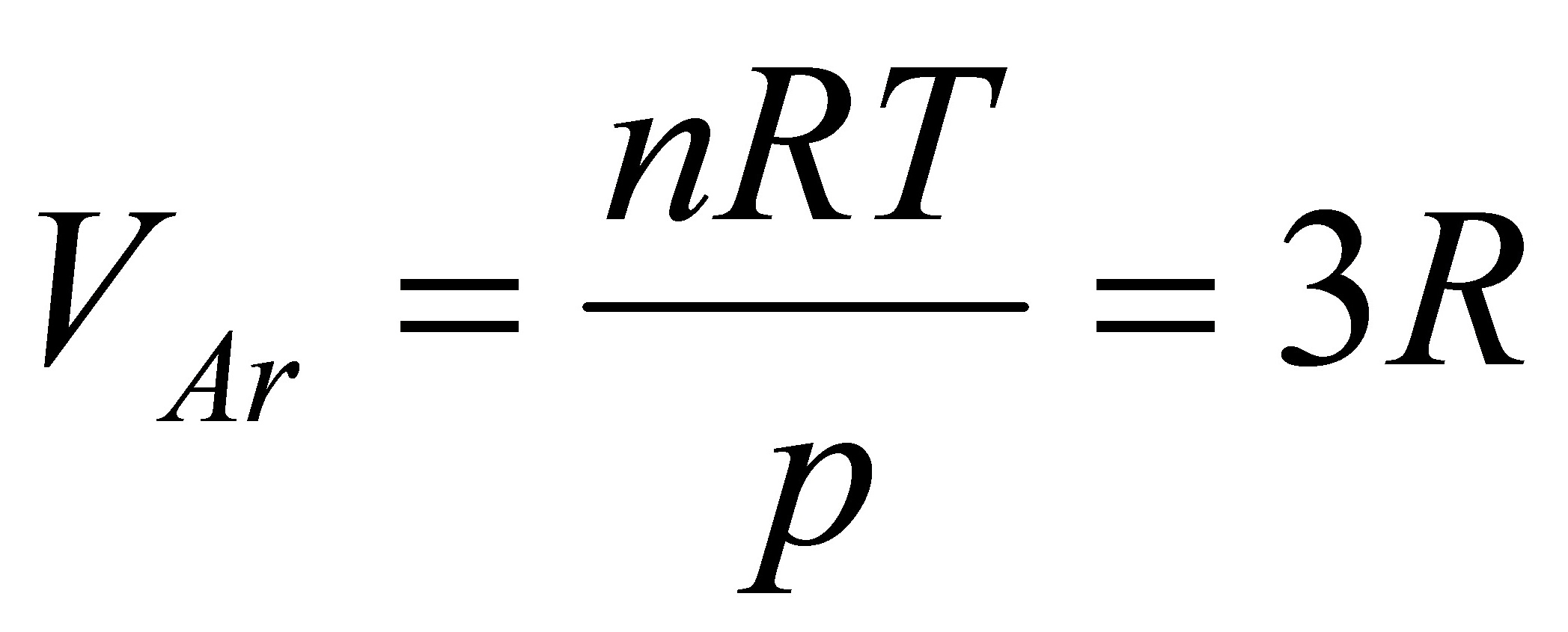 ,
, 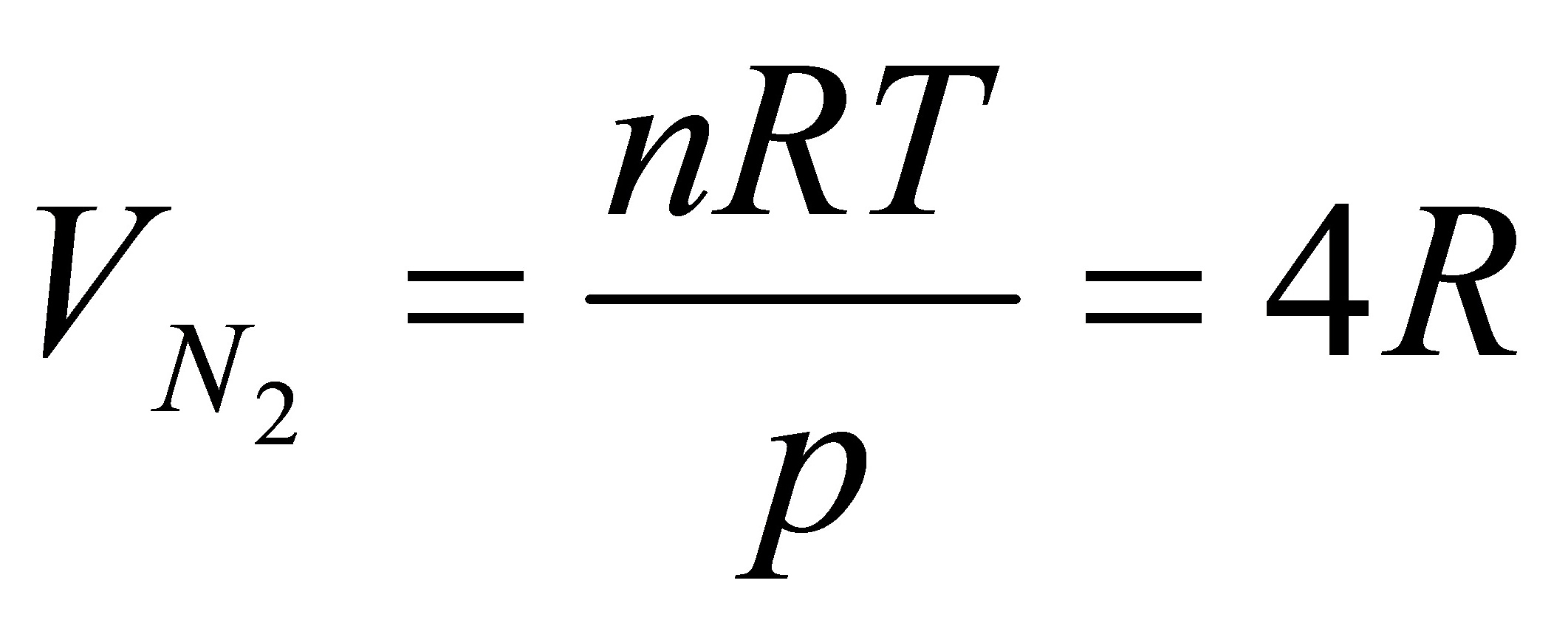
当混合时对于1molAr(g)相当于从300K,100kPa膨胀到T,P,V=7R
对于2molN2(g)相当于从400K,200kPa膨胀到T,P,V=7R
而整个体系的 W=0 QV=△U=0
所以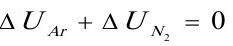
即 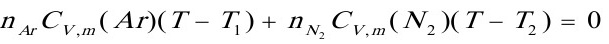
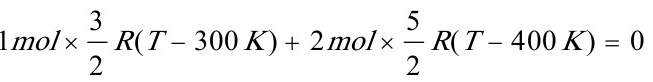
得 T=362.5K
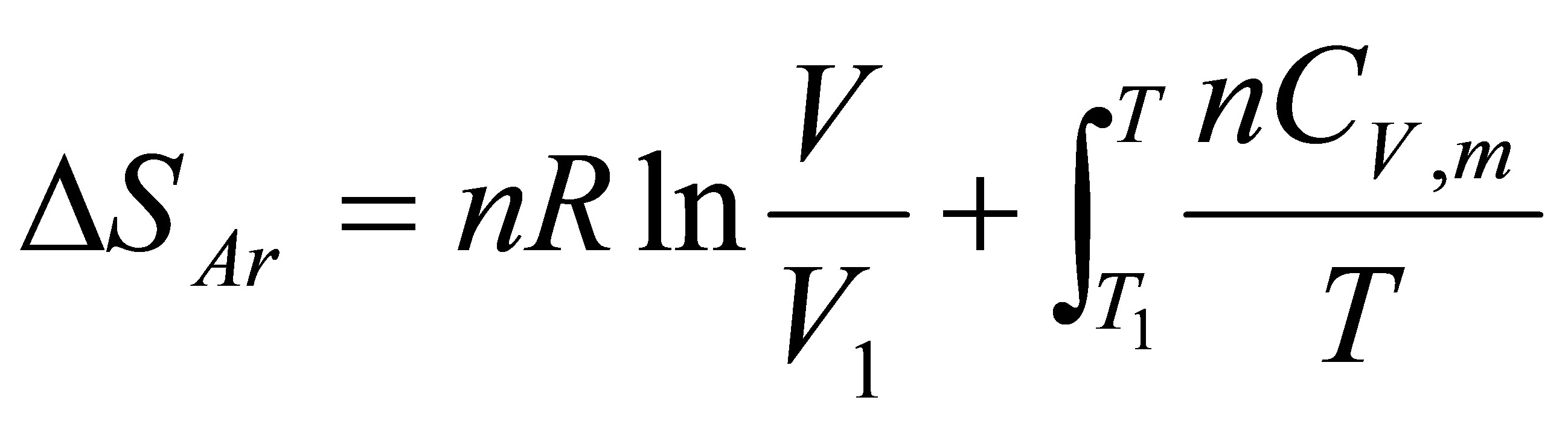
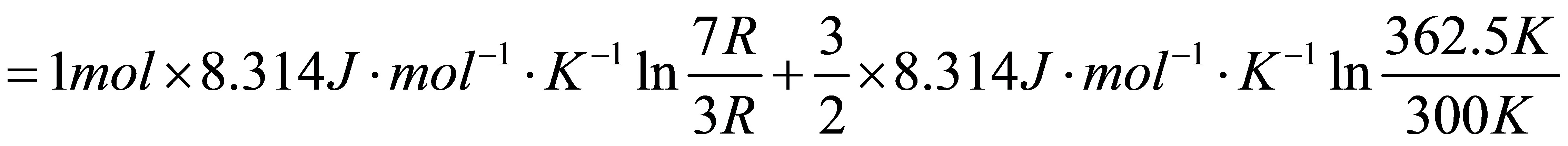
=9.4J
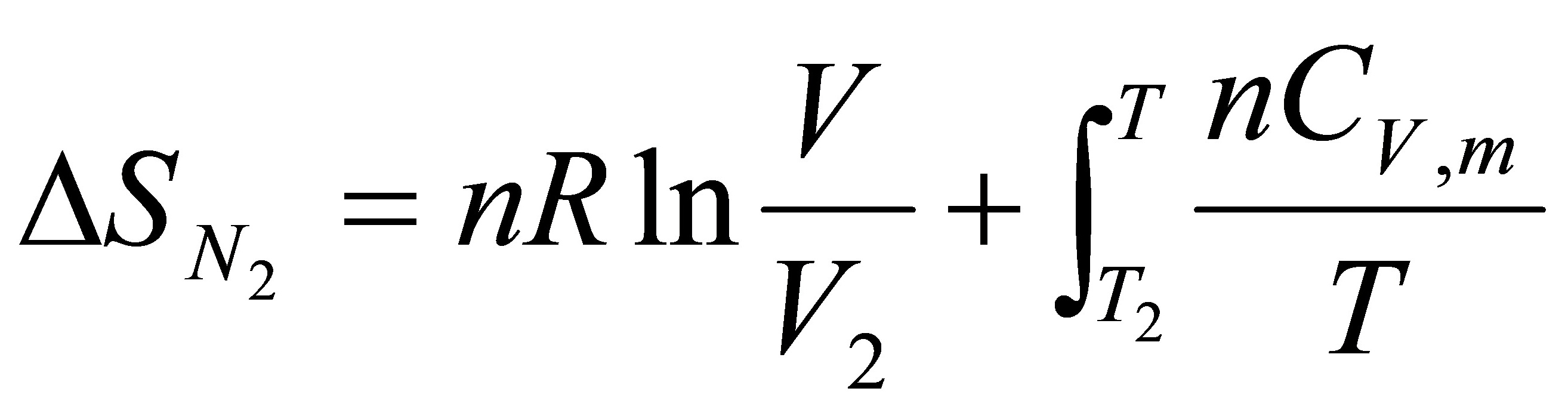
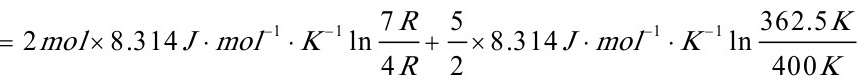
=7.26J
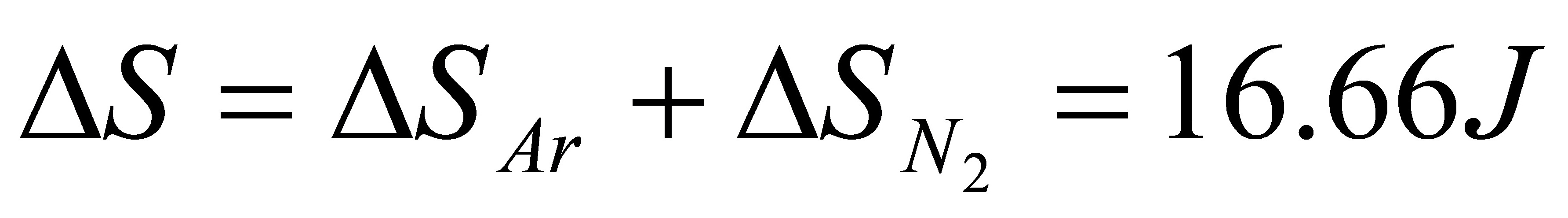
[06]有2mol理想气体,从始态300K,20dm3,经下列不同过程等温膨胀至50dm3,计算各过程的Q,W,△U,△H和△S。
(1)可逆膨胀;
(2)真空膨胀;
(3)对抗恒外压100kPa膨胀。
[解]由于是理想气体的等温过程,所以△U=△H=0
(1)可逆膨胀
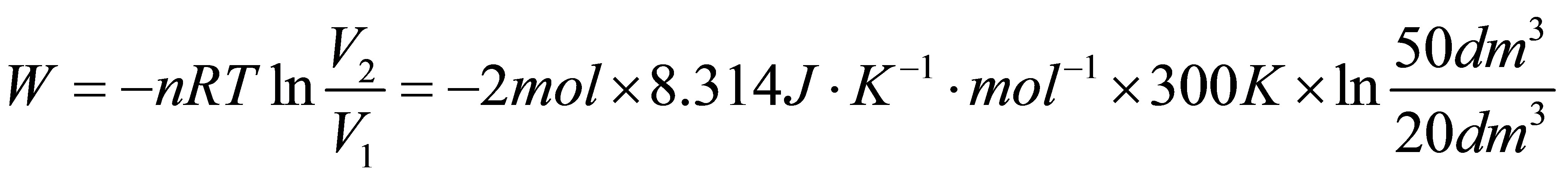
=-4570.8J
Q=-W=4570.8J
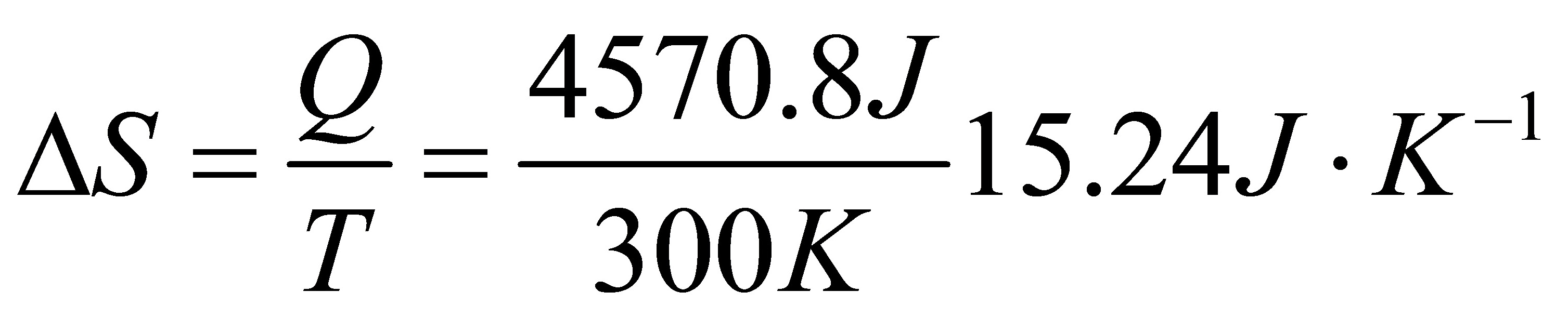
(2)真空膨胀;
W=Q=0
S是状态函数所以△S的值同(1)
(3)对抗恒外压100kPa膨胀。
W=-P(V2-V1)=-100kPa(50dm3-20dm3)=-3.0kJ
Q=-W=3.0kJ
S是状态函数所以△S的值同(1)
[07]有1mol甲苯CH3C6H5(l)在其沸点383K时蒸发为气,计算该过程的Q,W,△U,△H,△S,△A和△G.已知在该温度下甲苯的汽化热为362kJ•kg-1.
[解]在沸点时蒸发为可逆相变,所以 △G=0
△H=Q=362kJ•kg-1×1mol×0.092kg•mol-1=33.304kJ
W=-p(Vg-Vl)= -p Vg=-nRT
=-1mol×8.341J•K-1•mol-1×383K=-3184.26J=-3.184kJ
△U=△H-△PV=△H-P△V=△H+W=33.304kJ-3.184kJ=30.12kJ
△S=Q/T=33.304kJ/383K=86.96J•K-1
△A=△U-T△S=△U-Q=W=-3.184kJ
[08]在一个绝热容器中,装有298K的H2O(l)1.0kg,现投入0.15kg冰H2O(s),计算该过程的熵变.已知H2O(s)的熔化焓为333.4J•g-1. H2O(l)的平均比热容为4.184J•K-1•g-1.
[解]设计过程如下:
 1.0kg H2O(l)放出的热为: Q放=1.0×103×4.184×(298-T)
1.0kg H2O(l)放出的热为: Q放=1.0×103×4.184×(298-T)
0.15kgH2O(s)吸收的热为:
Q吸=0.15×103×4.184×(T-273)+0.15×103×333.4
根据Q放=Q吸 得 T=284.35K
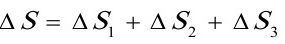
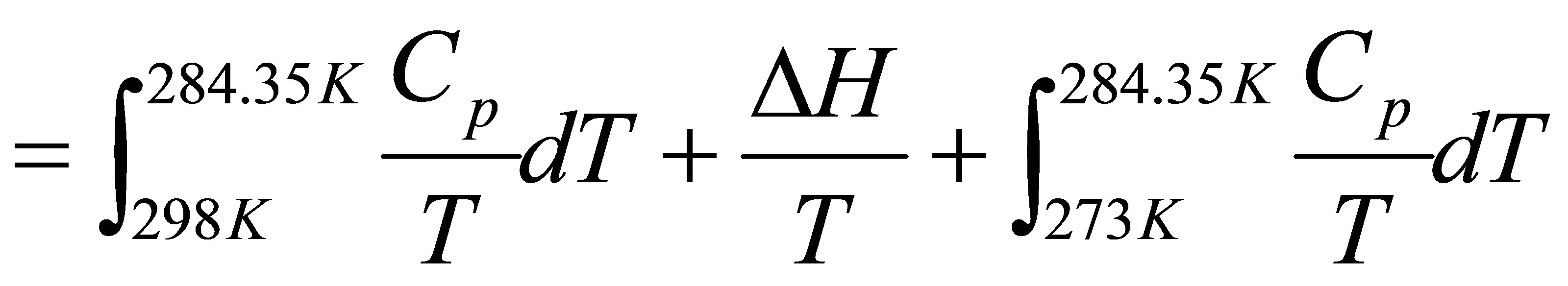
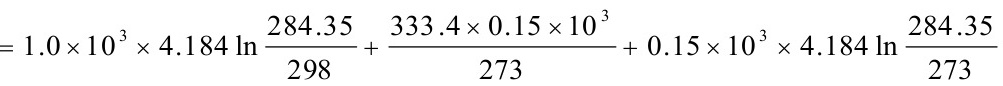
=12.57J•K-1
[09]实验室中有一个大恒温槽的温度为400K,室温为300K,因恒温槽绝热不良而有4.0kJ的热传给了室的空气,用计算说明这一过程是否可逆.
[解]该过程是体系放热Q,环境吸热-Q的过程
△S体系=Q/T体系=-4.0kJ/400K=-10J•K-1
△S环境=-Q/T环境=4.0kJ/300K=13.33J•K-1
△S隔离=△S体系+△S环境=-10J•K-1+13.33J•K-1=3.33J•K-1>0
所以该过程为不可逆过程.
[10]有1mol过冷水,从始态263K,101kPa变成同温、同压的冰,求该过程的熵变。并用计算说明这一过程的可逆性.已知水和冰在该温度围的平均摩尔定压热容分别为: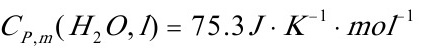 ,
,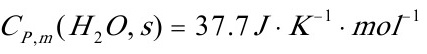 ;在273K, 101kPa时水的摩尔凝固热为600
;在273K, 101kPa时水的摩尔凝固热为600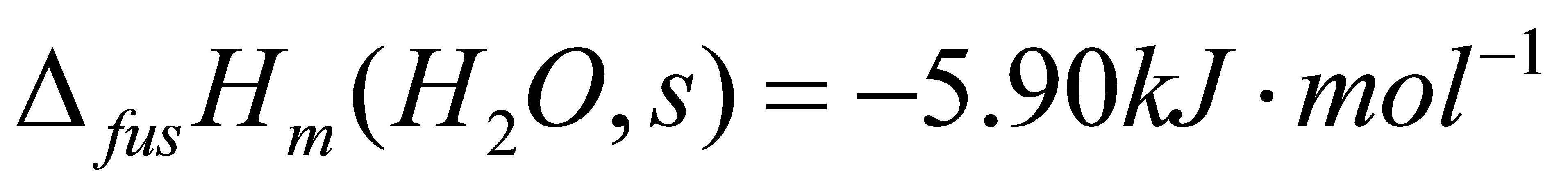 。
。
[解]设计如下过程
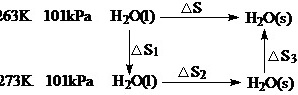
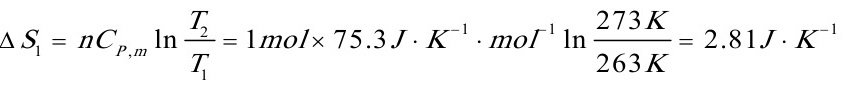
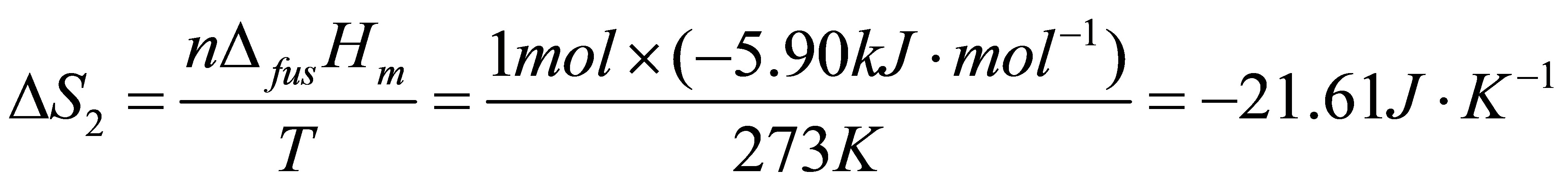
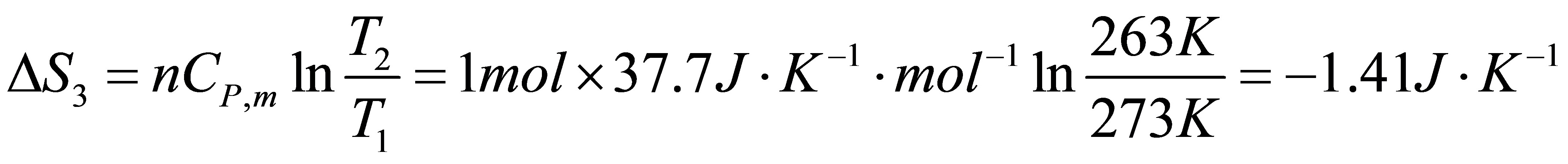
△S=△S1+△S2+△S3=-20.21J•K-1
[11]1molN2(g)可作理想气体,从始态298K,100kPa,经如下两个等温过程,分别到达终态压力为600kPa,分别求过程的Q,W,△U,△H,△A,△G,△S,和△Siso.
(1)等温可逆压缩;
(2)等外压为600kPa时压缩。
[解]由于都是理想气体的等温过程,所以△U=△H=0
(1)等温可逆压缩
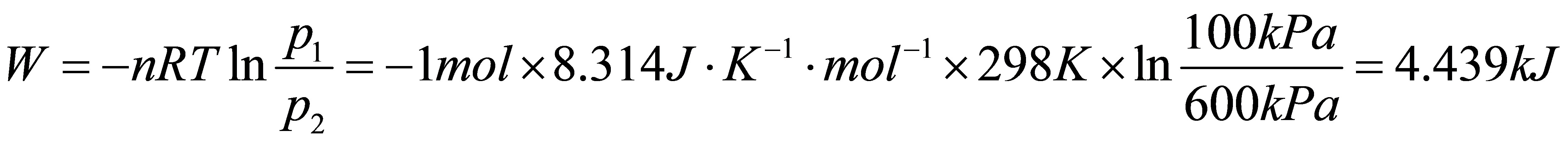
Q=-W=-4.439kJ
△S=Q/T=-4439J/298K=-14.90J•K-1
△A=△U-T△S=-Q=W=4.439kJ
△G=△H-T△S=-Q=W=4.439kJ
△S环境=-Q/T=14.90J•K-1
△Siso=△S体系+△S环境=0
(2)等外压为600kPa时压缩
W=-P2(V2-V1)=-nRT(1-P2/P1)
=-1mol×8.314J•K-1•mol-1×298K×(1-600kPa/100kPa)
=12.39kJ
Q=-W=-12.39kJ
△A,△G,△S都是状态函数的变化,所以值与(1)相同
△S环境=-Q/T=12.39kJ/298K=41.58J•K
△Siso=△S体系+△S环境=-14.90J•K-1+41.58J•K=26.28J•K
[12]将1molO2(g)从298K,100kPa的始态,绝热可逆压缩到600kPa,试求该过程Q,W,△U,△H,△A,△G,△S,和△Siso.设O2(g)为理想气体,已知O2(g)的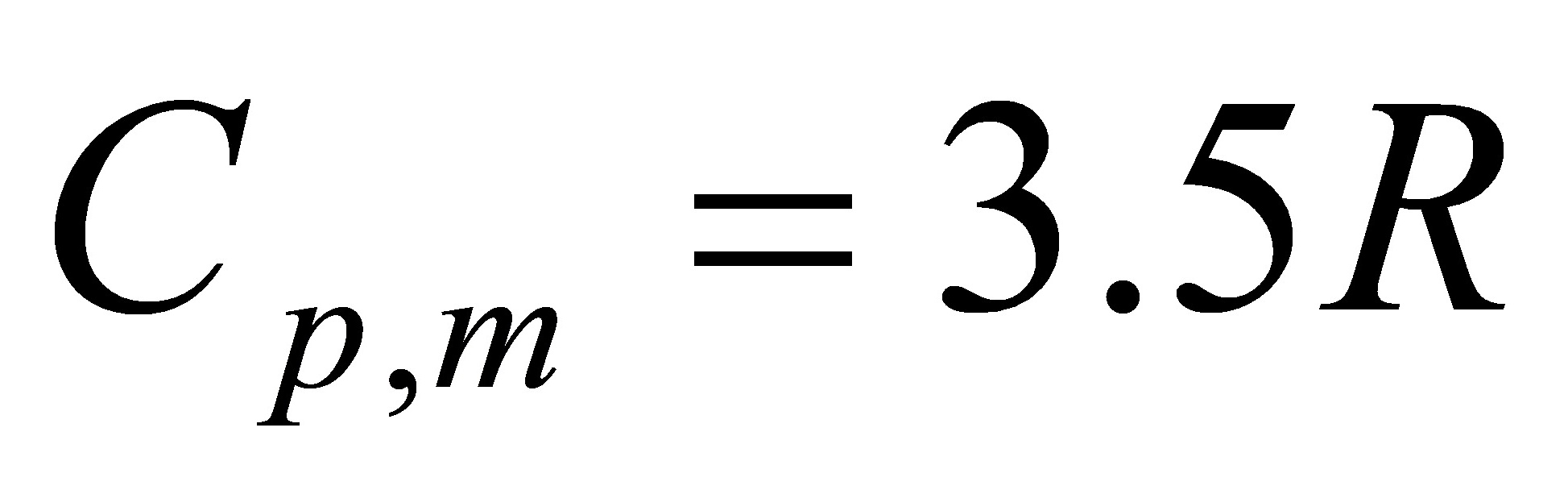 ,
,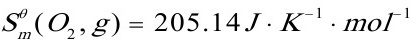 。
。
[解]由于是绝热可逆压缩 Q=0 △S体系=0
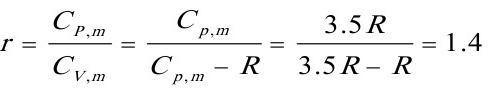
根据绝热过程方程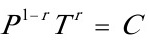 得
得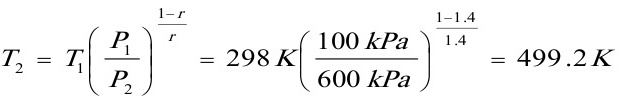
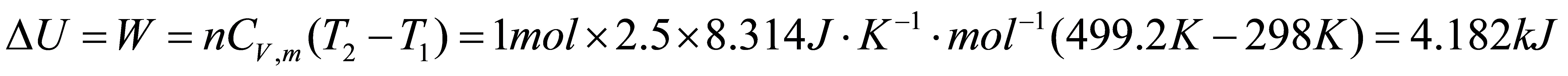
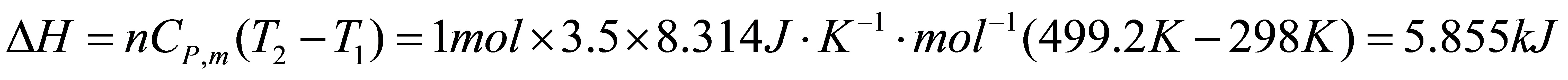
△A=△U- S△T=4182J-205.14J•K-1•mol-1×1mol×(499.2K-298K) =-37.092kJ
△G=△H- S△T=5855J-205.14J•K-1•mol-1×1mol×(499.2K-298K)
=-35.42kJ
△S环境=-Q/T=0
△Siso=△S体系+△S环境=0
[13]将1mol双原子理想气体从始态298K,100kPa,绝热可逆压缩到体积为5dm3,试求终态的温度、压力和过程的Q,W,△U,△H,和△S。
[解]对于双原子理想气体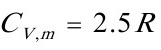
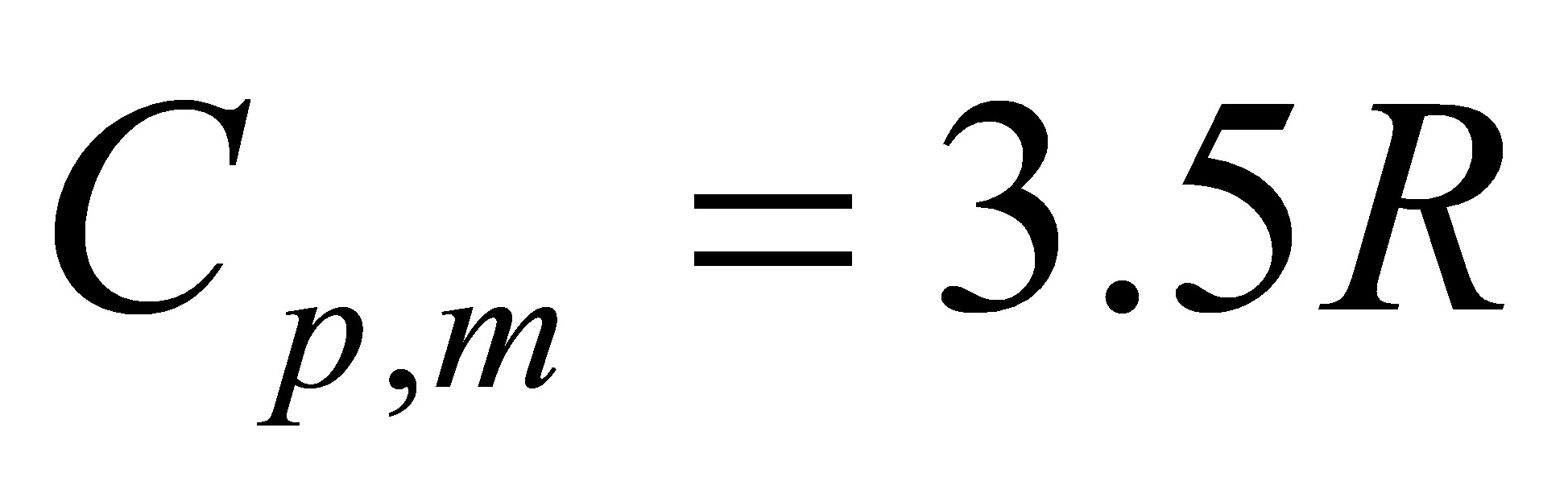
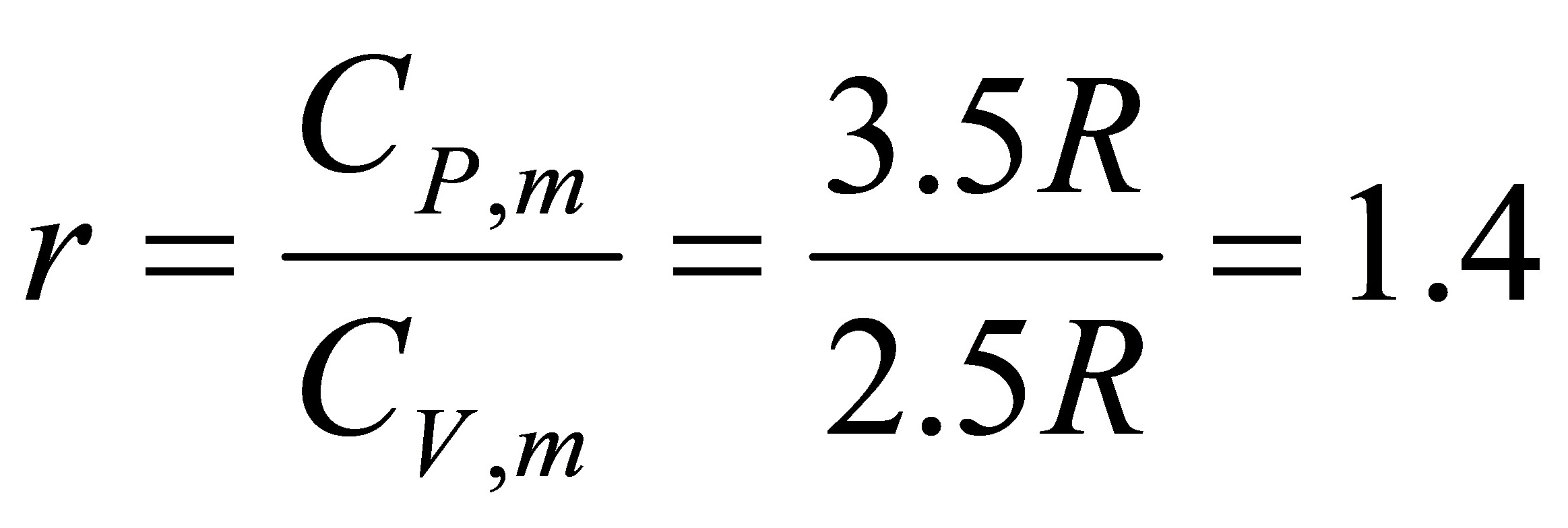
而 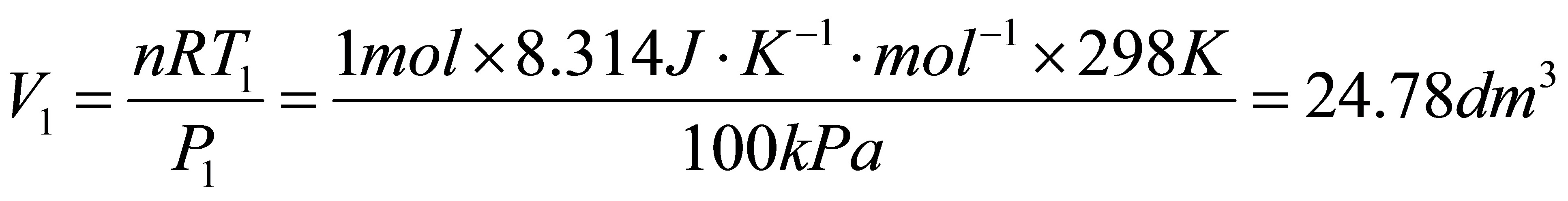
根据 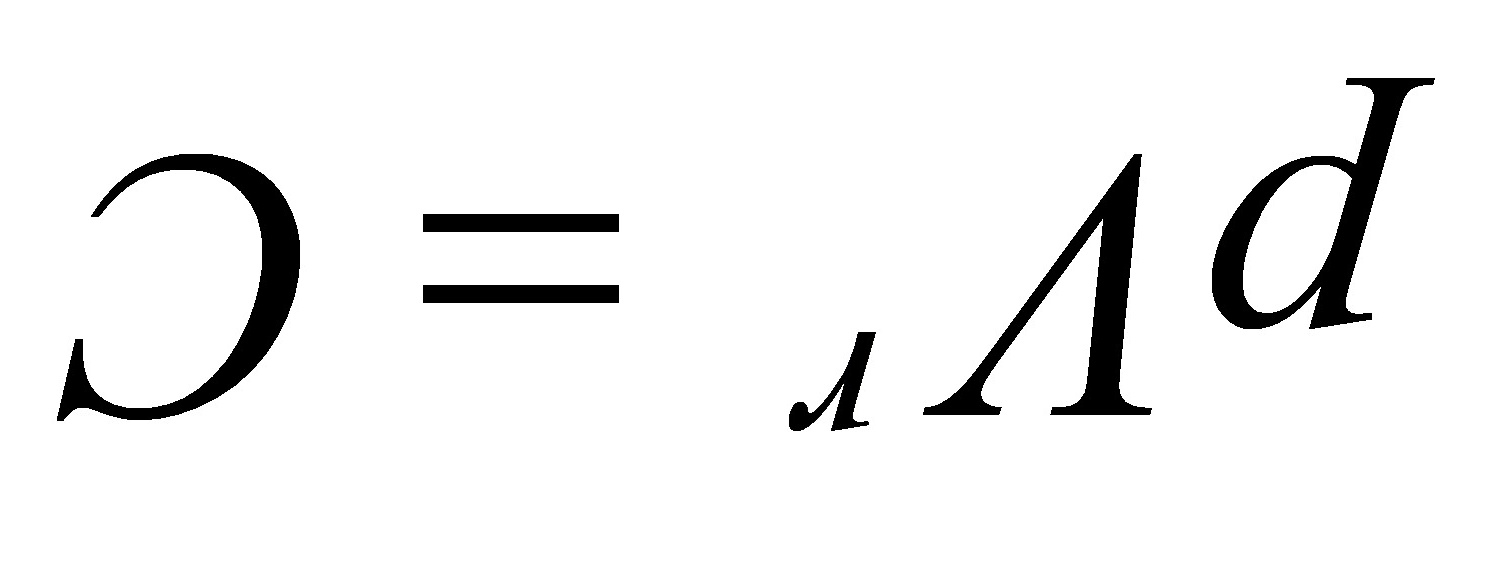 得:
得:
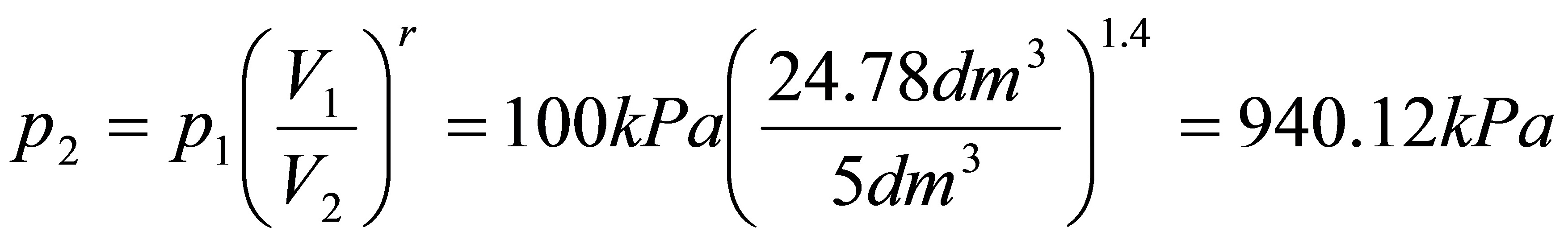
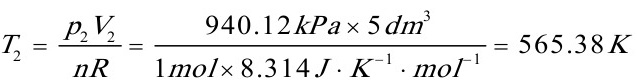
因为是绝热可逆,所以Q=0 △S=0
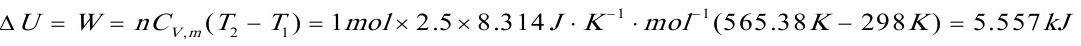
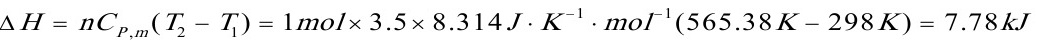
[14]将1mol苯C6H6(l)在正常沸点353K和101.3kPa压力下,向真空蒸发为同温、同压的蒸气,已知在该条件下,苯的摩尔汽化焓为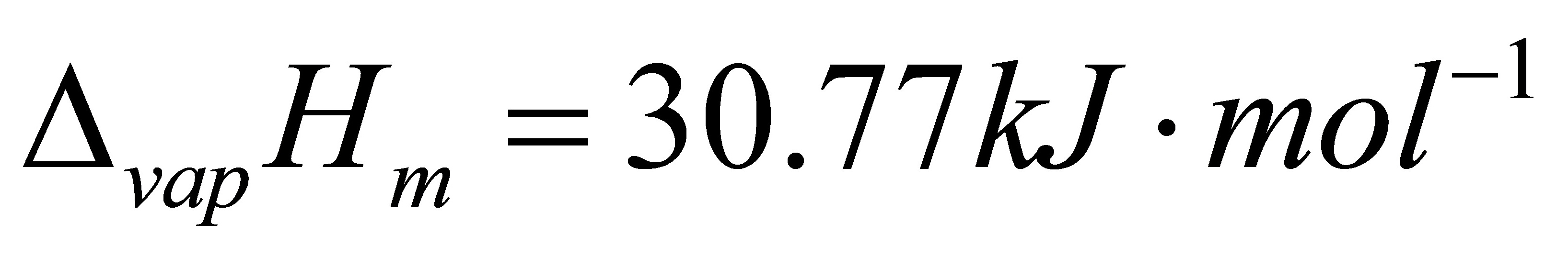 ,设气体为理想气体。试求
,设气体为理想气体。试求
(1)该过程的Q和W;
(2)苯的摩尔汽化熵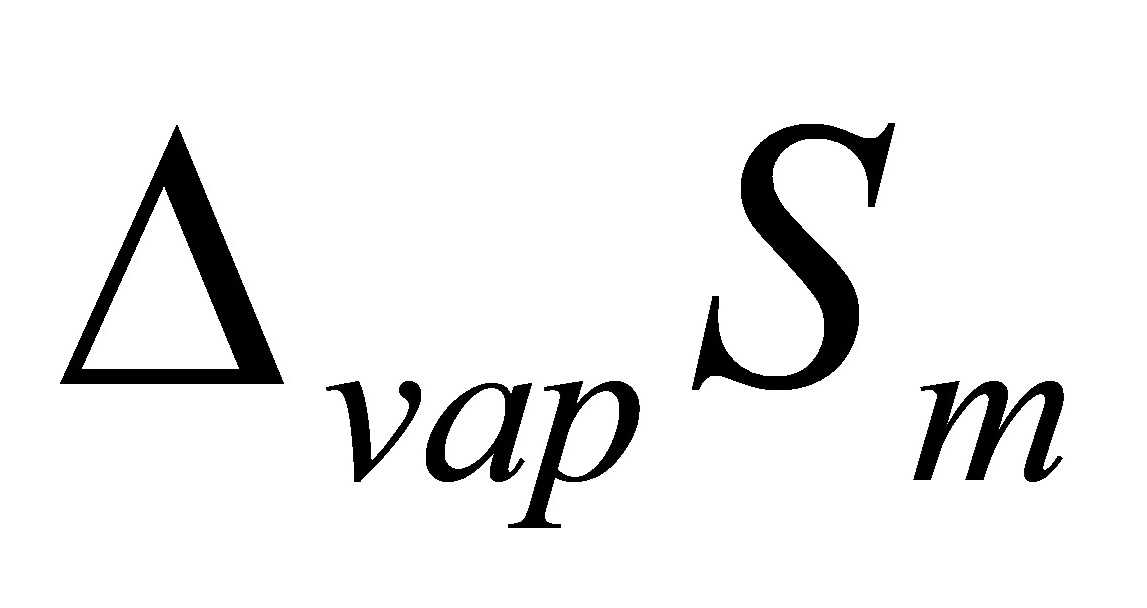 和摩尔汽化Gibbs自由能
和摩尔汽化Gibbs自由能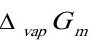 ;
;
(3)环境的熵变△S环;
(4)根据计算结果,判断上述过程的可逆性。
[解](1)向真空蒸发 W=0
Q=△U
而△U为状态函数的变化所以当等温等压时相变时:
W′=-nRT=-1mol×8.314J•K-1•mol-1×353K=-2.935kJ
Q=△H=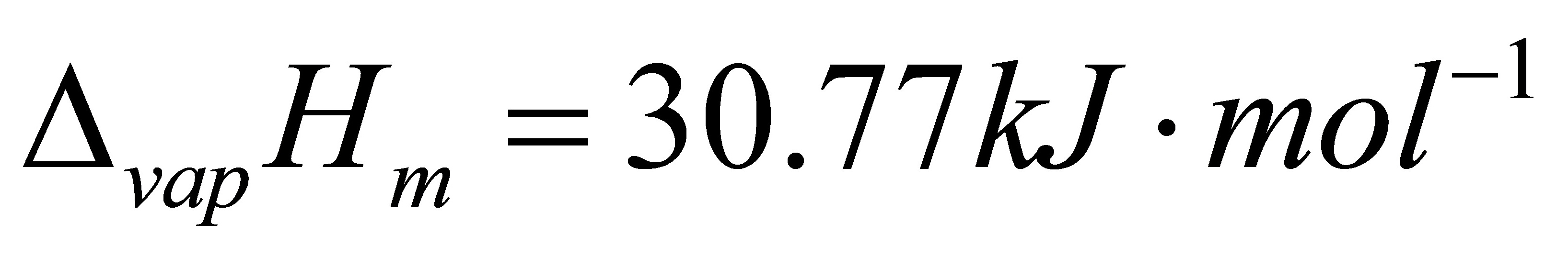
△U=Q+W=30.77kJ-2.935kJ=27.835kJ
所以Q=27.835kJ
(2)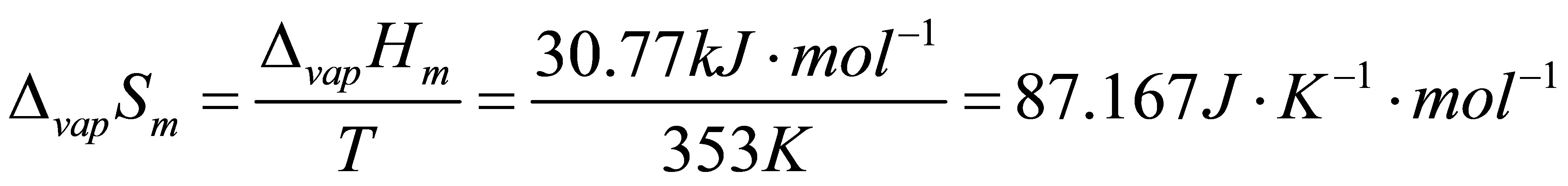
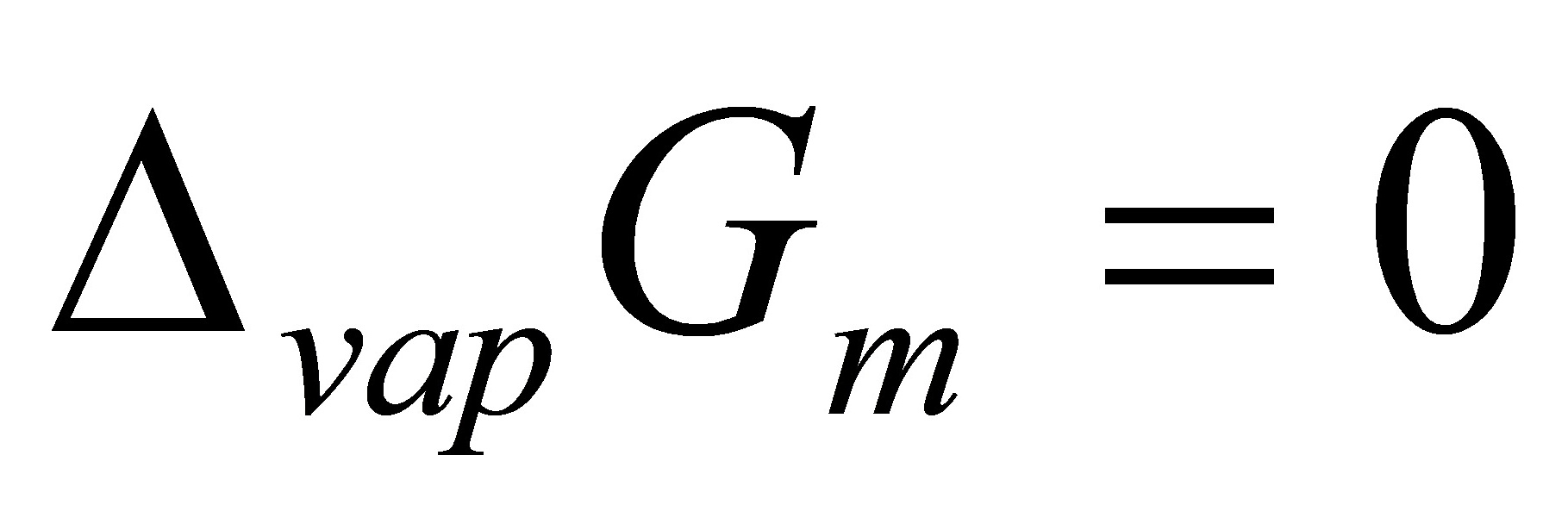 (G是状态函数,所以△G与可逆相变时相同)
(G是状态函数,所以△G与可逆相变时相同)
(3)△S环境=-Q/T=-27.835kJ/353K=-78.85J•K-1
(4)△Siso=△S体系+△S环境=87.167J•K-1-78.85J•K-1=8.317J•K-1
即 △Siso>0 可见是不可逆过程.
[15]某一化学反应,在298K和大气压力下进行,当反应进度为1mol时,放热40.0kJ,如果使反应通过可逆电池来完成,反应程度相同,则吸热4.0kJ。
(1)计算反应进度为1mol时的熵变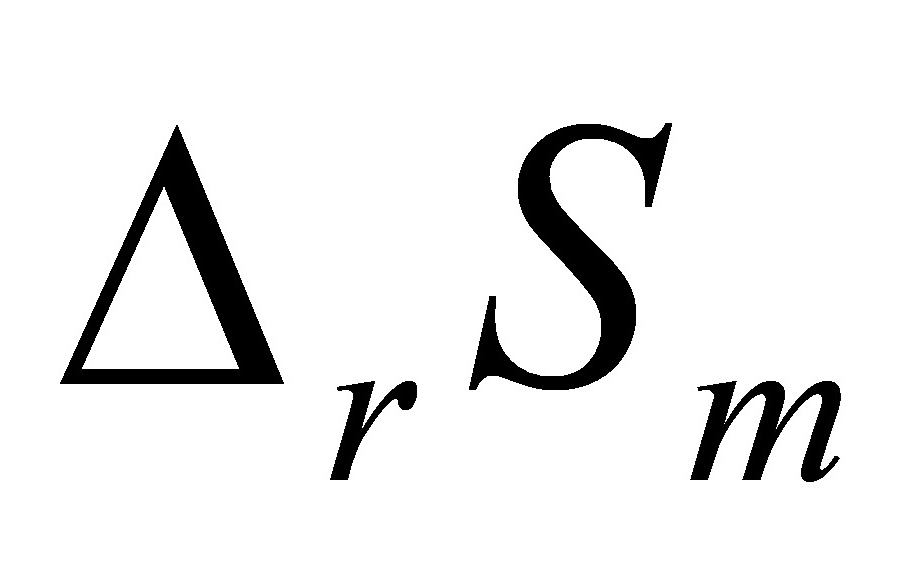 ;
;
(2)当反应不通过可逆电池完成时,求环境的熵变和隔离系统的总熵变,从隔离系统的总熵变值说明了什么问题;
(3)计算系统可能做的最大功的值。
[解](1)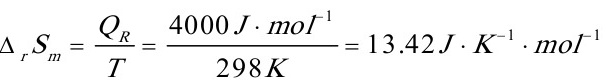
(2)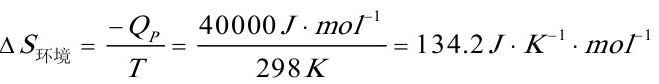
△Siso=△S体系+△S环境
=13.4J•K-1•mol-1+134.2J•K-1•mol-1=147.6 J•K-1•mol-1
即 △Siso>0 可见是不可逆过程.
(3)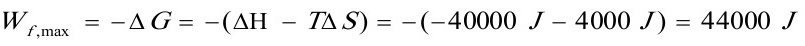
[16] 1mol单原子理想气体从始态273K,100kPa,分别经下列可逆变化到达各自的终态,试计算各过程的Q,W,△U,△H,△S,△A和△G。已知该气体在273K,100kPa的摩尔熵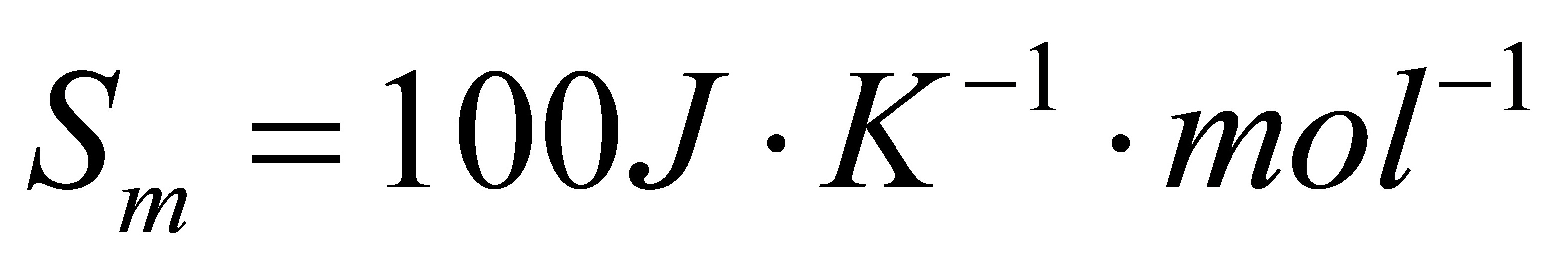 。
。
(1)恒温下压力加倍;
(2)恒压下体积加倍;
(3)恒容下压力加倍;
(4)绝热可逆膨胀至压力减少一半;
(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。
[解](1)恒温下压力加倍(即等温可逆)
△U=△H=0
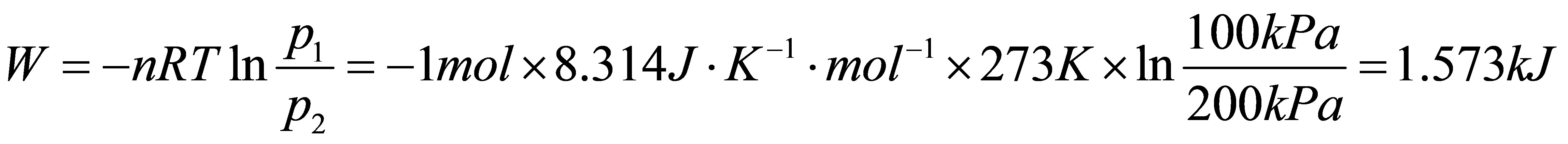
Q=-W=-1.573kJ
△S=Q/T=-1.573kJ/273K=-5.76J•K-1
△A=△U-T△S=-Q=W=1.573kJ
△G=△H-T△S=-Q=W=1.573kJ
(2)恒压下体积加倍T2=2T1
W=-P(V2-V1)=-P1V1=-nRT
=-1mol×8.314J•K-1•mol-1×273K
=-2.27kJ
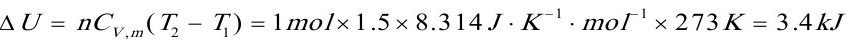
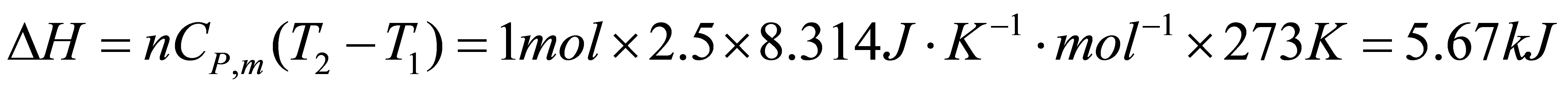
Q=△U-W=3.4kJ+2.27kJ=5.67kJ
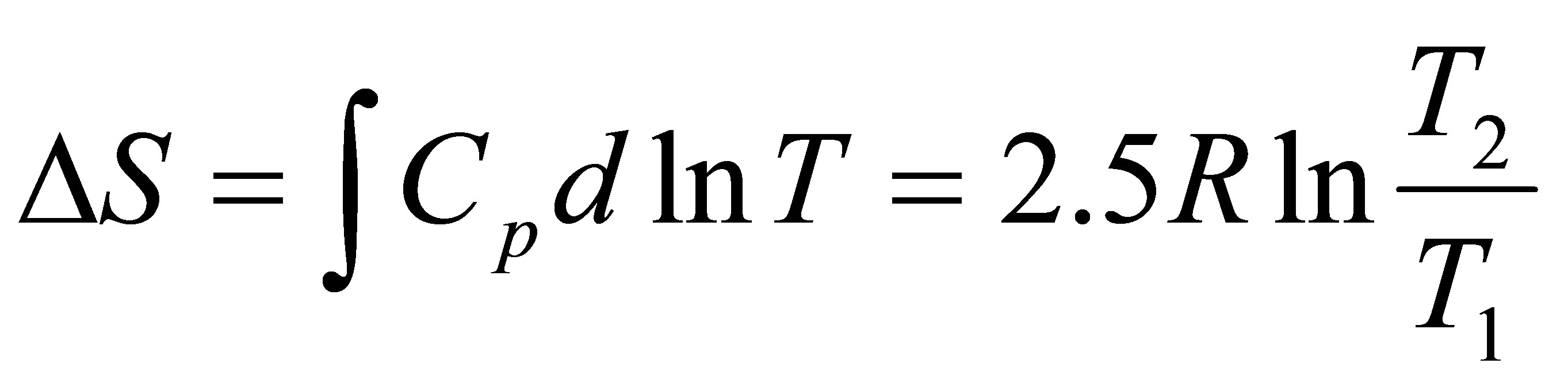

S2=△S+S1=14.4J•K-1+100J•K-1=114.4J•K-1
△A=△U-△TS=△U-(T2S2-T1S1)
=3.4×103J-(2×273K×114.4J•K-1-273K×100J•K-1)
=-31.76kJ
△G=△H-△TS=△H-(T2S2-T1S1)
=5.67×103J-(2×273K×114.4J•K-1-273K×100J•K-1)
=-29.49kJ
(3)恒容下压力加倍 T2=2T1
W=0
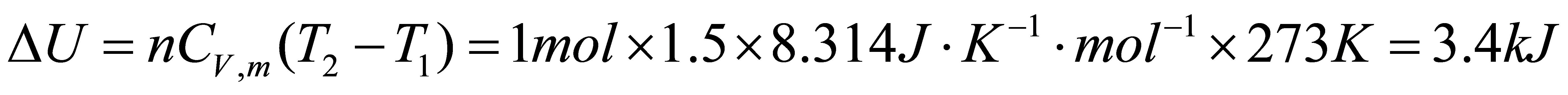
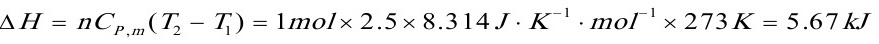
Q=△U=3.4kJ
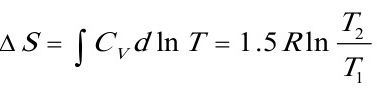
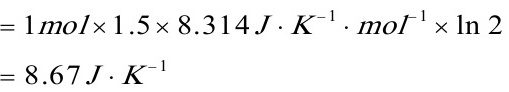
S2=△S+S1=8.67J•K-1+100J•K-1=108.67J•K-1
△A=△U-△TS=△U-(T2S2-T1S1)
=3.4×103J-(2×273K×108.67J•K-1-273K×100J•K-1)
=-28.63kJ
△G=△H-△TS=△H-(T2S2-T1S1)
=5.67×103J-(2×273K×108.67J•K-1-273K×100J•K-1)