题目
处于平衡态,相同体积和质量的一瓶氧气和氮气,内能相同,则A温度和分子数密度相同B温度相同,分子数密度不同C温度不同,分子数密度相同D温度和分子数都不同
处于平衡态,相同体积和质量的一瓶氧气和氮气,内能相同,则
A温度和分子数密度相同
B温度相同,分子数密度不同
C温度不同,分子数密度相同
D温度和分子数都不同
题目解答
答案
答案:A
解析:
1. 首先明确理想气体内能公式:
- 对于理想气体,内能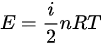 ,
,
2. 然后分析氧气和氮气的情况:
- 相同体积和质量的一瓶氧气和氮气,由于体积相同,所以它们的分子数密度(n/V)相同。
- 又已知它们内能相同,而氧气是双原子分子,自由度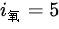 ;氮气也是双原子分子,自由度
;氮气也是双原子分子,自由度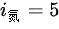 ,即两种气体自由度相同。
,即两种气体自由度相同。
- 由内能公式可知,在分子数密度相同、自由度相同且内能相同的情况下,温度必然相同。
综上所述,答案是 A,温度和分子数密度相同。
解析
步骤 1:理想气体内能公式
- 对于理想气体,内能$E=\dfrac {i}{2}nRT$,其中$i$是自由度,$n$是摩尔数,$R$是理想气体常数,$T$是温度。
步骤 2:分析氧气和氮气的分子数密度
- 相同体积和质量的一瓶氧气和氮气,由于体积相同,所以它们的分子数密度($n/V$)相同。
步骤 3:分析氧气和氮气的自由度
- 氧气是双原子分子,自由度$i=5$;氮气也是双原子分子,自由度$i=5$,即两种气体自由度相同。
步骤 4:分析内能相同的情况
- 由内能公式可知,在分子数密度相同、自由度相同且内能相同的情况下,温度必然相同。
- 对于理想气体,内能$E=\dfrac {i}{2}nRT$,其中$i$是自由度,$n$是摩尔数,$R$是理想气体常数,$T$是温度。
步骤 2:分析氧气和氮气的分子数密度
- 相同体积和质量的一瓶氧气和氮气,由于体积相同,所以它们的分子数密度($n/V$)相同。
步骤 3:分析氧气和氮气的自由度
- 氧气是双原子分子,自由度$i=5$;氮气也是双原子分子,自由度$i=5$,即两种气体自由度相同。
步骤 4:分析内能相同的情况
- 由内能公式可知,在分子数密度相同、自由度相同且内能相同的情况下,温度必然相同。