题目
4,处在热力学温度为T的平衡态的1 mol氦气(视为单原子分子理想气体)的内能为dfrac (3)(2)kpi B)dfrac (5)(2)kT(C) dfrac (3)(2)RT (D)5/2RT(k为玻尔兹曼常数,R为普适气体常数)
4,处在热力学温度为T的平衡态的1 mol氦气(视为单原子分子理想气体)的内能为
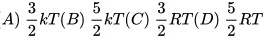
(k为玻尔兹曼常数,R为普适气体常数)
题目解答
答案
单原子分子的能量表达式为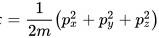 ,有三个平方线,所以根据能量均分定理,单个原子的平均能量为
,有三个平方线,所以根据能量均分定理,单个原子的平均能量为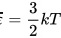 ,那么对于N个氦原子构成的氦气内能为
,那么对于N个氦原子构成的氦气内能为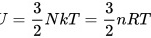 .则 1mol氦气的内能为
.则 1mol氦气的内能为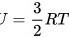 ,选C。
,选C。
解析
步骤 1:确定单原子分子理想气体的内能公式
单原子分子理想气体的内能公式为$U=\dfrac {3}{2}NkT$,其中$N$为分子数,$k$为玻尔兹曼常数,$T$为热力学温度。对于1 mol气体,$N=nN_{A}$,其中$n$为物质的量,$N_{A}$为阿伏伽德罗常数。因此,内能公式可以写为$U=\dfrac {3}{2}nN_{A}kT$。
步骤 2:将普适气体常数R代入内能公式
普适气体常数$R=N_{A}k$,因此内能公式可以进一步简化为$U=\dfrac {3}{2}nRT$。
步骤 3:计算1 mol氦气的内能
对于1 mol氦气,$n=1$,因此内能为$U=\dfrac {3}{2}RT$。
单原子分子理想气体的内能公式为$U=\dfrac {3}{2}NkT$,其中$N$为分子数,$k$为玻尔兹曼常数,$T$为热力学温度。对于1 mol气体,$N=nN_{A}$,其中$n$为物质的量,$N_{A}$为阿伏伽德罗常数。因此,内能公式可以写为$U=\dfrac {3}{2}nN_{A}kT$。
步骤 2:将普适气体常数R代入内能公式
普适气体常数$R=N_{A}k$,因此内能公式可以进一步简化为$U=\dfrac {3}{2}nRT$。
步骤 3:计算1 mol氦气的内能
对于1 mol氦气,$n=1$,因此内能为$U=\dfrac {3}{2}RT$。