题目
15-18 一个容器内储有氧气,其压强为 https:/img.zuoyebang.cc/zyb_7ab82ef45877df948f145358b32eb19b.jpg.013times -|||-^5Ncdot (m)^-2, 温度为300K,求:-|||-(1)氧气的密度;-|||-(2)分子的平均平动动能.

题目解答
答案
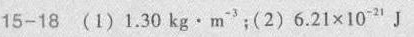
解析
步骤 1:计算氧气的密度
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压强,$V$ 是体积,$n$ 是物质的量,$R$ 是理想气体常数,$T$ 是温度。物质的量 $n$ 可以用质量 $m$ 除以摩尔质量 $M$ 来表示,即 $n=m/M$。因此,理想气体状态方程可以写成 $PV=mRT/M$。密度 $\rho$ 定义为质量 $m$ 除以体积 $V$,即 $\rho=m/V$。将 $m/V$ 代入理想气体状态方程,得到 $\rho=PM/RT$。对于氧气,摩尔质量 $M=32g/mol=0.032kg/mol$,理想气体常数 $R=8.31J/(mol\cdot K)$,代入已知的压强 $P=1.013\times 10^5N/m^2$ 和温度 $T=300K$,可以计算出氧气的密度。
步骤 2:计算分子的平均平动动能
分子的平均平动动能 $\overline{E_k}$ 可以用公式 $\overline{E_k}=(3/2)kT$ 来计算,其中 $k$ 是玻尔兹曼常数,$T$ 是温度。玻尔兹曼常数 $k=1.38\times 10^{-23}J/K$,代入已知的温度 $T=300K$,可以计算出分子的平均平动动能。
根据理想气体状态方程 $PV=nRT$,其中 $P$ 是压强,$V$ 是体积,$n$ 是物质的量,$R$ 是理想气体常数,$T$ 是温度。物质的量 $n$ 可以用质量 $m$ 除以摩尔质量 $M$ 来表示,即 $n=m/M$。因此,理想气体状态方程可以写成 $PV=mRT/M$。密度 $\rho$ 定义为质量 $m$ 除以体积 $V$,即 $\rho=m/V$。将 $m/V$ 代入理想气体状态方程,得到 $\rho=PM/RT$。对于氧气,摩尔质量 $M=32g/mol=0.032kg/mol$,理想气体常数 $R=8.31J/(mol\cdot K)$,代入已知的压强 $P=1.013\times 10^5N/m^2$ 和温度 $T=300K$,可以计算出氧气的密度。
步骤 2:计算分子的平均平动动能
分子的平均平动动能 $\overline{E_k}$ 可以用公式 $\overline{E_k}=(3/2)kT$ 来计算,其中 $k$ 是玻尔兹曼常数,$T$ 是温度。玻尔兹曼常数 $k=1.38\times 10^{-23}J/K$,代入已知的温度 $T=300K$,可以计算出分子的平均平动动能。