题目
[2.15]Li原子的3个电离能分别为 _(1)=5.392eV, _(2)=75.638eV, _(3)=122.451eV, 请计算-|||-Li原子的1s电子结合能。
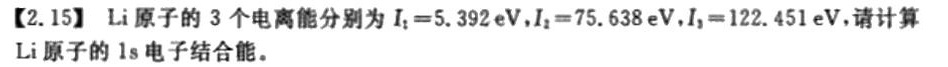
题目解答
答案

解析
考查要点:本题主要考查原子的电离能与电子结合能之间的关系,以及如何利用有效核电荷计算特定电子轨道的结合能。
解题核心思路:
- 电离能与结合能的区别:电离能是移除原子中一个电子所需的能量,而结合能是将电子束缚在原子中的能量(通常为负值)。
- 有效核电荷的概念:由于电子间的屏蔽效应,内层电子感受到的有效核电荷小于原子核电荷。对于1s电子,屏蔽常数$\sigma \approx 0.85$,有效核电荷$Z^* = Z - \sigma$。
- 氢原子能级公式的应用:结合能可由公式$E_n = -13.6 \, \text{eV} \cdot \frac{(Z^*)^2}{n^2}$计算,其中$n=1$对应1s轨道。
破题关键点:
- 明确1s电子的有效核电荷$Z^*$,代入公式计算结合能。
步骤1:确定有效核电荷
Li原子的原子序数$Z=3$,1s电子的屏蔽常数$\sigma \approx 0.85$,因此有效核电荷为:
$Z^* = Z - \sigma = 3 - 0.85 = 2.15$
步骤2:应用氢原子能级公式
1s电子的结合能为:
$E_{1s} = -13.6 \, \text{eV} \cdot \frac{(Z^*)^2}{1^2} = -13.6 \cdot (2.15)^2$
步骤3:计算数值
$(2.15)^2 = 4.6225$
$E_{1s} = -13.6 \cdot 4.6225 \approx -65.3 \, \text{eV}$