题目
设图示的两条曲线分别表示在相同温度下氧气和氢气分子的速率分布曲线;令((v)_(p))(O)_(2)和((v)_(p))(H)_(2)分别表示氧气和氢气的最概然速率,则( )。((v)_(p))(O)_(2)和((v)_(p))(H)_(2)((v)_(p))(O)_(2)和((v)_(p))(H)_(2)
设图示的两条曲线分别表示在相同温度下氧气和氢气分子的速率分布曲线;令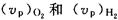 分别表示氧气和氢气的最概然速率,则( )。
分别表示氧气和氢气的最概然速率,则( )。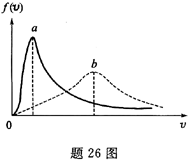

题目解答
答案
B. 图中a表示氧气分子的速率分布曲线; $({v}_{p}){v}_{2}/({v}_{p}){H}_{2}=1/4$
解析
步骤 1:理解最概然速率的定义
最概然速率是指在一定温度下,气体分子速率分布中出现频率最高的速率。根据麦克斯韦速率分布律,最概然速率与分子的质量有关,质量越小,最概然速率越大。
步骤 2:比较氧气和氢气的最概然速率
氧气和氢气在相同温度下,由于氢气分子的质量远小于氧气分子的质量,因此氢气分子的最概然速率远大于氧气分子的最概然速率。即 $({v}_{p}){H}_{2} > ({v}_{p}){O}_{2}$。
步骤 3:确定速率分布曲线
由于氢气分子的最概然速率大于氧气分子的最概然速率,因此氢气分子的速率分布曲线应该在氧气分子的速率分布曲线的右侧。根据题目中的图示,曲线a在曲线b的右侧,因此曲线a表示氢气分子的速率分布曲线,曲线b表示氧气分子的速率分布曲线。
步骤 4:计算最概然速率的比值
根据最概然速率的定义,最概然速率与分子的质量的平方根成反比。即 $({v}_{p}){H}_{2}/({v}_{p}){O}_{2} = \sqrt{M_{O2}/M_{H2}}$,其中 $M_{O2}$ 和 $M_{H2}$ 分别是氧气和氢气的摩尔质量。由于 $M_{O2} = 32 g/mol$,$M_{H2} = 2 g/mol$,因此 $({v}_{p}){H}_{2}/({v}_{p}){O}_{2} = \sqrt{32/2} = 4$。
最概然速率是指在一定温度下,气体分子速率分布中出现频率最高的速率。根据麦克斯韦速率分布律,最概然速率与分子的质量有关,质量越小,最概然速率越大。
步骤 2:比较氧气和氢气的最概然速率
氧气和氢气在相同温度下,由于氢气分子的质量远小于氧气分子的质量,因此氢气分子的最概然速率远大于氧气分子的最概然速率。即 $({v}_{p}){H}_{2} > ({v}_{p}){O}_{2}$。
步骤 3:确定速率分布曲线
由于氢气分子的最概然速率大于氧气分子的最概然速率,因此氢气分子的速率分布曲线应该在氧气分子的速率分布曲线的右侧。根据题目中的图示,曲线a在曲线b的右侧,因此曲线a表示氢气分子的速率分布曲线,曲线b表示氧气分子的速率分布曲线。
步骤 4:计算最概然速率的比值
根据最概然速率的定义,最概然速率与分子的质量的平方根成反比。即 $({v}_{p}){H}_{2}/({v}_{p}){O}_{2} = \sqrt{M_{O2}/M_{H2}}$,其中 $M_{O2}$ 和 $M_{H2}$ 分别是氧气和氢气的摩尔质量。由于 $M_{O2} = 32 g/mol$,$M_{H2} = 2 g/mol$,因此 $({v}_{p}){H}_{2}/({v}_{p}){O}_{2} = \sqrt{32/2} = 4$。