题目
在373 K的等温条件下,1 mol理想气体从始态体积25 dm3,分别按下列四个过程膨胀到终态体积为100 dm3。(1)向真空膨胀;(2)等温可逆膨胀;(3)在外压恒定为气体终态压力下膨胀;(4)先外压恒定为体积等于50 dm3 时气体的平衡压力下膨胀,当膨胀到50 dm3以后,再在外压等于100 dm3 时气体的平衡压力下膨胀。分别计算各个过程中所做的膨胀功,这说明了什么问题
在373 K的等温条件下,1 mol理想气体从始态体积25 dm3,分别按下列四个过程膨胀到终态体积为100 dm3。
(1)向真空膨胀;
(2)等温可逆膨胀;
(3)在外压恒定为气体终态压力下膨胀;
(4)先外压恒定为体积等于50 dm3 时气体的平衡压力下膨胀,当膨胀到50 dm3以后,再在外压等于100 dm3 时气体的平衡压力下膨胀。
分别计算各个过程中所做的膨胀功,这说明了什么问题
题目解答
答案
解:(1)向真空膨胀,外压为零,所以
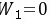
(2)理想气体的等温可逆膨胀
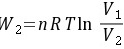
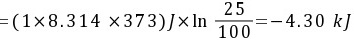
(3)等外压膨胀
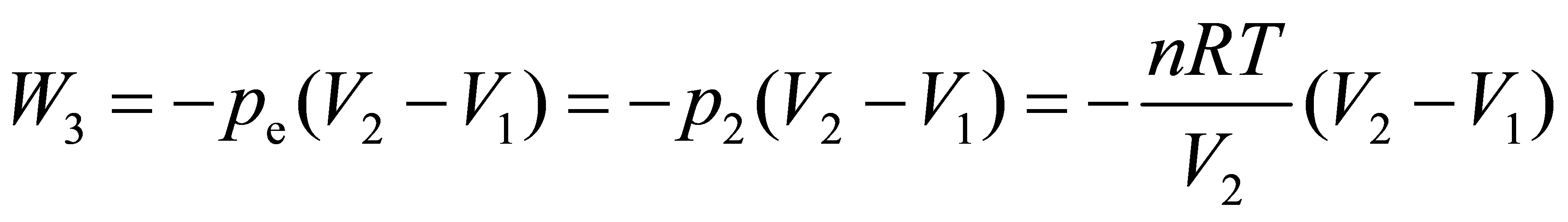
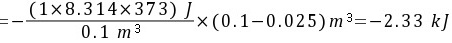
(4)分两步的等外压膨胀
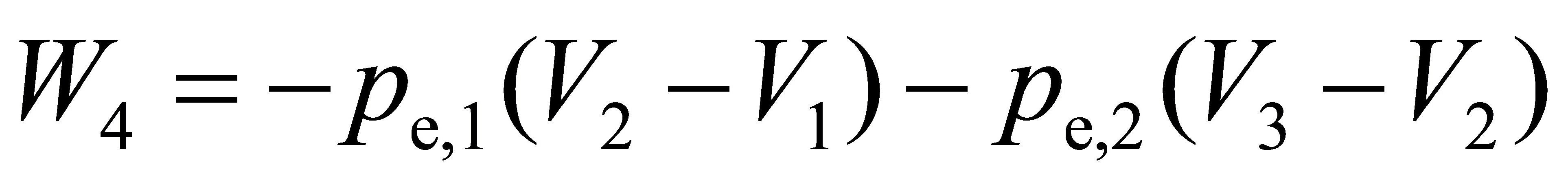
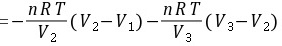
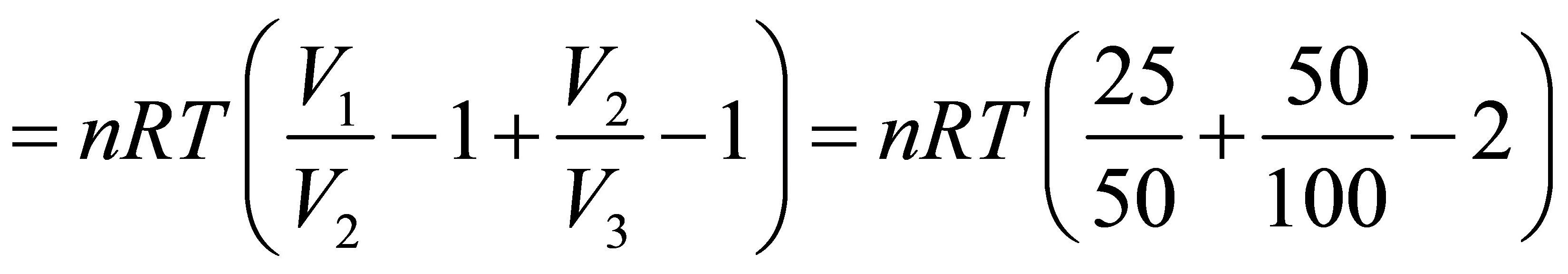
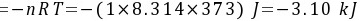
从计算说明了,功不是状态函数,是与过程有关的量。系统与环境的压力差越小,膨胀的次数越多,所做功的绝对值也越大。理想气体的等温可逆膨胀做功最大(指绝对值)。
解析
步骤 1:向真空膨胀
向真空膨胀时,外压为零,因此膨胀功为零。
步骤 2:等温可逆膨胀
等温可逆膨胀的膨胀功可以通过公式计算,其中 $W = -nRT\ln\frac{V_2}{V_1}$,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度,$V_1$ 和 $V_2$ 分别是初始和最终体积。
步骤 3:等外压膨胀
等外压膨胀的膨胀功可以通过公式计算,其中 $W = -P_{ext}(V_2 - V_1)$,$P_{ext}$ 是外压,$V_1$ 和 $V_2$ 分别是初始和最终体积。
步骤 4:分两步的等外压膨胀
分两步的等外压膨胀的膨胀功可以通过公式计算,其中 $W = -P_{ext1}(V_{12} - V_1) - P_{ext2}(V_2 - V_{12})$,$P_{ext1}$ 和 $P_{ext2}$ 分别是两步的外压,$V_1$,$V_{12}$ 和 $V_2$ 分别是初始、中间和最终体积。
向真空膨胀时,外压为零,因此膨胀功为零。
步骤 2:等温可逆膨胀
等温可逆膨胀的膨胀功可以通过公式计算,其中 $W = -nRT\ln\frac{V_2}{V_1}$,$n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度,$V_1$ 和 $V_2$ 分别是初始和最终体积。
步骤 3:等外压膨胀
等外压膨胀的膨胀功可以通过公式计算,其中 $W = -P_{ext}(V_2 - V_1)$,$P_{ext}$ 是外压,$V_1$ 和 $V_2$ 分别是初始和最终体积。
步骤 4:分两步的等外压膨胀
分两步的等外压膨胀的膨胀功可以通过公式计算,其中 $W = -P_{ext1}(V_{12} - V_1) - P_{ext2}(V_2 - V_{12})$,$P_{ext1}$ 和 $P_{ext2}$ 分别是两步的外压,$V_1$,$V_{12}$ 和 $V_2$ 分别是初始、中间和最终体积。