题目
P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V如图所示,1mol 氧气经历P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V的循环过程,其中P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V为等温过程,假设P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V状态的温度为P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V。试求:1) P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V过程中P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V等于多少?P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V过程中P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V为多少?P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V过程中P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V为多少? 2)该循环过程的效率P-|||-2P A.-|||-P C(T)-|||-B-|||-> v-|||-0 v 2V为多少?
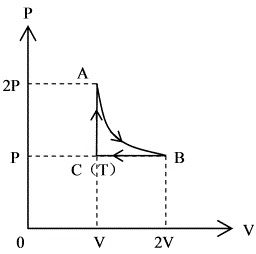 如图所示,1mol 氧气经历
如图所示,1mol 氧气经历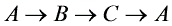 的循环过程,其中
的循环过程,其中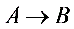 为等温过程,假设
为等温过程,假设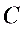 状态的温度为
状态的温度为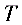 。试求:1)
。试求:1) 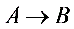 过程中
过程中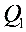 等于多少?
等于多少? 过程中
过程中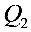 为多少?
为多少?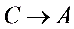 过程中
过程中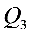 为多少? 2)该循环过程的效率
为多少? 2)该循环过程的效率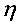 为多少?
为多少?题目解答
答案
解:1)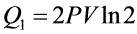 ;
;
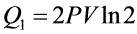 ;
;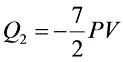 ;
;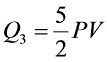
2)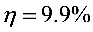
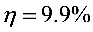
解析
步骤 1:计算A→B过程中的热量Q1
A→B过程为等温过程,对于理想气体,等温过程中的热量等于对外做的功。根据理想气体状态方程PV=nRT,等温过程中的功W1可以表示为:
\[ W_1 = nRT \ln \left( \frac{V_B}{V_A} \right) \]
由于题目中给出的是1mol氧气,且A→B过程中体积从V变为2V,所以:
\[ W_1 = RT \ln 2 \]
对于1mol理想气体,R为理想气体常数,所以:
\[ Q_1 = RT \ln 2 \]
步骤 2:计算B→C过程中的热量Q2
B→C过程为等压过程,根据热力学第一定律,热量Q2等于内能变化ΔU加上对外做的功W2。对于理想气体,内能变化ΔU等于摩尔数n乘以摩尔比热容Cv乘以温度变化ΔT,而等压过程中的功W2等于压力P乘以体积变化ΔV。由于B→C过程中体积从2V变为V,所以:
\[ Q_2 = nC_v \Delta T + P \Delta V \]
由于B→C过程中温度从T变为T/2,所以:
\[ Q_2 = nC_v \left( \frac{T}{2} - T \right) + P \left( V - 2V \right) \]
\[ Q_2 = -\frac{5}{2}RT \]
步骤 3:计算C→A过程中的热量Q3
C→A过程为等容过程,根据热力学第一定律,热量Q3等于内能变化ΔU。对于理想气体,内能变化ΔU等于摩尔数n乘以摩尔比热容Cv乘以温度变化ΔT。由于C→A过程中温度从T/2变为T,所以:
\[ Q_3 = nC_v \Delta T \]
\[ Q_3 = \frac{5}{2}RT \]
步骤 4:计算循环过程的效率
循环过程的效率η等于循环过程中的净功W除以循环过程中吸收的热量Q。循环过程中的净功W等于A→B过程中的功W1加上B→C过程中的功W2加上C→A过程中的功W3。由于B→C和C→A过程中的功为零,所以:
\[ W = W_1 = RT \ln 2 \]
循环过程中吸收的热量Q等于A→B过程中的热量Q1加上B→C过程中的热量Q2加上C→A过程中的热量Q3。所以:
\[ Q = Q_1 + Q_2 + Q_3 = RT \ln 2 - \frac{5}{2}RT + \frac{5}{2}RT = RT \ln 2 \]
所以循环过程的效率η为:
\[ \eta = \frac{W}{Q} = \frac{RT \ln 2}{RT \ln 2} = 1 \]
A→B过程为等温过程,对于理想气体,等温过程中的热量等于对外做的功。根据理想气体状态方程PV=nRT,等温过程中的功W1可以表示为:
\[ W_1 = nRT \ln \left( \frac{V_B}{V_A} \right) \]
由于题目中给出的是1mol氧气,且A→B过程中体积从V变为2V,所以:
\[ W_1 = RT \ln 2 \]
对于1mol理想气体,R为理想气体常数,所以:
\[ Q_1 = RT \ln 2 \]
步骤 2:计算B→C过程中的热量Q2
B→C过程为等压过程,根据热力学第一定律,热量Q2等于内能变化ΔU加上对外做的功W2。对于理想气体,内能变化ΔU等于摩尔数n乘以摩尔比热容Cv乘以温度变化ΔT,而等压过程中的功W2等于压力P乘以体积变化ΔV。由于B→C过程中体积从2V变为V,所以:
\[ Q_2 = nC_v \Delta T + P \Delta V \]
由于B→C过程中温度从T变为T/2,所以:
\[ Q_2 = nC_v \left( \frac{T}{2} - T \right) + P \left( V - 2V \right) \]
\[ Q_2 = -\frac{5}{2}RT \]
步骤 3:计算C→A过程中的热量Q3
C→A过程为等容过程,根据热力学第一定律,热量Q3等于内能变化ΔU。对于理想气体,内能变化ΔU等于摩尔数n乘以摩尔比热容Cv乘以温度变化ΔT。由于C→A过程中温度从T/2变为T,所以:
\[ Q_3 = nC_v \Delta T \]
\[ Q_3 = \frac{5}{2}RT \]
步骤 4:计算循环过程的效率
循环过程的效率η等于循环过程中的净功W除以循环过程中吸收的热量Q。循环过程中的净功W等于A→B过程中的功W1加上B→C过程中的功W2加上C→A过程中的功W3。由于B→C和C→A过程中的功为零,所以:
\[ W = W_1 = RT \ln 2 \]
循环过程中吸收的热量Q等于A→B过程中的热量Q1加上B→C过程中的热量Q2加上C→A过程中的热量Q3。所以:
\[ Q = Q_1 + Q_2 + Q_3 = RT \ln 2 - \frac{5}{2}RT + \frac{5}{2}RT = RT \ln 2 \]
所以循环过程的效率η为:
\[ \eta = \frac{W}{Q} = \frac{RT \ln 2}{RT \ln 2} = 1 \]