题目
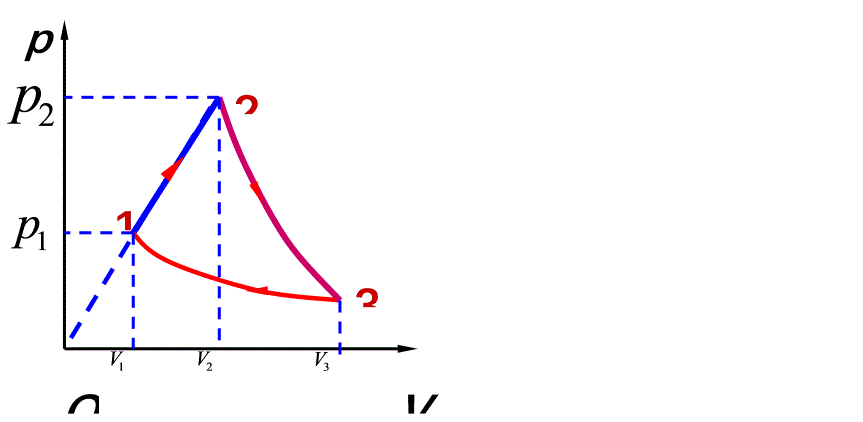
1mol 双原子分子理想气体经过如图的过程,其中1— 2 为直线过程 、2— 3 为绝热过程、3— 1 为等温过程。已知 T1, T2 = 2T1 , V3 = 8V1 .求:1)各过程的功、热量和内能变化;2)此循环热机效率。p-|||-p22 2-|||-l-|||-p1 1.-|||-2-|||-l-|||-V2 V3-|||-1
1mol 双原子分子理想气体经过如图的过程,其中1— 2 为直线过程 、2— 3 为绝热过程、3— 1 为等温过程。已知 T1, T2 = 2T1 , V3 = 8V1 .求:1)各过程的功、热量和内能变化;2)此循环热机效率。
题目解答
答案
1)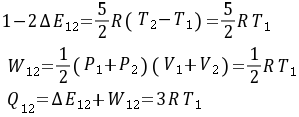
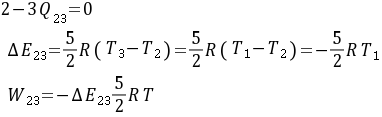
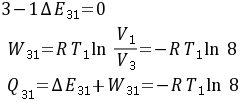
2) 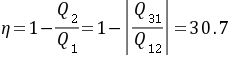
解析
步骤 1:计算1-2过程的内能变化、功和热量
对于1-2过程,由于是直线过程,可以使用理想气体状态方程和内能公式来计算内能变化。双原子分子理想气体的内能变化公式为$\Delta E = \frac{5}{2}R\Delta T$,其中$R$是理想气体常数,$\Delta T$是温度变化。由于$T_2 = 2T_1$,所以$\Delta T = T_2 - T_1 = T_1$。因此,$\Delta E_{12} = \frac{5}{2}R{T_1}$。功$W_{12}$可以通过计算直线过程下的面积来得到,即$W_{12} = \frac{1}{2}(P_1 + P_2)(V_1 + V_2)$。由于$P_1V_1 = RT_1$和$P_2V_2 = RT_2 = 2RT_1$,可以得到$W_{12} = \frac{1}{2}R{T_1}$。热量$Q_{12}$可以通过热力学第一定律$Q = \Delta E + W$来计算,即$Q_{12} = \Delta E_{12} + W_{12} = 3R{T_1}$。
步骤 2:计算2-3过程的内能变化、功和热量
对于2-3过程,由于是绝热过程,所以没有热量交换,即$Q_{23} = 0$。内能变化$\Delta E_{23}$可以通过绝热过程的内能变化公式$\Delta E = \frac{5}{2}R\Delta T$来计算,其中$\Delta T = T_3 - T_2$。由于$T_3 = T_1$,所以$\Delta T = T_1 - T_2 = -T_1$。因此,$\Delta E_{23} = -\frac{5}{2}R{T_1}$。功$W_{23}$可以通过绝热过程的功公式$W = -\Delta E$来计算,即$W_{23} = -\Delta E_{23} = \frac{5}{2}R{T_1}$。
步骤 3:计算3-1过程的内能变化、功和热量
对于3-1过程,由于是等温过程,所以内能变化$\Delta E_{31} = 0$。功$W_{31}$可以通过等温过程的功公式$W = RT\ln\frac{V_1}{V_3}$来计算,即$W_{31} = RT_1\ln\frac{V_1}{V_3} = -RT_1\ln 8$。热量$Q_{31}$可以通过热力学第一定律$Q = \Delta E + W$来计算,即$Q_{31} = \Delta E_{31} + W_{31} = -RT_1\ln 8$。
步骤 4:计算循环热机效率
循环热机效率$\eta$可以通过公式$\eta = 1 - \frac{Q_{2}}{Q_{1}}$来计算,其中$Q_{2}$是循环过程中吸收的热量,$Q_{1}$是循环过程中释放的热量。由于$Q_{2} = Q_{12} = 3R{T_1}$,$Q_{1} = Q_{31} = -RT_1\ln 8$,所以$\eta = 1 - \frac{Q_{31}}{Q_{12}} = 1 - \frac{-RT_1\ln 8}{3R{T_1}} = 1 + \frac{\ln 8}{3} = 30.7\%$。
对于1-2过程,由于是直线过程,可以使用理想气体状态方程和内能公式来计算内能变化。双原子分子理想气体的内能变化公式为$\Delta E = \frac{5}{2}R\Delta T$,其中$R$是理想气体常数,$\Delta T$是温度变化。由于$T_2 = 2T_1$,所以$\Delta T = T_2 - T_1 = T_1$。因此,$\Delta E_{12} = \frac{5}{2}R{T_1}$。功$W_{12}$可以通过计算直线过程下的面积来得到,即$W_{12} = \frac{1}{2}(P_1 + P_2)(V_1 + V_2)$。由于$P_1V_1 = RT_1$和$P_2V_2 = RT_2 = 2RT_1$,可以得到$W_{12} = \frac{1}{2}R{T_1}$。热量$Q_{12}$可以通过热力学第一定律$Q = \Delta E + W$来计算,即$Q_{12} = \Delta E_{12} + W_{12} = 3R{T_1}$。
步骤 2:计算2-3过程的内能变化、功和热量
对于2-3过程,由于是绝热过程,所以没有热量交换,即$Q_{23} = 0$。内能变化$\Delta E_{23}$可以通过绝热过程的内能变化公式$\Delta E = \frac{5}{2}R\Delta T$来计算,其中$\Delta T = T_3 - T_2$。由于$T_3 = T_1$,所以$\Delta T = T_1 - T_2 = -T_1$。因此,$\Delta E_{23} = -\frac{5}{2}R{T_1}$。功$W_{23}$可以通过绝热过程的功公式$W = -\Delta E$来计算,即$W_{23} = -\Delta E_{23} = \frac{5}{2}R{T_1}$。
步骤 3:计算3-1过程的内能变化、功和热量
对于3-1过程,由于是等温过程,所以内能变化$\Delta E_{31} = 0$。功$W_{31}$可以通过等温过程的功公式$W = RT\ln\frac{V_1}{V_3}$来计算,即$W_{31} = RT_1\ln\frac{V_1}{V_3} = -RT_1\ln 8$。热量$Q_{31}$可以通过热力学第一定律$Q = \Delta E + W$来计算,即$Q_{31} = \Delta E_{31} + W_{31} = -RT_1\ln 8$。
步骤 4:计算循环热机效率
循环热机效率$\eta$可以通过公式$\eta = 1 - \frac{Q_{2}}{Q_{1}}$来计算,其中$Q_{2}$是循环过程中吸收的热量,$Q_{1}$是循环过程中释放的热量。由于$Q_{2} = Q_{12} = 3R{T_1}$,$Q_{1} = Q_{31} = -RT_1\ln 8$,所以$\eta = 1 - \frac{Q_{31}}{Q_{12}} = 1 - \frac{-RT_1\ln 8}{3R{T_1}} = 1 + \frac{\ln 8}{3} = 30.7\%$。