1mol单原子理想气体,从始态273K、100kPa,分别经下列可逆变化到达各自的终态,试计算各过程的Q、W、ΔU、ΔH、ΔS、ΔA和ΔG.已知该气体在273K、100kPa的摩尔熵Sm=100 J·K—1·mol—1.(1)恒温下压力加倍;(2)恒压下体积加倍;(3)恒容下压力加倍;(4)绝热可逆膨胀至压力减少一半;(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。
1mol单原子理想气体,从始态273K、100kPa,分别经下列可逆变化到达各自的终态,试计算各过程的Q、W、ΔU、ΔH、ΔS、ΔA和ΔG.已知该气体在273K、100kPa的摩尔熵Sm=100 J·K—1·mol—1.
(1)恒温下压力加倍;
(2)恒压下体积加倍;
(3)恒容下压力加倍;
(4)绝热可逆膨胀至压力减少一半;
(5)绝热不可逆反抗50kPa恒外压膨胀至平衡。
题目解答
答案
解 (1) 理想气体恒温ΔU1=ΔH1=0
W1=—Q1=—nRTln(p1/p2)=—[1×8。315×273×ln(1/2)]J
=1573J
ΔS1= nRln(p1/ p2)= [1×8.315×ln(1/2)]=—5.763J·K—1。
ΔA1=ΔU1—TΔS1=—TΔS1= W1=1573J
ΔG1=ΔH1-TΔS1=—TΔS1=1573J
(2) 恒压下体积加倍V1/T1=V2/T2=2V1/T2,则T2=2T1,
ΔU2=nCV,m(T2-T1)=n(3/2)RT1=(1×1.5×8.3145×273)J
=3405J
ΔH2=nCp,m(T2—T1)=n(5/2)RT1=(1×2.5×8。3145×273)J
=5675J
恒压Q2=ΔH2=5675J,W2=ΔU2-Q2=3405J—5675J=—2270J
ΔS2= nCV,mln(T2/T1)+nRln(V2/V1)=(CV,m+R)nln2
=nCp,mln2
=[(5/2)×8。3145×1×ln2] J·K—1=14。41 J·K—1
ΔA2=ΔU2-(S1ΔT+T2ΔS2)
= 3405J-(100 J·K-1×273K+2×273K×14。41 J·K—1)
=—31。763kJ
ΔG2=ΔH2-(S1ΔT+T2ΔS2)
= 5675J—(100 J·K-1×273K+2×273K×14.41 J·K—1)
=-29.493kJ
(3) 恒容W3=0,压力加倍,温度也加倍.
ΔU3=nCV,m(T2—T1)=n(3/2)RT1=(1×1。5×8.3145×273)J
=3405J
ΔH3=nCp,m(T2-T1)=n(5/2)RT1=(1×2。5×8。3145×273)J
=5675J
Q3=ΔU3=3405J
ΔS3= nCV,mln(T2/T1)
=[1×(3/2)×8。3145×ln2] J·K-1=8.644 J·K-1
ΔA3=ΔU3—(S1ΔT+T2ΔS3)
= 3405J-(100 J·K-1×273K+2×273K×8。644J·K—1)
=-28.615kJ
ΔG3=ΔH3—(S1ΔT+T2ΔS3)
= 5675J-(100 J·K—1×273K+2×273K×8。644 J·K—1)
=-26.345kJ
(4)绝热可逆膨胀至压力减少一半
= Cp,m /CV,m=5/3,
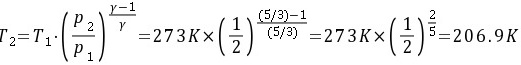
ΔU4=nCV,m(T2-T1)=n(3/2)R(T2—T1)
=(1×1.5×8.3145×(206.9—273)J
=-824J
ΔH4=nCp,m(T2-T1)= (1×2.5×8.3145×(206。9—273)J
=-1374J
ΔS4=0,Q4=0,W4=ΔU4=—824J
ΔA4=ΔU4-[S1(T2-T1)+T2ΔS4]
= -824J-[100 J·K-1×(206。9 K —273K)]
=5786J
ΔG4=ΔH4—(S1ΔT+T2ΔS4)
= —1374J -[100 J·K-1×(206。9 K -273K)]
=5236J
(5)绝热不可逆反抗50kPa恒外压膨胀至平衡
Q5=0,ΔU5=W5
nCV,m(T2-T1)=—p2(V2—V1)=—nR[T2-(p2/p1)T1]
T2=218。4K
ΔU5=W5=nCV,m(T2-T1)= n(3/2)R(T2-T1)
=(1×1.5×8。3145×(218。4—273)J
=-681J
ΔH5= nCp,m(T2—T1)= n(5/2)R(T2—T1)
=(1×2.5×8。3145×(218。4-273)J
=—1135J
ΔS5= nCp,mln(T2/T1)—nRln(p2/p1)
=(1×2。5×8。3145×ln(218。4/273)—1×8.3145×ln(50/100)
=1.125 J·K-1
ΔA5=ΔU5—[S1(T2—T1)+T2ΔS5]
=—681J-[100J·K—1×(218。4K—273K)+218.4K×1。125J·K-1]
=4533.3J
ΔG5=ΔH5—(S1ΔT+T2ΔS5)
=—1135J-[100J·K—1×(218.4K-273K)+218.4K×1.125J·K—1]
=4079。3J