题目
如图所示,一绝热密闭的容器,用隔板分成相等的两部分,左边盛有一定量的理想气体,压强为P0,右边为真空.今将隔板抽去,气体自由膨胀,当气体达到平衡时,气体的压强是( ). .-|||-:-|||-. .-|||-. . . . . .-|||-. .-|||-.. ...-|||-. . . .A.P03γB.P02C.P0D.P02γ
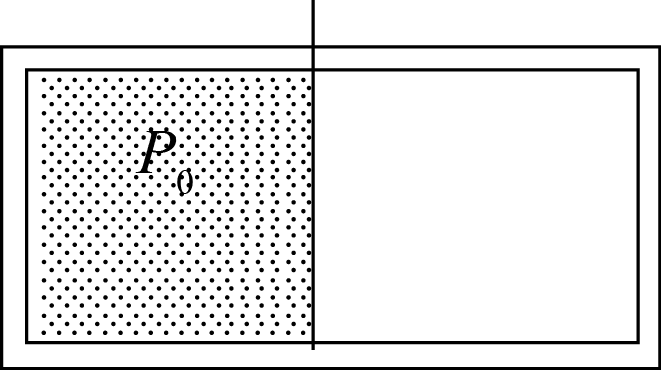
如图所示,一绝热密闭的容器,用隔板分成相等的两部分,左边盛有一定量的理想气体,压强为P0,右边为真空.今将隔板抽去,气体自由膨胀,当气体达到平衡时,气体的压强是( )
- A.P03γ
- B.P02
- C.P0
- D.P02γ
题目解答
答案
B
解析
考查要点:本题主要考查理想气体在绝热条件下的自由膨胀过程,需理解绝热过程与自由膨胀的特点,以及如何应用理想气体状态方程。
解题核心思路:
- 明确过程性质:容器绝热且气体自由膨胀,无热量交换(Q=0),且膨胀过程中气体对外做功为零(W=0)。
- 内能变化分析:根据热力学第一定律 $\Delta U = Q + W$,可知 $\Delta U = 0$,即温度保持不变。
- 应用理想气体状态方程:体积变为原来的两倍,温度不变,压强按反比例关系变化。
破题关键点:
- 区分绝热过程与自由膨胀:虽然容器绝热,但自由膨胀无做功,内能不变,温度恒定。
- 体积变化倍数:原体积为容器一半,膨胀后体积翻倍。
过程分析:
- 初始状态:气体占据容器左侧体积 $V$,压强为 $P_0$,温度为 $T$。
- 膨胀过程:隔板抽去后,气体自由膨胀至整个容器,体积变为 $2V$。
- 能量守恒:绝热且无做功,$\Delta U = 0$,温度 $T$ 不变。
- 理想气体方程:初始状态 $P_0 V = nRT$,平衡后 $P \cdot 2V = nRT$。
- 压强计算:联立得 $P = \frac{P_0 V}{2V} = \frac{P_0}{2}$。
结论:平衡时压强为 $P_0/2$,对应选项 B。