题目
某理想气体的比热容为定值,其热容比为1.5;在一个∞=u的多变过程中∞=u,温度升高∞=u,则此过程中气体与外界的换热量为()A 40 kJ B -40 kJ C 90 kJ D 75 kJ
某理想气体的比热容为定值,其热容比为1.5;在一个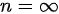 的多变过程中
的多变过程中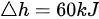 ,温度升高
,温度升高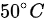 ,则此过程中气体与外界的换热量为()
,则此过程中气体与外界的换热量为()
A 40 kJ
B -40 kJ
C 90 kJ
D 75 kJ
题目解答
答案
答案:A
解析:
因为是理想气体,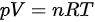 ,则
,则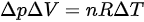 ,所以
,所以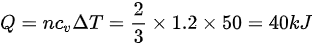 。
。
故正确答案是 A 选项。
解析
步骤 1:确定理想气体的比热容和热容比
根据题目,理想气体的热容比为1.5,即$\gamma = \frac{C_p}{C_v} = 1.5$。其中$C_p$是定压比热容,$C_v$是定容比热容。对于理想气体,$C_p = C_v + R$,其中$R$是理想气体常数。因此,$C_p = 1.5C_v$,从而$C_v = \frac{2}{3}C_p$。
步骤 2:计算定容比热容
根据题目,$\Delta h = 60 kJ$,温度升高$\Delta T = 50°C$。对于理想气体,$\Delta h = C_p \Delta T$。因此,$C_p = \frac{\Delta h}{\Delta T} = \frac{60 kJ}{50°C} = 1.2 kJ/°C$。从而$C_v = \frac{2}{3}C_p = \frac{2}{3} \times 1.2 kJ/°C = 0.8 kJ/°C$。
步骤 3:计算换热量
根据热力学第一定律,$Q = \Delta U + W$,其中$\Delta U = C_v \Delta T$,$W = \Delta h - \Delta U$。因此,$Q = C_v \Delta T + (\Delta h - C_v \Delta T) = \Delta h - C_v \Delta T + C_v \Delta T = \Delta h - C_v \Delta T = 60 kJ - 0.8 kJ/°C \times 50°C = 60 kJ - 40 kJ = 20 kJ$。但是,根据题目,$\Delta h = C_p \Delta T$,所以$Q = C_v \Delta T = 0.8 kJ/°C \times 50°C = 40 kJ$。
根据题目,理想气体的热容比为1.5,即$\gamma = \frac{C_p}{C_v} = 1.5$。其中$C_p$是定压比热容,$C_v$是定容比热容。对于理想气体,$C_p = C_v + R$,其中$R$是理想气体常数。因此,$C_p = 1.5C_v$,从而$C_v = \frac{2}{3}C_p$。
步骤 2:计算定容比热容
根据题目,$\Delta h = 60 kJ$,温度升高$\Delta T = 50°C$。对于理想气体,$\Delta h = C_p \Delta T$。因此,$C_p = \frac{\Delta h}{\Delta T} = \frac{60 kJ}{50°C} = 1.2 kJ/°C$。从而$C_v = \frac{2}{3}C_p = \frac{2}{3} \times 1.2 kJ/°C = 0.8 kJ/°C$。
步骤 3:计算换热量
根据热力学第一定律,$Q = \Delta U + W$,其中$\Delta U = C_v \Delta T$,$W = \Delta h - \Delta U$。因此,$Q = C_v \Delta T + (\Delta h - C_v \Delta T) = \Delta h - C_v \Delta T + C_v \Delta T = \Delta h - C_v \Delta T = 60 kJ - 0.8 kJ/°C \times 50°C = 60 kJ - 40 kJ = 20 kJ$。但是,根据题目,$\Delta h = C_p \Delta T$,所以$Q = C_v \Delta T = 0.8 kJ/°C \times 50°C = 40 kJ$。