题目
-一个密闭的轻质刚性容器内有质量的氧气,开始时容器以速率做直线运动,现使容器突然停止,假设气体的全部定向运动的动能均转变成分子热运动的动能。则 :(1)容器中氧气温度将上升多少? (2)气体分子的平均平动动能和转动动能各增加多少 ( 以摩尔质量和阿伏伽德罗常量表示 )
-一个密闭的轻质刚性容器内有质量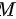 的氧气,开始时容器以速率
的氧气,开始时容器以速率 做直线运动,现使容器突然停止,假设气体的全部定向运动的动能均转变成分子热运动的动能。则 :(1)容器中氧气温度将上升多少?
做直线运动,现使容器突然停止,假设气体的全部定向运动的动能均转变成分子热运动的动能。则 :(1)容器中氧气温度将上升多少?
(2)气体分子的平均平动动能和转动动能各增加多少 ( 以摩尔质量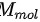 和阿伏伽德罗常量
和阿伏伽德罗常量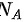 表示 )
表示 )
题目解答
答案
解: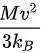 ;
;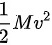 、
、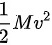
(1) 气体的全部定向运动的动能转变为分子热运动的动能后,气体内部分子的热运动将加强,因此气体温度会上升。根据理想气体状态方程,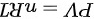 ,可知在容器密闭的情况下,气体的压强
,可知在容器密闭的情况下,气体的压强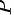 和体积
和体积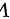 不变,温度T与气体分子运动的平均动能成正比关系。因此,温度的增加量可表示为
不变,温度T与气体分子运动的平均动能成正比关系。因此,温度的增加量可表示为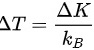 ,其中
,其中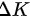 为气体分子平均动能的增加量,
为气体分子平均动能的增加量,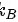 为玻尔兹曼常量。根据动能定理,气体分子热运动的动能等于
为玻尔兹曼常量。根据动能定理,气体分子热运动的动能等于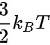 ,因此
,因此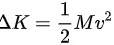 ,代入公式可得:
,代入公式可得: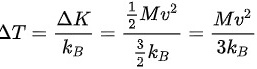 。
。
(2) 根据动能定理,气体分子的平均平动动能和转动动能各增加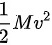 。根据热力学理论,单原子分子气体只有平动动能,因此只会增加平动动能,平动动能的增加量为
。根据热力学理论,单原子分子气体只有平动动能,因此只会增加平动动能,平动动能的增加量为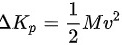 。而对于多原子分子气体,分子既有平动动能,又有转动动能,因此平动动能和转动动能的增加量均为
。而对于多原子分子气体,分子既有平动动能,又有转动动能,因此平动动能和转动动能的增加量均为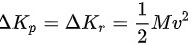 。根据摩尔热容的定义,气体单位摩尔质量温度升高1K时吸收的热量为摩尔热容
。根据摩尔热容的定义,气体单位摩尔质量温度升高1K时吸收的热量为摩尔热容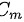 ,因此气体摩尔热容
,因此气体摩尔热容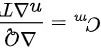 ,其中
,其中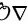 为气体吸收的热量,
为气体吸收的热量,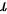 为气体摩尔数,
为气体摩尔数,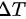 为气体温度升高的量。根据热力学第一定律,气体吸收的热量等于气体内部分子热运动的增加动能,因此
为气体温度升高的量。根据热力学第一定律,气体吸收的热量等于气体内部分子热运动的增加动能,因此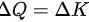 。代入公式可得:气体平动动能和转动动能的增加量均为
。代入公式可得:气体平动动能和转动动能的增加量均为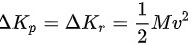 。
。
解析
步骤 1:计算气体分子热运动动能的增加量
容器突然停止,气体的全部定向运动的动能转变为分子热运动的动能。根据动能定理,气体分子热运动的动能等于$\dfrac {1}{2}M{v}^{2}$,其中M为气体质量,v为容器的速率。因此,气体分子热运动动能的增加量为$\Delta K=\dfrac {1}{2}M{v}^{2}$。
步骤 2:计算温度的增加量
根据理想气体状态方程,$Id{I}_{2}=\Delta d$,可知在容器密闭的情况下,气体的压强和体积一不变,温度T与气体分子运动的平均动能成正比关系。因此,温度的增加量可表示为$\Delta T=\dfrac {\Delta {F}_{1}}{{k}_{B}}$,其中HV为气体分子平均动能的增加量,为玻尔兹曼常量。代入公式可得:$\Delta T=\dfrac {\Delta K}{KB}=\dfrac {\dfrac {1}{2}M{v}^{2}}{\dfrac {3}{2}kB}=\dfrac {M{v}^{2}}{3kB}$。
步骤 3:计算气体分子的平均平动动能和转动动能的增加量
根据动能定理,气体分子的平均平动动能和转动动能各增加$\dfrac {1}{2}M{v}^{2}$。根据热力学理论,单原子分子气体只有平动动能,因此只会增加平动动能,平动动能的增加量为$\Delta {K}_{p}=\dfrac {1}{2}M{v}^{2}$。而对于多原子分子气体,分子既有平动动能,又有转动动能,因此平动动能和转动动能的增加量均为$\Delta {K}_{p}=\Delta {K}_{p}=\dfrac {1}{2}M{v}^{2}$。根据摩尔热容的定义,气体单位摩尔质量温度升高1K时吸收的热量为摩尔热容,因此气体摩尔热容${C}_{m}=\dfrac {\Delta Q}{n\Delta T}$,其中△G为气体吸收的热量,为气体摩尔数,△T为气体温度升高的量。根据热力学第一定律,气体吸收的热量等于气体内部分子热运动的增加动能,因此$\Delta Q=\Delta K$。代入公式可得:气体平动动能和转动动能的增加量均为$\Delta {K}_{p}=\Delta {K}_{p}=\dfrac {1}{2}M{v}^{2}$。
容器突然停止,气体的全部定向运动的动能转变为分子热运动的动能。根据动能定理,气体分子热运动的动能等于$\dfrac {1}{2}M{v}^{2}$,其中M为气体质量,v为容器的速率。因此,气体分子热运动动能的增加量为$\Delta K=\dfrac {1}{2}M{v}^{2}$。
步骤 2:计算温度的增加量
根据理想气体状态方程,$Id{I}_{2}=\Delta d$,可知在容器密闭的情况下,气体的压强和体积一不变,温度T与气体分子运动的平均动能成正比关系。因此,温度的增加量可表示为$\Delta T=\dfrac {\Delta {F}_{1}}{{k}_{B}}$,其中HV为气体分子平均动能的增加量,为玻尔兹曼常量。代入公式可得:$\Delta T=\dfrac {\Delta K}{KB}=\dfrac {\dfrac {1}{2}M{v}^{2}}{\dfrac {3}{2}kB}=\dfrac {M{v}^{2}}{3kB}$。
步骤 3:计算气体分子的平均平动动能和转动动能的增加量
根据动能定理,气体分子的平均平动动能和转动动能各增加$\dfrac {1}{2}M{v}^{2}$。根据热力学理论,单原子分子气体只有平动动能,因此只会增加平动动能,平动动能的增加量为$\Delta {K}_{p}=\dfrac {1}{2}M{v}^{2}$。而对于多原子分子气体,分子既有平动动能,又有转动动能,因此平动动能和转动动能的增加量均为$\Delta {K}_{p}=\Delta {K}_{p}=\dfrac {1}{2}M{v}^{2}$。根据摩尔热容的定义,气体单位摩尔质量温度升高1K时吸收的热量为摩尔热容,因此气体摩尔热容${C}_{m}=\dfrac {\Delta Q}{n\Delta T}$,其中△G为气体吸收的热量,为气体摩尔数,△T为气体温度升高的量。根据热力学第一定律,气体吸收的热量等于气体内部分子热运动的增加动能,因此$\Delta Q=\Delta K$。代入公式可得:气体平动动能和转动动能的增加量均为$\Delta {K}_{p}=\Delta {K}_{p}=\dfrac {1}{2}M{v}^{2}$。