一定量的实际气体(其状态方程已知)经历等温膨胀过程,压力从pl变为p2,若要计算该过的△S,需用到的麦克斯韦关系式是
一定量的实际气体(其状态方程已知)经历等温膨胀过程,压力从pl变为p2,若要计算该过
的△S,需用到的麦克斯韦关系式是
题目解答
答案
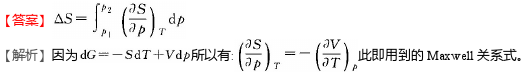
解析
考查要点:本题主要考查麦克斯韦关系式在计算熵变中的应用,以及如何根据热力学过程选择合适的热力学函数关系式。
解题核心思路:
在等温过程中,温度保持不变,因此需要找到熵$S$与压力$P$之间的关系。通过吉布斯自由能$dG$的全微分表达式,结合麦克斯韦关系式,可以推导出$\left(\dfrac{\partial S}{\partial P}\right)_T = -\left(\dfrac{\partial V}{\partial T}\right)_P$,这是计算等温过程中熵变的关键。
破题关键点:
- 明确等温过程的约束条件($dT=0$)。
- 选择与$S$和$P$相关的麦克斯韦关系式,将熵变的计算转化为对体积$V$和温度$T$的偏导数积分。
步骤1:写出吉布斯自由能的全微分表达式
吉布斯自由能$G$的全微分为:
$dG = -S dT + V dP$
步骤2:应用麦克斯韦关系式
根据全微分的对称性,可得:
$\left(\dfrac{\partial S}{\partial P}\right)_T = -\left(\dfrac{\partial V}{\partial T}\right)_P$
此式即为所需的麦克斯韦关系式。
步骤3:计算熵变$\Delta S$
在等温过程中($dT=0$),熵变为:
$\Delta S = \int_{P_1}^{P_2} \left(\dfrac{\partial S}{\partial P}\right)_T dP = -\int_{P_1}^{P_2} \left(\dfrac{\partial V}{\partial T}\right)_P dP$
通过实际气体的状态方程,可进一步计算$\left(\dfrac{\partial V}{\partial T}\right)_P$的具体表达式。