题目
.3-11 图 3-11 所示的两室,由活塞隔开。开始时两室的体积均为0.1 m^3,分别储有空-|||-气和H2,压力各为 .9807times (10)^5Pa ,温度各为15℃,若对空气侧壁加热,直到两室内气体压-|||-力升高到 https:/img.zuoyebang.cc/zyb_e9c0dcd7850c62ec1aa6b1edead39511.jpg.9614times (10)^5Pa 为止,求空气终温及外界加入-|||-的Q,已知 _(v)a=715.94J/(kgcdot k) ,_({H)_(2)}=1.41 ,活塞不导-|||-热,且与气缸间无摩擦。-|||-uum-|||-Q 氢气-|||-空气-|||-7 TITTIL-|||-绝热壁-|||-图 3-11 习题 3-11 图
题目解答
答案
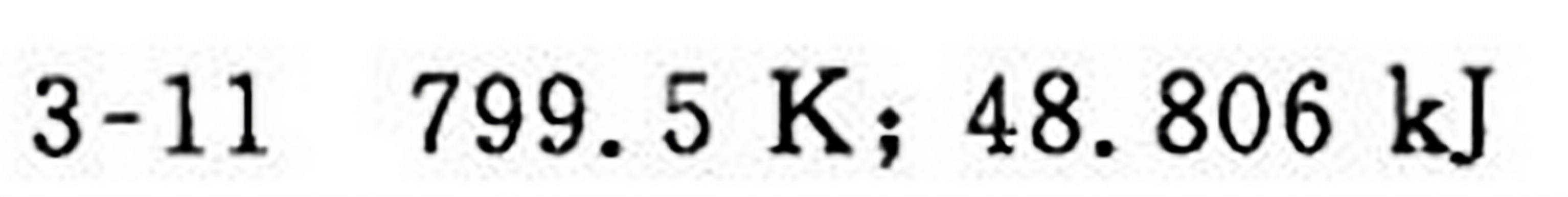
解析
步骤 1:确定初始状态和最终状态
初始状态:空气和氢气的初始压力 $P_1 = 0.9807 \times 10^5 Pa$,初始温度 $T_1 = 15^\circ C = 288.15 K$,初始体积 $V_1 = 0.1 m^3$。
最终状态:空气和氢气的最终压力 $P_2 = 1.9614 \times 10^5 Pa$,最终体积 $V_2$ 需要计算,最终温度 $T_2$ 需要计算。
步骤 2:计算氢气的最终体积
由于氢气室是绝热的,且活塞无摩擦,氢气室的体积变化遵循绝热过程方程 $P_1 V_1^{k} = P_2 V_2^{k}$,其中 $k = 1.41$。
$$
V_2 = V_1 \left(\frac{P_1}{P_2}\right)^{\frac{1}{k}} = 0.1 \times \left(\frac{0.9807 \times 10^5}{1.9614 \times 10^5}\right)^{\frac{1}{1.41}} = 0.0707 m^3
$$
步骤 3:计算空气的最终体积
由于活塞无摩擦,空气室的体积变化与氢气室的体积变化相同,即 $V_2 = 0.0707 m^3$。
步骤 4:计算空气的最终温度
空气室的体积变化遵循理想气体状态方程 $P_1 V_1 / T_1 = P_2 V_2 / T_2$。
$$
T_2 = T_1 \times \frac{P_2 V_2}{P_1 V_1} = 288.15 \times \frac{1.9614 \times 10^5 \times 0.0707}{0.9807 \times 10^5 \times 0.1} = 799.5 K
$$
步骤 5:计算外界加入的热量
外界加入的热量 $Q$ 可以通过计算空气的内能变化来确定,即 $Q = m C_v \Delta T$,其中 $m$ 是空气的质量,$C_v$ 是空气的定容比热容,$\Delta T$ 是温度变化。
首先,计算空气的质量 $m$,使用理想气体状态方程 $PV = m R T$,其中 $R$ 是气体常数,对于空气 $R = 287 J/(kg\cdot K)$。
$$
m = \frac{P_1 V_1}{R T_1} = \frac{0.9807 \times 10^5 \times 0.1}{287 \times 288.15} = 0.119 kg
$$
然后,计算热量 $Q$。
$$
Q = m C_v \Delta T = 0.119 \times 715.94 \times (799.5 - 288.15) = 48.806 kJ
$$
初始状态:空气和氢气的初始压力 $P_1 = 0.9807 \times 10^5 Pa$,初始温度 $T_1 = 15^\circ C = 288.15 K$,初始体积 $V_1 = 0.1 m^3$。
最终状态:空气和氢气的最终压力 $P_2 = 1.9614 \times 10^5 Pa$,最终体积 $V_2$ 需要计算,最终温度 $T_2$ 需要计算。
步骤 2:计算氢气的最终体积
由于氢气室是绝热的,且活塞无摩擦,氢气室的体积变化遵循绝热过程方程 $P_1 V_1^{k} = P_2 V_2^{k}$,其中 $k = 1.41$。
$$
V_2 = V_1 \left(\frac{P_1}{P_2}\right)^{\frac{1}{k}} = 0.1 \times \left(\frac{0.9807 \times 10^5}{1.9614 \times 10^5}\right)^{\frac{1}{1.41}} = 0.0707 m^3
$$
步骤 3:计算空气的最终体积
由于活塞无摩擦,空气室的体积变化与氢气室的体积变化相同,即 $V_2 = 0.0707 m^3$。
步骤 4:计算空气的最终温度
空气室的体积变化遵循理想气体状态方程 $P_1 V_1 / T_1 = P_2 V_2 / T_2$。
$$
T_2 = T_1 \times \frac{P_2 V_2}{P_1 V_1} = 288.15 \times \frac{1.9614 \times 10^5 \times 0.0707}{0.9807 \times 10^5 \times 0.1} = 799.5 K
$$
步骤 5:计算外界加入的热量
外界加入的热量 $Q$ 可以通过计算空气的内能变化来确定,即 $Q = m C_v \Delta T$,其中 $m$ 是空气的质量,$C_v$ 是空气的定容比热容,$\Delta T$ 是温度变化。
首先,计算空气的质量 $m$,使用理想气体状态方程 $PV = m R T$,其中 $R$ 是气体常数,对于空气 $R = 287 J/(kg\cdot K)$。
$$
m = \frac{P_1 V_1}{R T_1} = \frac{0.9807 \times 10^5 \times 0.1}{287 \times 288.15} = 0.119 kg
$$
然后,计算热量 $Q$。
$$
Q = m C_v \Delta T = 0.119 \times 715.94 \times (799.5 - 288.15) = 48.806 kJ
$$