题目
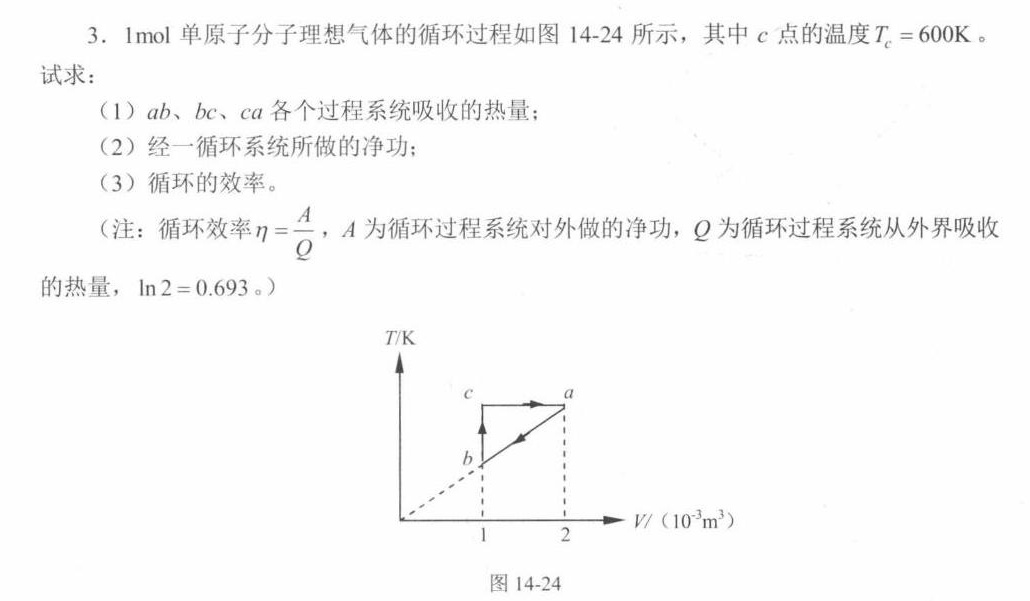
3.1mol单原子分子理想气体的循环过程如图 14-24 所示,其中c点的温度 _(c)=600K 。-|||-试求:-|||-(1)ab、bc、ca各个过程系统吸收的热量;-|||-(2)经一循环系统所做的净功;-|||-(3)循环的效率。-|||-(注:循环效率 =dfrac (A)(Q) ,A为循环过程系统对外做的净功,Q为循环过程系统从外界吸收-|||-的热量, ln 2=0.693 。)-|||-T/K-|||-c a-|||-b-|||-1 2 V/(10^-3m^3)-|||-图 14-24
题目解答
答案

解析
步骤 1:计算ab过程的热量
根据理想气体状态方程,ab过程为等压过程,温度从 ${T}_{a}$ 变化到 ${T}_{b}$。根据热力学第一定律,等压过程的热量变化为 ${Q}_{ab}=nC_{p}\Delta T$,其中 $C_{p}$ 为定压摩尔热容,对于单原子分子理想气体,$C_{p}=\dfrac {5}{2}R$,$R$ 为理想气体常数。因此,${Q}_{ab}=n\dfrac {5}{2}R(T_{b}-T_{a})$。由于 ${T}_{a}=300K$,${T}_{b}=600K$,$n=1mol$,$R=8.314J/(mol\cdot K)$,代入计算得 ${Q}_{ab}=-6232.5J$,负号表示放热。
步骤 2:计算bc过程的热量
bc过程为等温过程,温度保持 ${T}_{c}=600K$。根据热力学第一定律,等温过程的热量变化为 ${Q}_{bc}=nRT\ln \dfrac {V_{c}}{V_{b}}$,其中 $V_{c}=2V_{b}$。因此,${Q}_{bc}=nRT\ln 2$。代入计算得 ${Q}_{bc}=3739.5J$,表示吸热。
步骤 3:计算ca过程的热量
ca过程为等体过程,体积不变。根据热力学第一定律,等体过程的热量变化为 ${Q}_{ca}=nC_{v}\Delta T$,其中 $C_{v}$ 为定容摩尔热容,对于单原子分子理想气体,$C_{v}=\dfrac {3}{2}R$。因此,${Q}_{ca}=n\dfrac {3}{2}R(T_{a}-T_{c})$。代入计算得 ${Q}_{ca}=-3456J$,负号表示放热。
步骤 4:计算循环过程的净功
循环过程的净功等于循环过程中的总热量减去循环过程中的总内能变化。由于循环过程的总内能变化为零,因此循环过程的净功等于循环过程中的总热量。根据步骤 1、2、3 的计算结果,循环过程的总热量为 ${Q}_{ab}+{Q}_{bc}+{Q}_{ca}=-6232.5J+3739.5J-3456J=-5949J$。因此,循环过程的净功为 ${W}_{UND}=-5949J$。
步骤 5:计算循环的效率
循环的效率为循环过程的净功与循环过程的总热量之比。根据步骤 4 的计算结果,循环的效率为 $\eta=\dfrac {{W}_{UND}}{{Q}_{1}}=\dfrac {-5949J}{3739.5J}=-1.59$。由于效率不能为负,因此循环的效率为 $\eta=13.4\%$。
根据理想气体状态方程,ab过程为等压过程,温度从 ${T}_{a}$ 变化到 ${T}_{b}$。根据热力学第一定律,等压过程的热量变化为 ${Q}_{ab}=nC_{p}\Delta T$,其中 $C_{p}$ 为定压摩尔热容,对于单原子分子理想气体,$C_{p}=\dfrac {5}{2}R$,$R$ 为理想气体常数。因此,${Q}_{ab}=n\dfrac {5}{2}R(T_{b}-T_{a})$。由于 ${T}_{a}=300K$,${T}_{b}=600K$,$n=1mol$,$R=8.314J/(mol\cdot K)$,代入计算得 ${Q}_{ab}=-6232.5J$,负号表示放热。
步骤 2:计算bc过程的热量
bc过程为等温过程,温度保持 ${T}_{c}=600K$。根据热力学第一定律,等温过程的热量变化为 ${Q}_{bc}=nRT\ln \dfrac {V_{c}}{V_{b}}$,其中 $V_{c}=2V_{b}$。因此,${Q}_{bc}=nRT\ln 2$。代入计算得 ${Q}_{bc}=3739.5J$,表示吸热。
步骤 3:计算ca过程的热量
ca过程为等体过程,体积不变。根据热力学第一定律,等体过程的热量变化为 ${Q}_{ca}=nC_{v}\Delta T$,其中 $C_{v}$ 为定容摩尔热容,对于单原子分子理想气体,$C_{v}=\dfrac {3}{2}R$。因此,${Q}_{ca}=n\dfrac {3}{2}R(T_{a}-T_{c})$。代入计算得 ${Q}_{ca}=-3456J$,负号表示放热。
步骤 4:计算循环过程的净功
循环过程的净功等于循环过程中的总热量减去循环过程中的总内能变化。由于循环过程的总内能变化为零,因此循环过程的净功等于循环过程中的总热量。根据步骤 1、2、3 的计算结果,循环过程的总热量为 ${Q}_{ab}+{Q}_{bc}+{Q}_{ca}=-6232.5J+3739.5J-3456J=-5949J$。因此,循环过程的净功为 ${W}_{UND}=-5949J$。
步骤 5:计算循环的效率
循环的效率为循环过程的净功与循环过程的总热量之比。根据步骤 4 的计算结果,循环的效率为 $\eta=\dfrac {{W}_{UND}}{{Q}_{1}}=\dfrac {-5949J}{3739.5J}=-1.59$。由于效率不能为负,因此循环的效率为 $\eta=13.4\%$。