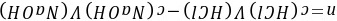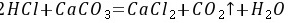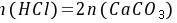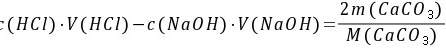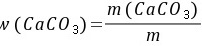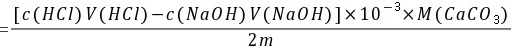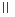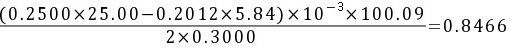第5章 分析化学概述5-1.某试样中铁的质量分数四次平行测定结果为 25.61%,25.53%,25.54%和25.82%,用Q检验法判断是否有可疑值应舍弃(置信度90%)。
第5章 分析化学概述
5-1.某试样中铁的质量分数四次平行测定结果为 25.61%,25.53%,25.54%和25.82%,用Q检验法判断是否有可疑值应舍弃(置信度90%)。
题目解答
答案
解: 将分析结果从小到大排序25.53% 25.54% 25.61% 25.82%
Q计=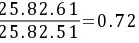
查表5-3,当p=90%, n=4时 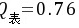
 25.82%应保留
25.82%应保留
5-2.测定某溶液物质的量浓度,得到如下数据(mol.L-1):0.2041,0.2049, 0.2039, 0.2046 ,0.2043, 0.2040计算平均值、平均偏差、相对平均偏差和标准偏差。
解: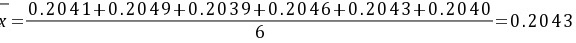
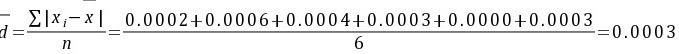
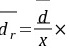 100%
100%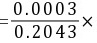 100%
100%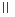 0.1%
0.1%
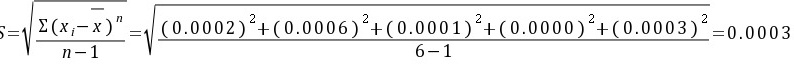
5-3.计算0.001135mo·L-1 HCl溶液对CaCO3的滴定度。
解: CaCO3 + 2HCl = CaCl2 + CO2↑+ H2O
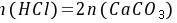
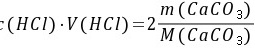
当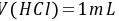 时
时
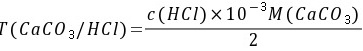
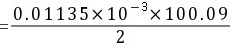
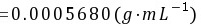
5-4.已知浓硫酸的相对密度为1.84,其中H2SO4含量约为96%。如欲配制1L 0.20mo·L-1 H2SO4溶液,应取这种浓硫酸多少毫升?
解: 设应取浓H2SO4 x mL
该浓硫酸溶液物质的量浓度为:
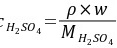

5-5.取无水Na2CO3 2.6500g,溶解后定量转移到 500mL 容量瓶中定容,计算Na2CO3的物质的量浓度。
解: 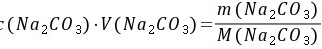
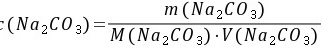
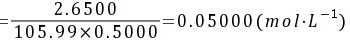
5-6. 0.02500gNa2C2O4溶解后,在酸性溶液中需要35.50mL KMnO4滴定至终点,求KMnO4的物质的量浓度。若用此KMnO4溶液滴定Fe2+,求KMnO4溶液对Fe2+的滴定度。
解: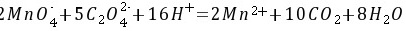
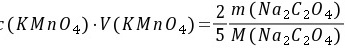
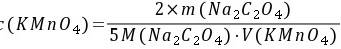
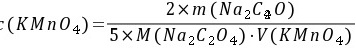
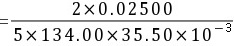
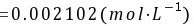
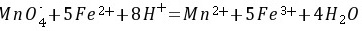
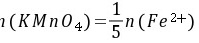
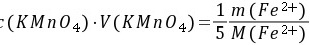
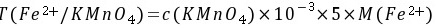
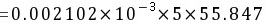
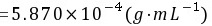
5-7.滴定 0.1560g草酸试样用去 0.1011 mol·L-1 NaOH 22.60mL。求试样中 H2C2O4·2H2O 的质量分数。
解: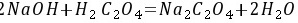
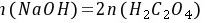
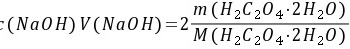
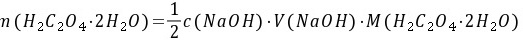
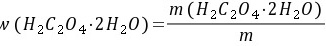
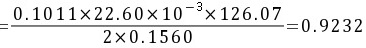
M(NaOH)= 40g·mol-1 M(NaCl)= 58.5g·mol-1 M(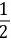 CaCl2)= 55.5g·mol-1
CaCl2)= 55.5g·mol-1
所以,它们的物质的量浓度分别为:
c(NaOH) =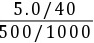 = 0.25 (mol·L-1)
= 0.25 (mol·L-1)
c(NaCl) =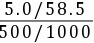 = 0.17 (mo·L-1)
= 0.17 (mo·L-1)
c(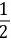 CaCl2)=
CaCl2)=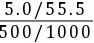 = 0.18 (mol·L-1)
= 0.18 (mol·L-1)
1-4.盐酸含HCl 37.0%(质量分数),密度为1.19g·mL-1。计算:
(1)盐酸的物质的量浓度。
(2)盐酸的质量摩尔浓度。
(3)HCl和H2O的物质的量分数。
解:(1)盐酸的分子量为36.5
c(HCl) = 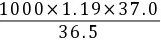 = 12.06 mol·L-1
= 12.06 mol·L-1
(2)b(HCl) =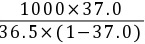 = 16.09 mol·kg-1
= 16.09 mol·kg-1
(3)x2 = 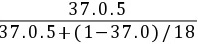 =0.225;
=0.225;
x1 = 1-x2 = 0.775
1-5.计算0.10mol·L-1K3[Fe(CN)6]溶液的离子强度。
解:I=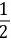 (0.30×12+0.10×32)=0.6
(0.30×12+0.10×32)=0.6
1-6.应用德拜-休克尔极限公式计算0.10mol·L-1KCl溶液中的离子平均活度系数。
解:KCl I=0.1
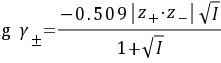 =
=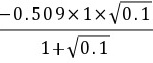 =-0.12
=-0.12
γ±=0.76
5-8.分析不纯CaCO3(其中不含干扰物质)时,称取试样 0.3000g,加入浓度为 0.2500 mol·L-1的 HCl标准溶液 25.00mL。煮沸除去CO2,用浓度为 0.2012 mol·L-1的NaOH溶液返滴过量盐酸,消耗了5.84mL。计算试样中CaCO3的质量分数。
解:与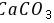 作用后剩余的HCl物质的量
作用后剩余的HCl物质的量