设有一定量的某种理想气体,其状态参量满足方程rho (V)^2= 常量。问:(1) rho (V)^2= 常量、rho (V)^2= 常量 之间的关系如何?(2) 该气体膨胀时,温度是升高还是降低?
设有一定量的某种理想气体,其状态参量满足方程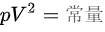 。问:
。问:
(1) 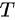 、
、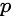 之间的关系如何?
之间的关系如何?
(2) 该气体膨胀时,温度是升高还是降低?
题目解答
答案
(1) 根据理想气体状态方程 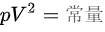 ,可以将其变形为
,可以将其变形为 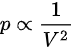 。这说明压强
。这说明压强 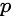 与体积
与体积 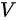 的平方成反比,即当体积增大时,压强会减小;当体积减小时,压强会增大。而根据理想气体状态方程
的平方成反比,即当体积增大时,压强会减小;当体积减小时,压强会增大。而根据理想气体状态方程 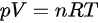 ,其中
,其中 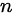 为物质的摩尔数,
为物质的摩尔数,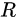 为气体常数,
为气体常数,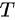 为温度,可以得知温度
为温度,可以得知温度 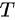 和压强
和压强 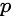 成正比关系,即当压强增大时,温度也会增大;当压强减小时,温度也会减小。
成正比关系,即当压强增大时,温度也会增大;当压强减小时,温度也会减小。
(2) 由于 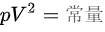 ,当气体膨胀时,体积
,当气体膨胀时,体积 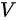 增大,根据
增大,根据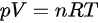 的关系,如果
的关系,如果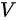 增大,为了使等式成立,压强
增大,为了使等式成立,压强 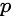 必然会减小。根据前面的推导,当压强减小时,温度也会减小。因此,在该气体膨胀时,温度会降低。
必然会减小。根据前面的推导,当压强减小时,温度也会减小。因此,在该气体膨胀时,温度会降低。
综上所述:
(1) 温度 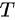 和压强
和压强 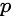 成正比关系。
成正比关系。
(2) 该气体膨胀时,温度会降低。
解析
本题考查理想气体状态方程的应用及气体参量之间的关系推导。核心思路是将题目给出的方程与理想气体状态方程结合,推导出温度与压强、体积的关系。关键点在于正确联立方程,分析变量间的依赖关系,并判断气体膨胀时温度的变化趋势。
第(1)题
-
联立方程
已知 $\rho V^2 = \text{常量}$(假设 $\rho$ 为压强 $p$),即 $p = \frac{\text{常量}}{V^2}$。
结合理想气体状态方程 $pV = nRT$,将 $p = \frac{\text{常量}}{V^2}$ 代入得:
$\frac{\text{常量}}{V^2} \cdot V = nRT \implies \frac{\text{常量}}{V} = nRT \implies T = \frac{\text{常量}}{nR V}.$
这表明 温度 $T$ 与体积 $V$ 成反比。 -
推导 $T$ 与 $p$ 的关系
由 $p = \frac{\text{常量}}{V^2}$ 得 $V = \sqrt{\frac{\text{常量}}{p}}$,代入 $T = \frac{\text{常量}}{nR V}$:
$T = \frac{\text{常量}}{nR} \cdot \sqrt{\frac{p}{\text{常量}}} \implies T \propto \sqrt{p}.$
因此,温度 $T$ 与压强 $p$ 的平方根成正比。
第(2)题
- 分析膨胀过程
当气体膨胀时,体积 $V$ 增大。根据 $\rho V^2 = \text{常量}$,$V$ 增大导致压强 $p$ 减小。
由 $T \propto \sqrt{p}$ 可知,压强 $p$ 减小会导致温度 $T$ 降低。