题目
A-|||-①-|||-②-|||-B-|||-。 iv如图所示为一定质量的理想气体的压强随体积变化的P-(1)/(V)图象,其中AB段为双曲线,则下列有关说法正确的是 ( ) A. 过程①中气体分子的平均动能不变 B. 过程②中气体分子单位时间内对容器壁的碰撞次数减小 C. 过程②中气体分子的平均动能减小 D. 过程③中气体分子对容器壁的碰撞次数增大 E. 过程③中气体的内能不变
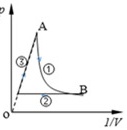 如图所示为一定质量的理想气体的压强随体积变化的P-$\frac{1}{V}$图象,其中AB段为双曲线,则下列有关说法正确的是 ( )
如图所示为一定质量的理想气体的压强随体积变化的P-$\frac{1}{V}$图象,其中AB段为双曲线,则下列有关说法正确的是 ( )- A. 过程①中气体分子的平均动能不变
- B. 过程②中气体分子单位时间内对容器壁的碰撞次数减小
- C. 过程②中气体分子的平均动能减小
- D. 过程③中气体分子对容器壁的碰撞次数增大
- E. 过程③中气体的内能不变
题目解答
答案
BDE
B. 过程②中气体分子单位时间内对容器壁的碰撞次数减小
D. 过程③中气体分子对容器壁的碰撞次数增大
E. 过程③中气体的内能不变
B. 过程②中气体分子单位时间内对容器壁的碰撞次数减小
D. 过程③中气体分子对容器壁的碰撞次数增大
E. 过程③中气体的内能不变
解析
步骤 1:理解P-$\frac{1}{V}$图象的物理意义
根据理想气体状态方程:PV=nRT,可得:P=nRT•$\frac{1}{V}$,故可知,P-$\frac{1}{V}$图象的斜率k=nRT,而对一定质量的理想气体而言,斜率定性的反映温度的高低。
步骤 2:分析过程①
P-$\frac{1}{V}$图象在过程①的每点与坐标原点连线构成的斜率逐渐减小,表示理想气体的温度逐渐降低,可知平均动能减小,故A错误。
步骤 3:分析过程②
P-$\frac{1}{V}$图象过程②的每点与坐标原点连线构成的斜率逐渐逐渐增大,则温度升高,平均动能增大,故C错误。
P-$\frac{1}{V}$图象过程②可读出压强不变,体积增大,根据理想气体状态方程PV=nRT,可以推出温度升高,分子的平均动能$\overline{{E}_{k}}$增大,由理想气体压强的微观意义,气体压强与气体分子单位时间内对容器壁的碰撞次数N、气体分子平均动能$\overline{{E}_{k}}$有关,在压强P不变,$\overline{{E}_{k}}$增大的条件下,可得N减小,故B正确。
步骤 4:分析过程③
过程③可读出压强增大,温度不变,分子的平均动能$\overline{{E}_{k}}$不变,根据理想气体压强的微观意义,气体压强与气体分子单位时间内对容器壁的碰撞次数N、气体分子平均动能$\overline{{E}_{k}}$有关,在压强增大,温度不变的情况下,气体分子对容器壁的碰撞次数N增大,故D正确。
过程③中气体可知理想气体的内能不变,故E正确。
根据理想气体状态方程:PV=nRT,可得:P=nRT•$\frac{1}{V}$,故可知,P-$\frac{1}{V}$图象的斜率k=nRT,而对一定质量的理想气体而言,斜率定性的反映温度的高低。
步骤 2:分析过程①
P-$\frac{1}{V}$图象在过程①的每点与坐标原点连线构成的斜率逐渐减小,表示理想气体的温度逐渐降低,可知平均动能减小,故A错误。
步骤 3:分析过程②
P-$\frac{1}{V}$图象过程②的每点与坐标原点连线构成的斜率逐渐逐渐增大,则温度升高,平均动能增大,故C错误。
P-$\frac{1}{V}$图象过程②可读出压强不变,体积增大,根据理想气体状态方程PV=nRT,可以推出温度升高,分子的平均动能$\overline{{E}_{k}}$增大,由理想气体压强的微观意义,气体压强与气体分子单位时间内对容器壁的碰撞次数N、气体分子平均动能$\overline{{E}_{k}}$有关,在压强P不变,$\overline{{E}_{k}}$增大的条件下,可得N减小,故B正确。
步骤 4:分析过程③
过程③可读出压强增大,温度不变,分子的平均动能$\overline{{E}_{k}}$不变,根据理想气体压强的微观意义,气体压强与气体分子单位时间内对容器壁的碰撞次数N、气体分子平均动能$\overline{{E}_{k}}$有关,在压强增大,温度不变的情况下,气体分子对容器壁的碰撞次数N增大,故D正确。
过程③中气体可知理想气体的内能不变,故E正确。