题目
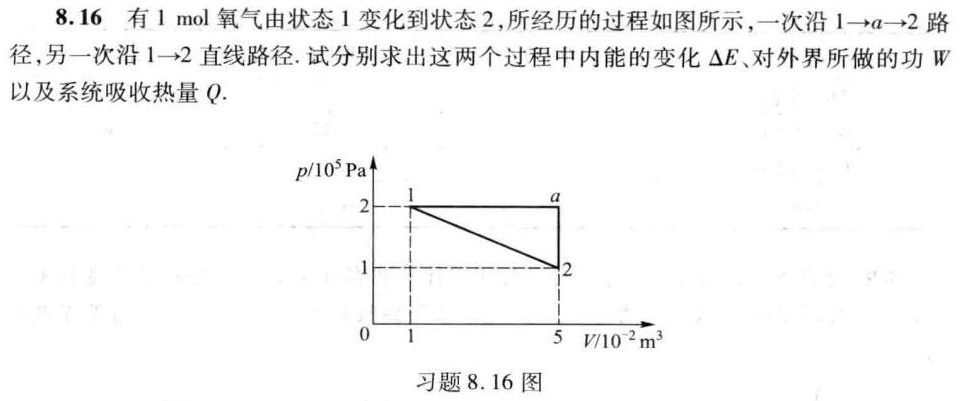
8.16 有1 mol氧气由状态1变化到状态2,所经历的过程如图所示,一次沿1 →a→2路-|||-径,另一次沿 https:/img.zuoyebang.cc/zyb_3b9d0ed4dbf0f93ce25abde836bd2997.jpgarrow 2 直线路径.试分别求出这两个过程中内能的变化 Delta E 对外界所做的功W-|||-以及系统吸收热量Q.-|||-p/10^5Pa-|||-2 1 a-|||-: 1 2-|||-0 1 5 V/10 ^2m^3-|||-习题8.16图
题目解答
答案
解析
步骤 1:确定内能变化 $\Delta E$
内能变化 $\Delta E$ 只与初末状态有关,与过程无关。对于理想气体,内能变化只与温度变化有关,即 $\Delta E = \frac{3}{2}nR\Delta T$,其中 $n$ 为摩尔数,$R$ 为理想气体常数,$\Delta T$ 为温度变化。由于题目中没有给出温度变化,我们可以通过理想气体状态方程 $pV=nRT$ 来计算温度变化。对于1 mol氧气,$n=1$,$R=8.314$ J/(mol·K)。
步骤 2:计算沿1 →a→2路径的功W
对于1 →a→2路径,可以分为两段:1 →a和a→2。1 →a为等容过程,体积不变,所以对外界做的功为0。a→2为等压过程,对外界做的功为 $W = p\Delta V$,其中 $p$ 为等压过程中的压强,$\Delta V$ 为体积变化。
步骤 3:计算沿1 →a→2路径的热量Q
根据热力学第一定律,$Q = \Delta E + W$,其中 $Q$ 为系统吸收的热量,$\Delta E$ 为内能变化,$W$ 为对外界做的功。
步骤 4:计算沿1 →2直线路径的功W
对于1 →2直线路径,对外界做的功为 $W = \frac{1}{2}(p_1 + p_2)\Delta V$,其中 $p_1$ 和 $p_2$ 分别为初末状态的压强,$\Delta V$ 为体积变化。
步骤 5:计算沿1 →2直线路径的热量Q
根据热力学第一定律,$Q = \Delta E + W$,其中 $Q$ 为系统吸收的热量,$\Delta E$ 为内能变化,$W$ 为对外界做的功。
内能变化 $\Delta E$ 只与初末状态有关,与过程无关。对于理想气体,内能变化只与温度变化有关,即 $\Delta E = \frac{3}{2}nR\Delta T$,其中 $n$ 为摩尔数,$R$ 为理想气体常数,$\Delta T$ 为温度变化。由于题目中没有给出温度变化,我们可以通过理想气体状态方程 $pV=nRT$ 来计算温度变化。对于1 mol氧气,$n=1$,$R=8.314$ J/(mol·K)。
步骤 2:计算沿1 →a→2路径的功W
对于1 →a→2路径,可以分为两段:1 →a和a→2。1 →a为等容过程,体积不变,所以对外界做的功为0。a→2为等压过程,对外界做的功为 $W = p\Delta V$,其中 $p$ 为等压过程中的压强,$\Delta V$ 为体积变化。
步骤 3:计算沿1 →a→2路径的热量Q
根据热力学第一定律,$Q = \Delta E + W$,其中 $Q$ 为系统吸收的热量,$\Delta E$ 为内能变化,$W$ 为对外界做的功。
步骤 4:计算沿1 →2直线路径的功W
对于1 →2直线路径,对外界做的功为 $W = \frac{1}{2}(p_1 + p_2)\Delta V$,其中 $p_1$ 和 $p_2$ 分别为初末状态的压强,$\Delta V$ 为体积变化。
步骤 5:计算沿1 →2直线路径的热量Q
根据热力学第一定律,$Q = \Delta E + W$,其中 $Q$ 为系统吸收的热量,$\Delta E$ 为内能变化,$W$ 为对外界做的功。