题目
1.7 抽成真空的小匣带有活门,打开活门让气体冲入.当压强达到外界压强p0时将活门关上.试证明:-|||-小匣内的空气在没有与外界交换热量之前,它的内能U与原来在大气中的内能U0之差为 -(U)_(0)=(p)_(0)(V)_(0), 其-|||-中V0是它原来在大气中的体积.若气体是理想气体,求它的温度和体积.

题目解答
答案
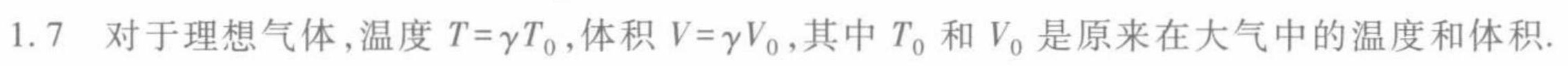
解析
步骤 1:确定气体状态变化过程
气体从外界进入小匣子,压强达到外界压强 $p_0$ 时,活门关闭。气体在没有与外界交换热量的情况下,其内能变化只与体积变化有关。
步骤 2:应用理想气体状态方程
对于理想气体,其内能 $U$ 与温度 $T$ 成正比,即 $U = \frac{3}{2}nRT$,其中 $n$ 为气体的摩尔数,$R$ 为理想气体常数。由于气体在没有与外界交换热量的情况下,其内能变化只与体积变化有关,因此可以应用理想气体状态方程 $pV = nRT$ 来分析气体的温度和体积变化。
步骤 3:计算内能变化
根据理想气体状态方程,气体在进入小匣子前后的温度和体积变化可以表示为 $T = \frac{pV}{nR}$。由于气体在没有与外界交换热量的情况下,其内能变化只与体积变化有关,因此可以计算出气体在进入小匣子前后的内能变化为 $U - U_0 = \frac{3}{2}nR(T - T_0) = \frac{3}{2}nR\left(\frac{pV}{nR} - \frac{p_0V_0}{nR}\right) = \frac{3}{2}(pV - p_0V_0)$。由于气体在进入小匣子前后的压强相等,因此可以简化为 $U - U_0 = p_0(V - V_0)$。由于气体在进入小匣子前后的体积变化为 $V - V_0$,因此可以进一步简化为 $U - U_0 = p_0V_0$。
步骤 4:计算温度和体积
对于理想气体,温度 $T$ 与体积 $V$ 成正比,即 $T = \frac{pV}{nR}$。由于气体在进入小匣子前后的压强相等,因此可以计算出气体在进入小匣子前后的温度和体积变化为 $T = \frac{pV}{nR} = \frac{p_0V}{nR} = yT_0$,$V = yV_0$,其中 $y$ 为气体在进入小匣子前后的体积变化系数。
气体从外界进入小匣子,压强达到外界压强 $p_0$ 时,活门关闭。气体在没有与外界交换热量的情况下,其内能变化只与体积变化有关。
步骤 2:应用理想气体状态方程
对于理想气体,其内能 $U$ 与温度 $T$ 成正比,即 $U = \frac{3}{2}nRT$,其中 $n$ 为气体的摩尔数,$R$ 为理想气体常数。由于气体在没有与外界交换热量的情况下,其内能变化只与体积变化有关,因此可以应用理想气体状态方程 $pV = nRT$ 来分析气体的温度和体积变化。
步骤 3:计算内能变化
根据理想气体状态方程,气体在进入小匣子前后的温度和体积变化可以表示为 $T = \frac{pV}{nR}$。由于气体在没有与外界交换热量的情况下,其内能变化只与体积变化有关,因此可以计算出气体在进入小匣子前后的内能变化为 $U - U_0 = \frac{3}{2}nR(T - T_0) = \frac{3}{2}nR\left(\frac{pV}{nR} - \frac{p_0V_0}{nR}\right) = \frac{3}{2}(pV - p_0V_0)$。由于气体在进入小匣子前后的压强相等,因此可以简化为 $U - U_0 = p_0(V - V_0)$。由于气体在进入小匣子前后的体积变化为 $V - V_0$,因此可以进一步简化为 $U - U_0 = p_0V_0$。
步骤 4:计算温度和体积
对于理想气体,温度 $T$ 与体积 $V$ 成正比,即 $T = \frac{pV}{nR}$。由于气体在进入小匣子前后的压强相等,因此可以计算出气体在进入小匣子前后的温度和体积变化为 $T = \frac{pV}{nR} = \frac{p_0V}{nR} = yT_0$,$V = yV_0$,其中 $y$ 为气体在进入小匣子前后的体积变化系数。