题目
8-10 一气缸内储有10 mol的单原子理想气体,在压缩过程中,外力做-|||-功209J,气体温度升高1K。试计算气体内能增量和所吸收的热量,在此过程-|||-中气体的摩尔热容是多少?

题目解答
答案
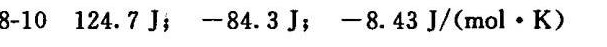
解析
步骤 1:计算气体内能增量
根据理想气体的内能公式,单原子理想气体的内能与温度的关系为 $U = \frac{3}{2}nRT$,其中 $n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度。因此,内能增量 $\Delta U$ 可以表示为 $\Delta U = \frac{3}{2}nR\Delta T$。将题目中给出的数值代入,得到 $\Delta U = \frac{3}{2} \times 10 \times 8.314 \times 1 = 124.71$ J。
步骤 2:计算所吸收的热量
根据热力学第一定律,内能的改变量等于外界对系统做的功加上系统吸收的热量,即 $\Delta U = W + Q$。题目中已知外力做功 $W = 209$ J,内能增量 $\Delta U = 124.71$ J,代入公式得到 $124.71 = 209 + Q$,解得 $Q = -84.29$ J。
步骤 3:计算摩尔热容
摩尔热容 $C$ 定义为单位摩尔物质温度升高1K时所吸收的热量,即 $C = \frac{Q}{n\Delta T}$。将题目中给出的数值代入,得到 $C = \frac{-84.29}{10 \times 1} = -8.429$ J/(mol·K)。
根据理想气体的内能公式,单原子理想气体的内能与温度的关系为 $U = \frac{3}{2}nRT$,其中 $n$ 是摩尔数,$R$ 是理想气体常数,$T$ 是温度。因此,内能增量 $\Delta U$ 可以表示为 $\Delta U = \frac{3}{2}nR\Delta T$。将题目中给出的数值代入,得到 $\Delta U = \frac{3}{2} \times 10 \times 8.314 \times 1 = 124.71$ J。
步骤 2:计算所吸收的热量
根据热力学第一定律,内能的改变量等于外界对系统做的功加上系统吸收的热量,即 $\Delta U = W + Q$。题目中已知外力做功 $W = 209$ J,内能增量 $\Delta U = 124.71$ J,代入公式得到 $124.71 = 209 + Q$,解得 $Q = -84.29$ J。
步骤 3:计算摩尔热容
摩尔热容 $C$ 定义为单位摩尔物质温度升高1K时所吸收的热量,即 $C = \frac{Q}{n\Delta T}$。将题目中给出的数值代入,得到 $C = \frac{-84.29}{10 \times 1} = -8.429$ J/(mol·K)。