(12分)氯气和氯乙烯都是非常重要的化工产品,年产量均在107t左右,氯气的实验室制备和氯乙烯的工业生产都有多种不同方法。完成下列填空:(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要 饱和食盐水 、 烧碱溶液 (填写试剂或溶液名称)(2)实验室用2.00mol/L盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为 100 mL。(3)实验室通常用向上排空气法收集氯气。设计一个简单实验,验证所收集的氯气中是否含有空气。 将集气瓶倒置于有足量烧碱溶液的水槽里,若气体不能充满集气瓶,液面上有无色气体,则有空气,若充满,则无空气工业上用电石﹣乙炔生产氯乙烯的反应如下:CaO+3Csquare square Csim 23square square square CaC2+COCaC2+2H2O→HC≡CH↑+Ca(OH)2HC≡CH+HClsquare square Csim 23square square square CH2═CHCl电石﹣乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源。电石﹣乙炔法的缺点是: 能耗大 、 使用的催化剂毒性大 。(4)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢。设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件)。要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液。[分析](1)实验室制备纯净的氯气,应用饱和氯化钠溶液除去HCl,用氢氧化钠溶液进行尾气吸收;(2)反应的方程式为ClO﹣+Cl﹣+2H+=Cl2↑+H2O,n(Cl2)=square square Csim 23square square square =0.1mol,结合反应的方程式计算;(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;用电石生产乙炔,耗能大,且污染环境;(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2﹣二氯乙烷,1,2﹣二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2﹣二氯乙烷。.
(12分)氯气和氯乙烯都是非常重要的化工产品,年产量均在107t左右,氯气的实验室制备和氯乙烯的工业生产都有多种不同方法。
完成下列填空:
(1)实验室制取纯净的氯气,除了二氧化锰、浓盐酸和浓硫酸,还需要 饱和食盐水 、 烧碱溶液 (填写试剂或溶液名称)
(2)实验室用2.00mol/L盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为 100 mL。
(3)实验室通常用向上排空气法收集氯气。设计一个简单实验,验证所收集的氯气中是否含有空气。 将集气瓶倒置于有足量烧碱溶液的水槽里,若气体不能充满集气瓶,液面上有无色气体,则有空气,若充满,则无空气
工业上用电石﹣乙炔生产氯乙烯的反应如下:
CaO+3C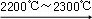 CaC2+CO
CaC2+CO
CaC2+2H2O→HC≡CH↑+Ca(OH)2
HC≡CH+HCl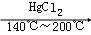 CH2═CHCl
CH2═CHCl
电石﹣乙炔法的优点是流程简单,产品纯度高,而且不依赖于石油资源。
电石﹣乙炔法的缺点是: 能耗大 、 使用的催化剂毒性大 。
(4)乙烷和氯气反应可制得ClCH2CH2Cl,ClCH2CH2Cl加热分解得到氯乙烯和氯化氢。
设计一种以乙烯和氯气为原料制取氯乙烯的方案(其他原料自选),用化学方程式表示(不必注明反应条件)。
要求:①反应产生的氯化氢必须用于氯乙烯的制备;②不再产生其他废液。
[分析](1)实验室制备纯净的氯气,应用饱和氯化钠溶液除去HCl,用氢氧化钠溶液进行尾气吸收;
(2)反应的方程式为ClO﹣+Cl﹣+2H+=Cl2↑+H2O,n(Cl2)=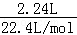 =0.1mol,结合反应的方程式计算;
=0.1mol,结合反应的方程式计算;
(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;用电石生产乙炔,耗能大,且污染环境;
(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2﹣二氯乙烷,1,2﹣二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2﹣二氯乙烷。
.题目解答
答案
[解答]解:(1)实验室用盐酸制备氯气,氯气中混有氯化氢,得到纯净的氯气,应用饱和氯化钠溶液除去HCl,再用浓硫酸干燥,最后用氢氧化钠溶液进行尾气吸收,
故答案为:饱和食盐水;烧碱溶液;
(2)反应的方程式为ClO﹣+Cl﹣+2H+=Cl2↑+H2O,n(Cl2)=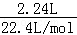 =0.1mol,则需要n(HCl)=0.2mol,
=0.1mol,则需要n(HCl)=0.2mol,
发生反应的盐酸的体积为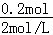 =0.1L=100mL,
=0.1L=100mL,
故答案为:100;
(3)氯气可与氢氧化钠溶液反应,如含有空气,则与氢氧化钠反应后试管内有残留气体;
工业在高温下生产电石,用电石生产乙炔,耗能大,由于乙炔与HCl的反应在氯化汞的作用下进行,污染环境,
故答案为:将集气瓶倒置于有足量烧碱溶液的水槽里,若气体不能充满集气瓶,液面上有无色气体,则有空气,若充满,则无空气;反应温度高,能耗大;使用的催化剂毒性大;
(4)以乙烯和氯气为原料制取氯乙烯,可由乙烯和氯气发生加成反应生成1,2﹣二氯乙烷,1,2﹣二氯乙烷发生消去反应生成氯乙烯,生成的氯化氢电解生成氢气和氯气,氢气和乙烯发生加成反应生成乙烷,乙烷和氯气发生取代反应生成1,2﹣二氯乙烷,涉及反应有CH2=CH2+Cl2→CH2ClCH2Cl CH2ClCH2Cl  CH2=CHCl+HCl;
CH2=CHCl+HCl;
2 HCl H2↑+Cl2↑; CH2=CH2+H2
H2↑+Cl2↑; CH2=CH2+H2 CH3CH3;CH3CH3+Cl2→CH2ClCH2Cl,
CH3CH3;CH3CH3+Cl2→CH2ClCH2Cl,
故答案为:CH2=CH2+Cl2→CH2ClCH2Cl CH2ClCH2Cl  CH2=CHCl+HCl;2 HCl
CH2=CHCl+HCl;2 HCl H2↑+Cl2↑; CH2=CH2+H2
H2↑+Cl2↑; CH2=CH2+H2 CH3CH3;CH3CH3+Cl2→CH2ClCH2Cl。
CH3CH3;CH3CH3+Cl2→CH2ClCH2Cl。
.