化工热力学课后答案朱自强2-1 试分别用下述方法求出400℃、4.053MPa下甲烷气体的摩尔体积。(1) 理想气体方程;(2) RK方程;(3)PR方程;(4) 维里截断式(2-7)。其中B用Pitzer的普遍化关联法运算。[解] (1) 按照理想气体状态方程,可求出甲烷气体在理想情形下的摩尔体积为(2) 用RK方程求摩尔体积将RK方程稍加变形,可写为 (E1)其中从附表1查得甲烷的临界温度和压力分别为=190.6K, =4.60MPa,将它们代入a, b表达式得以理想气体状态方程求得的为初值,代入式(E1)中迭代求解,第一次迭代得到值为第二次迭代得为和差不多相差专门小,可终止迭代。故用RK方程求得的摩尔体积近似为(3)用PR方程求摩尔体积将PR方程稍加变形,可写为 (E2)式中 从附表1查得甲烷的=0.008。将与代入上式用、和求a和b,以RK方程求得的V值代入式(E2),同时将a和b的值也代入该式的右边,藉此求式(E2)左边的V值,得 再按上法迭代一次,V值仍为,故最后求得甲烷的摩尔体积近似为。(4)维里截断式求摩尔体积按照维里截断式(2-7) (E3) (E4) (E5) (E6)其中已知甲烷的偏心因子=0.008,故由式(E4)~(E6)可运算得到从式(E3)可得因,故四种方法运算得到的甲烷气体的摩尔体积分别为、、和。其中后三种方法求得的甲烷的摩尔体积差不多相等,且与第一种方法求得的值差异也小,这是由于该物系比较接近理想气体的缘故。2-2 含有丙烷的0.5的容器具有2.7Mpa的耐压极限。出于安全考虑,规定充进容器的丙烷为127℃,压力不得超过耐压极限的一半。试咨询可充入容器的丙烷为多少千克?[解] 从附表1查得丙烷的、和,分别为4.25MPa,369.8K和0.152。则[解] (1) 理想气体方程法按照理想气体方程求得混合物的摩尔体积为(2) Amagat定律和普遍化压缩因子图法按照Amagat定律 (E1)从附表1查得和的和,(1): =,=(2): =,=按照、值,求出(1)和(2)的和为(1): , (2):, 从普遍化二参数压缩因子图查得相应的值: ; :代入式(E1)得(3) 虚拟临界常数法(Kay规则)法按照Kay规则运算混合物虚拟临界常数,故可求出混合物的对比温度和对比压力,, 按照和,查二参数普遍化压缩因子图(2-4),得,故(4)混合物的第二维里系数法按照式(2-71)(2-72e), (E2) (E3) (E4) (E5) (E6) (E7) (E8)和用Pitzer的普遍化关联法运算,即 (E9) (E10)其中 , (E11)纯组分的第二维里系数,可按通常的方法求出,即只须用式(E3)、式(E9)和式(E10),所以现在i=j。而对交叉第二维里系数,须从式(E3)式(E11)求出。先从附表1查得各组分的、、、和,具体数值见后面的表1,具体的运算步骤如下:对(1),按照式(E11),, 按照式(E9)和(E10),, 代入式(E3),得对(2),按照式(E11),, 按照式(E9)和(E10),, 代入式(E3),得交叉第二维里系数的运算如下:按照式(E4)式(E8),按照式(E11),代入式(E9)和(E10),, 代入式(E3)得将上述运算结果综合成表1。表1、维里方程运算混合气体的摩尔体积时的一些中间参数注:方框中的数值系从附表1查得,其余的分别按照式(E3)式(E11)求得。按照式(E2)求出,得按照维里截断式(2-7),求出混合物的压缩因子为若压缩因子为“负值”,意味着摩尔体积为负值。这是没有任何物理意义的,也是不合理的。讲明方法(4)在高达60.67Mpa的压力下是不适合的。将四种方法运算结果综合成表2。由表可知,(2)、(3)两种方法求出的结果和实验值专门接近,而方法(1)也即理想气体方程求得的结果偏差专门大,这是由于系统非理想的缘故。比较(2)、(3)两种方法,能够看出(2)法,也即Amagat定律,求出的结果为最优。表2、由4种方法运算混合气体的压缩因子和摩尔体积2-12 以化学计量比的和合成氨,在25℃和30.395Mpa下,混合气以的流速进入反应器。氨的转化率为15%。从反应器出来的气体经冷却和凝缩,将氨分离出后,再行循环。(1)运算每小时合成氨的量;(2)若反应器出口的条件为27.86Mpa,150℃,求内径为的出口管中气体的流速。[解] 先求出(1)+(2)混合气体的摩尔体积,拟用Amagat定律求解。由附表1分别查得和的、为:, :, 然后求和的、,: , : , 按照、查二参数普遍化Z图得, 因为和是以化学计量比输入,故, 按照Amagat定律故 已知混合气体的进口体积流量,,则混合气体的进口摩尔流速为按照反应的计量关系, (总量)开始 1 3 0 4终止 1-0.15 3.7则每小时合成氨的量可由下式运算得出,(2) 先求出口气体的组成。因为出口气体中,故,,,再求出口气体的摩尔流速利用Amagat定律求出口气体的摩尔体积。先从附表查得的,,则可求出各组分的对比性质为: , : , : , 按照上述对比参数,查二参数普遍化Z图,得,,则 故 出口管中气体的体积流速为出口管中气体的流速,,可按下式运算,式中:A为管子的截面积。运算得出出口管中混合气体的流速为。58页第2章2-1 求温度673.15K、压力4.053MPa的甲烷气体摩尔体积。
化工热力学课后答案朱自强
2-1 试分别用下述方法求出400℃、4.053MPa下甲烷气体的摩尔体积。(1) 理想气体方程;(2) RK方程;(3)PR方程;(4) 维里截断式(2-7)。其中B用Pitzer的普遍化关联法运算。
[解] (1) 按照理想气体状态方程,可求出甲烷气体在理想情形下的摩尔体积为
(2) 用RK方程求摩尔体积
将RK方程稍加变形,可写为
(E1)
其中
从附表1查得甲烷的临界温度和压力分别为=190.6K, =4.60MPa,将它们代入a, b表达式得
以理想气体状态方程求得的为初值,代入式(E1)中迭代求解,第一次迭代得到值为
第二次迭代得为
和差不多相差专门小,可终止迭代。故用RK方程求得的摩尔体积近似为
(3)用PR方程求摩尔体积
将PR方程稍加变形,可写为
(E2)
式中
从附表1查得甲烷的=0.008。
将与代入上式
用、和求a和b,
以RK方程求得的V值代入式(E2),同时将a和b的值也代入该式的右边,藉此求式(E2)左边的V值,得
再按上法迭代一次,V值仍为,故最后求得甲烷的摩尔体积近似为。
(4)维里截断式求摩尔体积
按照维里截断式(2-7)
(E3)
(E4)
(E5)
(E6)
其中
已知甲烷的偏心因子=0.008,故由式(E4)~(E6)可运算得到
从式(E3)可得
因,故
四种方法运算得到的甲烷气体的摩尔体积分别为、、和。其中后三种方法求得的甲烷的摩尔体积差不多相等,且与第一种方法求得的值差异也小,这是由于该物系比较接近理想气体的缘故。
2-2 含有丙烷的0.5的容器具有2.7Mpa的耐压极限。出于安全考虑,规定充进容器的丙烷为127℃,压力不得超过耐压极限的一半。试咨询可充入容器的丙烷为多少千克?
[解] 从附表1查得丙烷的、和,分别为4.25MPa,369.8K和0.152。则
[解] (1) 理想气体方程法
按照理想气体方程求得混合物的摩尔体积为
(2) Amagat定律和普遍化压缩因子图法
按照Amagat定律
(E1)
从附表1查得和的和,
(1): =,=
(2): =,=
按照、值,求出(1)和(2)的和为
(1): ,
(2):,
从普遍化二参数压缩因子图查得相应的值
: ; :
代入式(E1)得
(3) 虚拟临界常数法(Kay规则)法
按照Kay规则运算混合物虚拟临界常数,
故可求出混合物的对比温度和对比压力,
,
按照和,查二参数普遍化压缩因子图(2-4),得,故
(4)混合物的第二维里系数法
按照式(2-71)(2-72e),
(E2)
(E3)
(E4)
(E5)
(E6)
(E7)
(E8)
和用Pitzer的普遍化关联法运算,即
(E9)
(E10)
其中 , (E11)
纯组分的第二维里系数,可按通常的方法求出,即只须用式(E3)、式(E9)和式(E10),所以现在i=j。而对交叉第二维里系数,须从式(E3)式(E11)求出。
先从附表1查得各组分的、、、和,具体数值见后面的表1,具体的运算步骤如下:
对(1),按照式(E11),
,
按照式(E9)和(E10),
,
代入式(E3),得
对(2),按照式(E11),
,
按照式(E9)和(E10),
,
代入式(E3),得
交叉第二维里系数的运算如下:
按照式(E4)式(E8),
按照式(E11),
代入式(E9)和(E10),
,
代入式(E3)得
将上述运算结果综合成表1。
表1、维里方程运算混合气体的摩尔体积时的一些中间参数
注:方框中的数值系从附表1查得,其余的分别按照式(E3)式(E11)求得。
按照式(E2)求出,得
按照维里截断式(2-7),求出混合物的压缩因子为
若压缩因子为“负值”,意味着摩尔体积为负值。这是没有任何物理意义的,也是不合理的。讲明方法(4)在高达60.67Mpa的压力下是不适合的。
将四种方法运算结果综合成表2。由表可知,(2)、(3)两种方法求出的结果和实验值专门接近,而方法(1)也即理想气体方程求得的结果偏差专门大,这是由于系统非理想的缘故。比较(2)、(3)两种方法,能够看出(2)法,也即Amagat定律,求出的结果为最优。
表2、由4种方法运算混合气体的压缩因子和摩尔体积
2-12 以化学计量比的和合成氨,在25℃和30.395Mpa下,混合气以的流速进入反应器。氨的转化率为15%。从反应器出来的气体经冷却和凝缩,将氨分离出后,再行循环。(1)运算每小时合成氨的量;(2)若反应器出口的条件为27.86Mpa,150℃,求内径为的出口管中气体的流速。
[解] 先求出(1)+(2)混合气体的摩尔体积,拟用Amagat定律求解。
由附表1分别查得和的、为
:,
:,
然后求和的、,
: ,
: ,
按照、查二参数普遍化Z图得
,
因为和是以化学计量比输入,故
,
按照Amagat定律
故
已知混合气体的进口体积流量,,则混合气体的进口摩尔流速为
按照反应的计量关系,
(总量)
开始 1 3 0 4
终止 1-0.15 3.7
则每小时合成氨的量可由下式运算得出,
(2) 先求出口气体的组成。
因为出口气体中,故
,,,
再求出口气体的摩尔流速
利用Amagat定律求出口气体的摩尔体积。
先从附表查得的,,则可求出各组分的对比性质为
: ,
: ,
: ,
按照上述对比参数,查二参数普遍化Z图,得
,,
则
故
出口管中气体的体积流速为
出口管中气体的流速,,可按下式运算,
式中:A为管子的截面积。运算得出出口管中混合气体的流速为。
58页第2章
2-1 求温度673.15K、压力4.053MPa的甲烷气体摩尔体积。
题目解答
答案
(a)Consfantinou, Gani和O’Connell法推测估算法,对上述三种不同化合物的偏心因子和298K饱和液体的摩尔体积都比较成功地进行了推测,误差也不算太大,在工程运算中应该有其应用价值。
(b)从预期来讲,二阶估算的结果应该要比一阶估算的好。但从实际估算结果知,并非如此,例如环乙烷的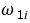 和
和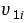 两者的二阶估算结果都比一阶估算结果差;丙烯酸的
两者的二阶估算结果都比一阶估算结果差;丙烯酸的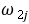 估算,情形也与上述相同。估量显现相仿情形的场合,可能为数许多,讲明该法应有改进的需要。
估算,情形也与上述相同。估量显现相仿情形的场合,可能为数许多,讲明该法应有改进的需要。
2-10 估算150℃时乙硫醇的液体的摩尔体积。已知实验值为0.095。乙硫醇的物性参数为=499K、=5.49MPa、=0.207、=0.190,20℃的饱和液体密度为839。
[解] 方法1:用Rackett方程运算液体摩尔体积。
Rackett方程为
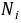
其中:
故 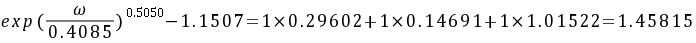
乙硫醇的摩尔体积为0.0972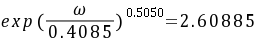 ,该值和实验值0.095相比,误差为2.31%。
,该值和实验值0.095相比,误差为2.31%。
方法2:用Lyderson方法运算
由20℃时的饱和液体密度求出此状态的摩尔体积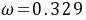 ,M为乙硫醇的摩尔质量,则
,M为乙硫醇的摩尔质量,则
20℃时的对比温度为
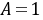
按照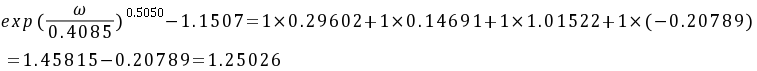 值,从图2-11的饱和液体线上查得对比度密度,
值,从图2-11的饱和液体线上查得对比度密度,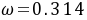 =2.77。同理,
=2.77。同理,
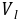
按照此值,从图2-11的饱和液体线上查得 。故按照Lyderson方程,有
。故按照Lyderson方程,有
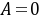
乙硫醇的摩尔体积运算值为0.0954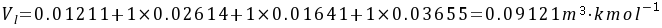 ,和实验值相比,误差为0.42%。
,和实验值相比,误差为0.42%。
2-11 50℃、60.97Mpa由0.401(摩尔分数)的氮和0.599(摩尔分数)的乙烯组成混合气体,试用下列4种方法求算混合气体的摩尔体积。已知从实验数据,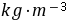 。(1)理想气体方程;(2)Amagat定律和普遍化压缩因子图;(3) 虚拟临界常数法(Kay规则);(4) 混合物的第二维里系数法。
。(1)理想气体方程;(2)Amagat定律和普遍化压缩因子图;(3) 虚拟临界常数法(Kay规则);(4) 混合物的第二维里系数法。