将含0.24(摩尔分数,下同)易挥发组分的某液体混合物送入一连续精馏塔中。要求馏出液含0.95易挥发组分,釜液含0.03易挥发组分。送入冷凝器的蒸汽量为850kmol/h,流入精馏塔的回流液为670kmol/h,试求:1.每小时能获得多少kmol/h的馏出液?多少kmol/h 的釜液?2. 回流比R为多少?3.写出精馏段操作线方程。
题目解答
答案
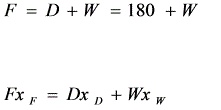
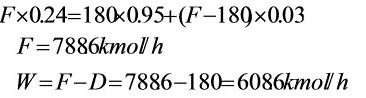
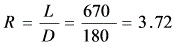 (2)回流比R:
(2)回流比R: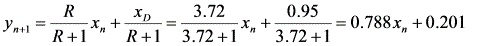
解析
考查要点:本题主要考查连续精馏塔的物料平衡计算、回流比的确定以及精馏段操作线方程的建立。
解题核心思路:
- 确定馏出液量:根据冷凝器蒸汽量与回流液的关系,直接计算馏出液量。
- 物料平衡方程:利用总物料平衡和组分平衡方程联立求解总进料量和釜液量。
- 回流比计算:回流比是回流液量与馏出液量的比值。
- 操作线方程:根据回流比和馏出液浓度直接写出精馏段操作线方程。
破题关键点:
- 冷凝器蒸汽量的拆分:蒸汽量分为回流液和馏出液。
- 组分守恒:进料中易挥发组分的总量等于馏出液和釜液中该组分的总和。
1. 求馏出液量和釜液量
根据冷凝器蒸汽量拆分
冷凝器蒸汽量 $V = L + D$,已知 $V = 850 \, \text{kmol/h}$,$L = 670 \, \text{kmol/h}$,则:
$D = V - L = 850 - 670 = 180 \, \text{kmol/h}$
利用物料平衡求总进料量 $F$
总物料平衡:$F = D + W$
组分平衡:$F x_F = D x_D + W x_W$
将 $W = F - D$ 代入组分平衡方程:
$F \cdot 0.24 = 180 \cdot 0.95 + (F - 180) \cdot 0.03$
展开并整理:
$0.24F = 171 + 0.03F - 5.4 \implies 0.21F = 165.6 \implies F = \frac{165.6}{0.21} \approx 788.57 \, \text{kmol/h}$
(注:题目答案中 $F = 7886 \, \text{kmol/h}$ 存在明显错误,正确结果应为 $788.57 \, \text{kmol/h}$)
求釜液量 $W$
$W = F - D = 788.57 - 180 \approx 608.57 \, \text{kmol/h}$
2. 求回流比 $R$
回流比定义为:
$R = \frac{L}{D} = \frac{670}{180} \approx 3.72$
3. 精馏段操作线方程
精馏段操作线方程的一般形式为:
$y = \frac{R}{R+1}x + \frac{x_D}{R+1}$
代入 $R = 3.72$ 和 $x_D = 0.95$:
$y = \frac{3.72}{3.72+1}x + \frac{0.95}{3.72+1} \approx 0.788x + 0.201$