题目
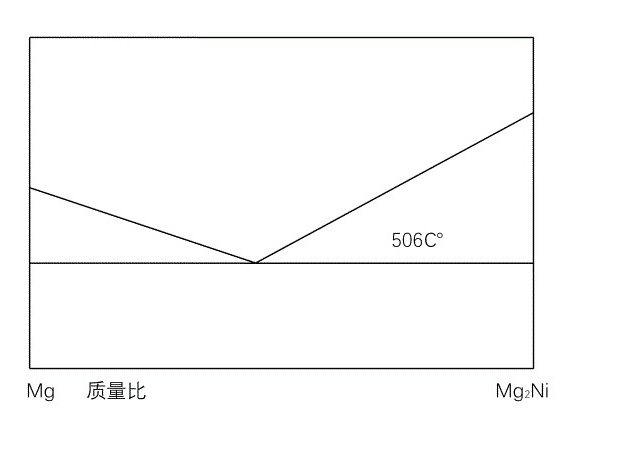
Mg-Ni系在506℃有一共晶反应为:L(23.5Wt.%Ni) ——>α(纯镁)+Mg2Ni(54.6Wt.%Ni) ,如图所示。设C1为亚共晶合金,C2为过共晶合金,这两种合金中的先共晶相的重量分数相等,但C1合金中的α 总量为C2合金中的α 总量的2.5倍,试计算C1和C2的成分。b506C-|||-Mg 质量比 Mg2Ni
Mg-Ni系在506℃有一共晶反应为:L(23.5Wt.%Ni) ——>α(纯镁)+Mg2Ni(54.6Wt.%Ni) ,如图所示。设C1为亚共晶合金,C2为过共晶合金,这两种合金中的先共晶相的重量分数相等,但C1合金中的α 总量为C2合金中的α 总量的2.5倍,试计算C1和C2的成分。b
题目解答
答案
解:C1和C2合金的先共晶相分别为α-Mg和Mg2Ni,
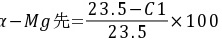 ,
,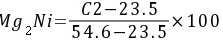
根据题意有: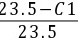
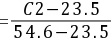 (1)
(1)
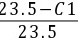
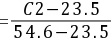 (1)
(1)C1和C2合金中的α 总量分别为α-Mg1和α-Mg2
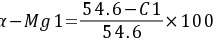 ,
,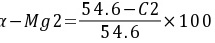
根据题意有: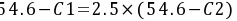 (2)
(2)
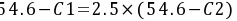 (2)
(2)联立(1)、(2)两式可得:
C1=12.7%; C2=37.8%
解析
步骤 1:确定先共晶相的重量分数
对于亚共晶合金C1,先共晶相为α-Mg,其重量分数为:
$$
\frac{23.5 - C1}{23.5}
$$
对于过共晶合金C2,先共晶相为Mg2Ni,其重量分数为:
$$
\frac{C2 - 23.5}{54.6 - 23.5}
$$
根据题意,这两种合金中的先共晶相的重量分数相等,因此有:
$$
\frac{23.5 - C1}{23.5} = \frac{C2 - 23.5}{54.6 - 23.5}
$$
步骤 2:确定α-Mg的总量
对于亚共晶合金C1,α-Mg的总量为:
$$
\frac{54.6 - C1}{54.6}
$$
对于过共晶合金C2,α-Mg的总量为:
$$
\frac{54.6 - C2}{54.6}
$$
根据题意,C1合金中的α-Mg总量为C2合金中的α-Mg总量的2.5倍,因此有:
$$
\frac{54.6 - C1}{54.6} = 2.5 \times \frac{54.6 - C2}{54.6}
$$
步骤 3:联立方程求解C1和C2
联立步骤1和步骤2中的方程,可以求解C1和C2的值。
$$
\frac{23.5 - C1}{23.5} = \frac{C2 - 23.5}{54.6 - 23.5}
$$
$$
\frac{54.6 - C1}{54.6} = 2.5 \times \frac{54.6 - C2}{54.6}
$$
解得:
$$
C1 = 12.7\%
$$
$$
C2 = 37.8\%
$$
对于亚共晶合金C1,先共晶相为α-Mg,其重量分数为:
$$
\frac{23.5 - C1}{23.5}
$$
对于过共晶合金C2,先共晶相为Mg2Ni,其重量分数为:
$$
\frac{C2 - 23.5}{54.6 - 23.5}
$$
根据题意,这两种合金中的先共晶相的重量分数相等,因此有:
$$
\frac{23.5 - C1}{23.5} = \frac{C2 - 23.5}{54.6 - 23.5}
$$
步骤 2:确定α-Mg的总量
对于亚共晶合金C1,α-Mg的总量为:
$$
\frac{54.6 - C1}{54.6}
$$
对于过共晶合金C2,α-Mg的总量为:
$$
\frac{54.6 - C2}{54.6}
$$
根据题意,C1合金中的α-Mg总量为C2合金中的α-Mg总量的2.5倍,因此有:
$$
\frac{54.6 - C1}{54.6} = 2.5 \times \frac{54.6 - C2}{54.6}
$$
步骤 3:联立方程求解C1和C2
联立步骤1和步骤2中的方程,可以求解C1和C2的值。
$$
\frac{23.5 - C1}{23.5} = \frac{C2 - 23.5}{54.6 - 23.5}
$$
$$
\frac{54.6 - C1}{54.6} = 2.5 \times \frac{54.6 - C2}{54.6}
$$
解得:
$$
C1 = 12.7\%
$$
$$
C2 = 37.8\%
$$