工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下: +2(H)_(2)leftharpoons C(H)_(3)OH-|||-+A(H)_(2)leftharpoons (C(H)_(3))_(2)O+(H)_(2)O-|||-CO+3H2 CH4+H 2O-|||-4CO+8H2 C4H9OH+3H2 o-|||-+(H)_(2)Oleftharpoons C(O)_(2)+(H)_(2)-|||-由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,-|||-为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷-|||-却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部-|||-分放空,大部分经循环压缩机后与原料气混合返回合成塔中。下图是-|||-生产流程示意图-|||-冷凝分离-|||-合成-|||-__-|||-原料气 Bkg/h 粗甲醇-|||-/h-|||-循环压缩-|||-100kmol+2(H)_(2)leftharpoons C(H)_(3)OH-|||-+A(H)_(2)leftharpoons (C(H)_(3))_(2)O+(H)_(2)O-|||-CO+3H2 CH4+H 2O-|||-4CO+8H2 C4H9OH+3H2 o-|||-+(H)_(2)Oleftharpoons C(O)_(2)+(H)_(2)-|||-由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,-|||-为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷-|||-却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部-|||-分放空,大部分经循环压缩机后与原料气混合返回合成塔中。下图是-|||-生产流程示意图-|||-冷凝分离-|||-合成-|||-__-|||-原料气 Bkg/h 粗甲醇-|||-/h-|||-循环压缩-|||-100kmol
工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下: 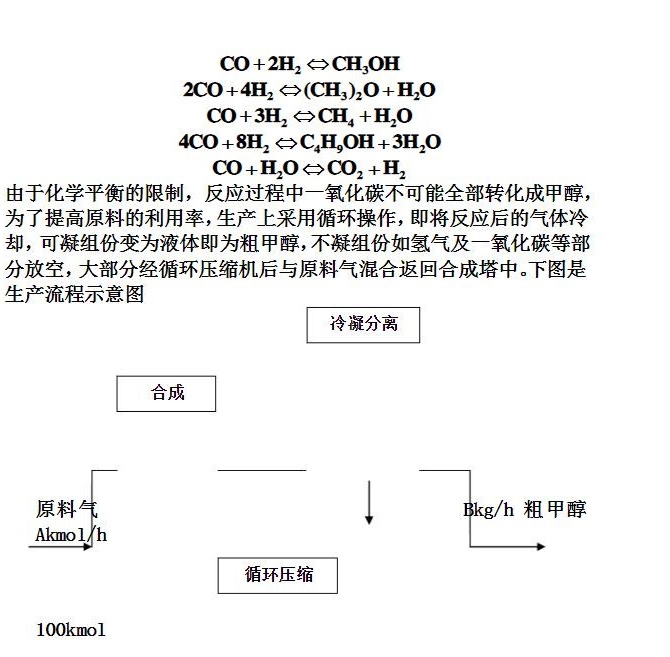
题目解答
答案


解析
题目考察知识
本题主要考察化工原理中的物料衡算、转化率与收率的计算,涉及多组分反应系统的物料平衡、关键组分(如N₂)的衡算以及溶解气体的处理。
解题思路详解
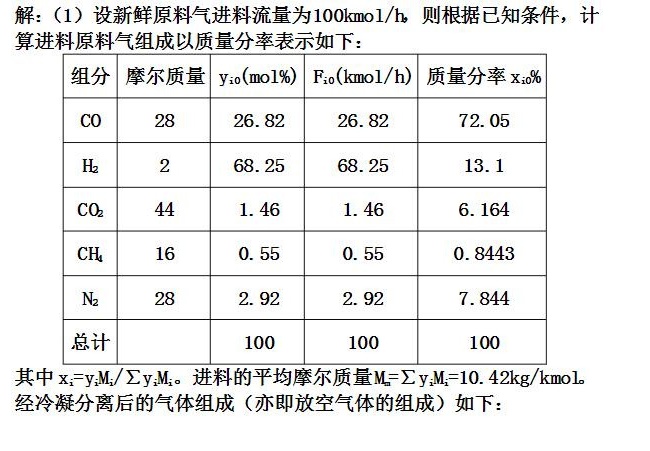
1. 新鲜原料气组成计算
设新鲜原料气进料流量为 $100\ \text{kmol/h}$,根据题目给出的摩尔分数($y_{i0}$)和各组分摩尔质量(\\(M_i\)),计算质量分率:
$x_{i0} = \frac{y_{i0}M_i}{\sum y_{i0}M_i}$
进料平均摩尔质量:
$M_n = \sum y_{i0}M_i = 10.42\ \text{kg/kmol}$
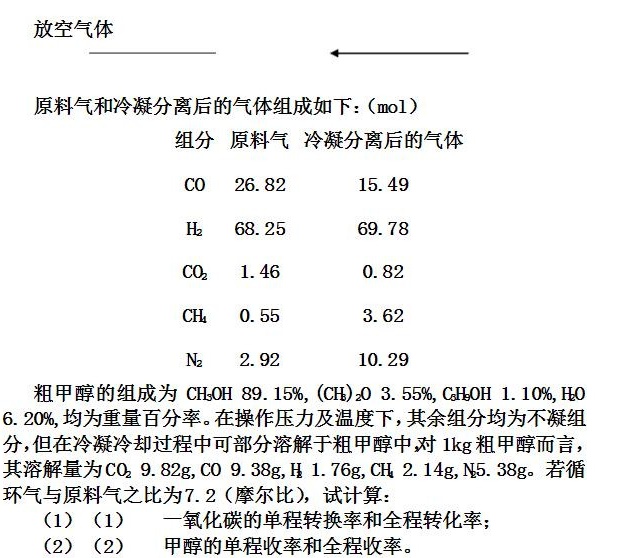
2. 放空气体与粗甲醇流量计算
通过N₂衡算和总物料衡算联立求解:
- N₂衡算:放空气中N₂摩尔分数为0.1029,粗甲醇中溶解N₂量为 $5.38\ \text{g/kg}$,则:
$\frac{5.38B}{28 \times 1000} + 0.1029A = = 2.92$ - 总物料衡衡算:新鲜原料气总质量等于粗甲醇质量加放空气体质量:
$100 \times 10.42 = B + 9.554A$
联立解得:$A = 26.91\ \ \text{kmol/h}$,$B = 785.2\text{kg/h}$
3. 一氧化碳转化率计算
-
全程转化率:
反应后CO摩尔流量 $F_{\text{CO}} = 0.1549A + \frac{9.38B}{28 \times 1000} = 4.435\ \text{kmol/h}$
全程转化率:
$X_{\text{CO,全程}} = \frac{F_{\text{CO,0}} - F_{\text{CO}}}{F_{\text{CO,0}}} = \frac{26.82 - 4.435}{26.82} = 83.48\%$ -
单程转化率:
反应器出口CO流量(新鲜气+循环气):
$F_{\text{CO\}} = 100 \times 0.2682 + 7.2 \times 100 \times 0.1549 = 138.4\ \text{kmol/h}$
单程转化率:
$X_{\text{CO,单程}} = \frac{F_{\text{CO,0}} - F_{\text{CO}}}{F_{\text{CO}}} = \frac{26.82 - 4.435}{138.4} = 16.2\%$
4. 甲醇收率计算
-
粗甲醇中甲醇含量:粗甲醇总质量 $B = 785\ \text{kg/h}$,扣除溶解气体质量($0.02848\ \text{kg}$),甲醇质量:
$m_{\text{CH3OH}} = 785 \times 0.620 - 0.02848 \approx 486.7\ \text{g} = 0.4867\ \text{kmol}$ -
全程收率:以CO为基准,理论甲醇量为 $F_{\text{CO,0}} = 26.82\ \text{kmol}$,则:
$Y_{\text{全程}} = \frac{0_{\text{CH3OH}}}{F_{\text{CO,0}}} = \frac{0.4867}{26.82} \times 1000} \approx 79.2\%$ -
单程收率:以反应器入口CO为基准:
$Y_{\text{单程}} = \frac{0.4867}{138.4} \approx 15.36\%$