求3-9. 有A和B两个容器,A容器充满饱和液态水,B容器充满饱和蒸气。两个容器的体积均为1L,压力都为1MPa。如果这两个容器爆炸,试问哪一个容器被破坏的更严重?假定A、B容器内物质做可逆绝热膨胀,快速绝热膨胀到0.1 MPa。3-10. 一容器内的液体水和蒸汽在1MPa压力下处于平衡状态,质量为1kg。假如容器内液体和蒸汽各占一半体积,试求容器内的液体水和蒸汽的总焓。解:查按压力排列的饱和水蒸汽表,1MPa时,根据题意液体和蒸汽各占一半体积,设干度为x则解之得:所以3-1.br>1. 过热蒸汽的状态为533Khe 1.0.36MPa,通过喷嘴膨胀,出口压力为0.2067MPa,如果过程为可逆绝热且达到平衡,试问蒸汽在喷嘴出口的状态如何?3-12. 试求算366K、2.0.6MPa下1mol乙烷的体积、焓、熵与内能。设255K、0.1013MPa时乙烷的焓、熵为零。已知乙烷在理想气体状态下的摩尔恒压热容3-13. 试采用RK方程求算在227℃、5 MPa下气相正丁烷的剩余焓和剩余熵。
9. 有A和B两个容器,A容器充满饱和液态水,B容器充满饱和蒸气。两个容器的体积均为1L,压力都为1MPa。如果这两个容器爆炸,试问哪一个容器被破坏的更严重?假定A、B容器内物质做可逆绝热膨胀,快速绝热膨胀到
0.1 MPa。3-1
0. 一容器内的液体水和蒸汽在1MPa压力下处于平衡状态,质量为1kg。假如容器内液体和蒸汽各占一半体积,试求容器内的液体水和蒸汽的总焓。解:查按压力排列的饱和水蒸汽表,1MPa时,根据题意液体和蒸汽各占一半体积,设干度为x则解之得:所以3-
1.br>1. 过热蒸汽的状态为533Khe 1.
0.36MPa,通过喷嘴膨胀,出口压力为0.2067MPa,如果过程为可逆绝热且达到平衡,试问蒸汽在喷嘴出口的状态如何?3-1
2. 试求算366K、2.
0.6MPa下1mol乙烷的体积、焓、熵与内能。设255K、0.1013MPa时乙烷的焓、熵为零。已知乙烷在理想气体状态下的摩尔恒压热容3-1
3. 试采用RK方程求算在227℃、5 MPa下气相正丁烷的剩余焓和剩余熵。
题目解答
答案
解:查附录得正丁烷的临界参数:Tc=425.2K、Pc=3.800MPa、ω=0.193
又R-K方程: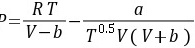
∴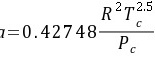
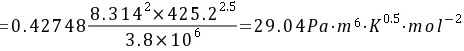

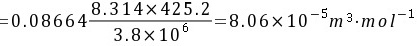
∴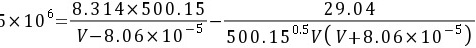
试差求得:V=5.61×10-4m3/mol
∴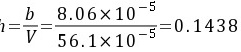
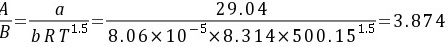
∴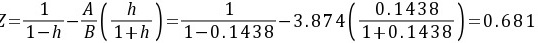
∴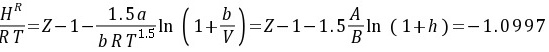
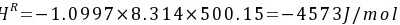
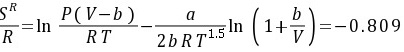
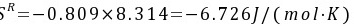
3-14. 假设二氧化碳服从RK状态方程,试计算50℃、10.13 MPa时二氧化碳的逸度。
解:查附录得二氧化碳的临界参数:Tc=304.2.2K、Pc=7.376MPa
∴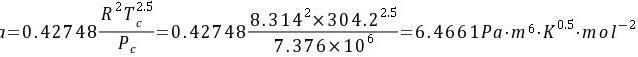
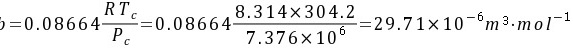
又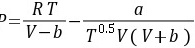
∴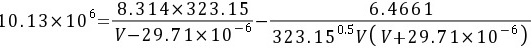
迭代求得:V=294.9cm3/mol
∴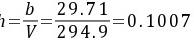
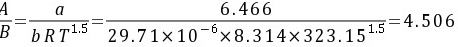
∴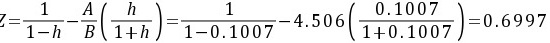
∴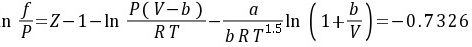
∴f=4.869MPa
3-15. 试计算液态水在30℃下,压力分别为(a)饱和蒸汽压、(b)100×105Pa下的逸度和逸度系数。已知:(1)水在30℃时饱和蒸汽压pS=0.0424×105Pa;(2)30℃,0~100×105Pa范围内将液态水的摩尔体积视为常数,其值为0.01809m3/kmol;(3)1×105Pa以下的水蒸气可以视为理想气体。
解:(a)30℃,Ps=0.0424×105Pa
∵汽液平衡时,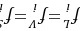
又1×105Pa以下的水蒸气可以视为理想气体,Ps=0.0424×105Pa<1×105Pa
∴30℃、0.0424×105Pa下的水蒸气可以视为理想气体。
又 理想气体的fi=P
∴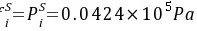
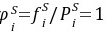
(b)30℃,100×105Pa
∵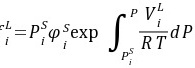
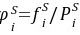
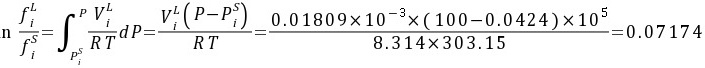
∴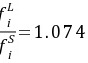
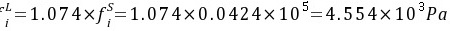
3-16. 有人用A和B两股水蒸汽通过绝热混合获得0.5MPa的饱和蒸汽,其中A股是干度为98%的湿蒸汽,压力为0.5MPa,流量为1kg/s;而B股是473.15K,0.5MPa的过热蒸汽,试求B股过热蒸汽的流量该为多少?
 解:A股:查按压力排列的饱和水蒸汽表, 0.5MPa(151.9℃)时,
解:A股:查按压力排列的饱和水蒸汽表, 0.5MPa(151.9℃)时,
B股: 473.15K,0.5MPa的过热蒸汽
根据题意,为等压过程,
忽略混合过程中的散热损失,绝热混合 Qp = 0,所以混合前后焓值不变
设B股过热蒸汽的流量为 x kg/s,以1秒为计算基准,列能量衡算式
解得:
该混合过程为不可逆绝热混合,所以混合前后的熵值不相等。
只有可逆绝热过程,
因为是等压过程,该题也不应该用进行计算。