题目
废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、SiO2。某研究性学习小组设计如图1工艺流程回收镍,制备硫酸镍晶体(NiSO4⋅7H2O)。稀H2SO4-|||-废镍 →滤液 有机溶剂 含铜有机层 →滤液2 、操作B →NiSO4·7H2O-|||-液化剂→份碎 →酸变 操作A →溶液→阅pH-|||-→滤流1 ↑ →滤渣2-|||-H2O2 图1该小组同学查阅资料知:①镍的化学性质与铁相似,能与酸缓慢反应;②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示: 金属离子 Ni2+ Al3+ Fe3+ Fe2+ 开始沉淀时(c=0.01mol⋅L-1)的pH 7.2 3.7 2.2 7.5 沉淀完全时(c=1.0×10-5mol⋅L-1)的pH 8.7 4.7 3.2 9.0 (1)除“粉碎”外,请你再写出一条提高废镍催化剂酸浸效率的措施 ____ 。(2)滤渣1的主要成分有 ____ 。(3)实验室中进行操作A所用的主要玻璃仪器有 ____ 。(4)“溶液”中加入H2O2目的是 ____ (用离子方程式表示)。(5)下列物质调溶液pH,最好选用 ____ (填字母标号)。a.氨水b.稀H2SO4c.NiCO3d.Na2CO3若调pH前c(Ni2+)=1.0mol⋅L-1,Al3+和Fe3+浓度均为0.01mol⋅L-1,则“调pH”需控制溶液pH的范围为 ____ 。(6)如图2为NiSO4,溶解度随温度变化关系,据图分析操作B是 ____ 。稀H2SO4-|||-废镍 →滤液 有机溶剂 含铜有机层 →滤液2 、操作B →NiSO4·7H2O-|||-液化剂→份碎 →酸变 操作A →溶液→阅pH-|||-→滤流1 ↑ →滤渣2-|||-H2O2 图1
废镍催化剂主要含Ni,还有少量Cu、Fe、Al及其氧化物、SiO2。某研究性学习小组设计如图1工艺流程回收镍,制备硫酸镍晶体(NiSO4⋅7H2O)。
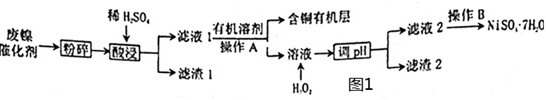
该小组同学查阅资料知:
①镍的化学性质与铁相似,能与酸缓慢反应;
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
(1)除“粉碎”外,请你再写出一条提高废镍催化剂酸浸效率的措施 ____ 。
(2)滤渣1的主要成分有 ____ 。
(3)实验室中进行操作A所用的主要玻璃仪器有 ____ 。
(4)“溶液”中加入H2O2目的是 ____ (用离子方程式表示)。
(5)下列物质调溶液pH,最好选用 ____ (填字母标号)。
a.氨水
b.稀H2SO4
c.NiCO3
d.Na2CO3
若调pH前c(Ni2+)=1.0mol⋅L-1,Al3+和Fe3+浓度均为0.01mol⋅L-1,则“调pH”需控制溶液pH的范围为 ____ 。
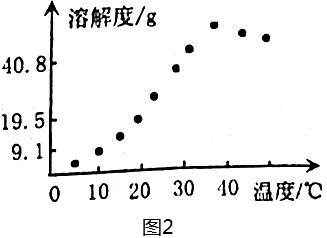
(6)如图2为NiSO4,溶解度随温度变化关系,据图分析操作B是 ____ 。

该小组同学查阅资料知:
①镍的化学性质与铁相似,能与酸缓慢反应;
②溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol⋅L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10-5mol⋅L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(2)滤渣1的主要成分有 ____ 。
(3)实验室中进行操作A所用的主要玻璃仪器有 ____ 。
(4)“溶液”中加入H2O2目的是 ____ (用离子方程式表示)。
(5)下列物质调溶液pH,最好选用 ____ (填字母标号)。
a.氨水
b.稀H2SO4
c.NiCO3
d.Na2CO3
若调pH前c(Ni2+)=1.0mol⋅L-1,Al3+和Fe3+浓度均为0.01mol⋅L-1,则“调pH”需控制溶液pH的范围为 ____ 。
(6)如图2为NiSO4,溶解度随温度变化关系,据图分析操作B是 ____ 。

题目解答
答案
解:(1)根据外界条件对反应速率的影响可知除“粉碎”外,能提高废镍催化剂酸浸效率的措施还有升高酸浸温度或适当增大硫酸浓度、搅拌等,
故答案为:升高酸浸温度或适当增大硫酸浓度、搅拌等;
(2)根据以上分析可知滤渣1的主要成分有SiO2、Cu,
故答案为:SiO2、Cu;
(3)操作A是萃取分液,则实验室中进行操作A所用的主要玻璃仪器有分液漏斗、烧杯,
故答案为:分液漏斗、烧杯;
(4)根据以上分析可知“溶液”中加入H2O2目的是氧化溶液中的亚铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(5)氨水、Na2CO3能调节pH,但引入新杂质,稀H2SO4增强酸性,不能消耗氢离子,NiCO3能消耗氢离子,调节pH,且不会引入新杂质,故选c;根据表中数据可知铁离子完全沉淀的pH是3.2,铝离子完全沉淀的pH是4.7,镍离子开始沉淀的pH是7.2,所以氢氧化镍的溶度积常数是0.01×(10-6.8)2=10-15.6,由于调pH前镍离子浓度是1.0mol⋅L-1,则镍离子开始沉淀时氢氧根浓度是$\sqrt{1{0}^{-15.6}}$mol/L=10-7.8mol/L,对应的pH是6.2,则需控制溶液pH的范围为4.7≤pH<6.2,
故答案为:c;4.7≤pH<6.2;
(6)根据图象可知NiSO4的溶解度随温度的升高先增大后减小,所以据图分析操作B是加热浓缩、降温结晶,
故答案为:加热浓缩、降温结晶。
故答案为:升高酸浸温度或适当增大硫酸浓度、搅拌等;
(2)根据以上分析可知滤渣1的主要成分有SiO2、Cu,
故答案为:SiO2、Cu;
(3)操作A是萃取分液,则实验室中进行操作A所用的主要玻璃仪器有分液漏斗、烧杯,
故答案为:分液漏斗、烧杯;
(4)根据以上分析可知“溶液”中加入H2O2目的是氧化溶液中的亚铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(5)氨水、Na2CO3能调节pH,但引入新杂质,稀H2SO4增强酸性,不能消耗氢离子,NiCO3能消耗氢离子,调节pH,且不会引入新杂质,故选c;根据表中数据可知铁离子完全沉淀的pH是3.2,铝离子完全沉淀的pH是4.7,镍离子开始沉淀的pH是7.2,所以氢氧化镍的溶度积常数是0.01×(10-6.8)2=10-15.6,由于调pH前镍离子浓度是1.0mol⋅L-1,则镍离子开始沉淀时氢氧根浓度是$\sqrt{1{0}^{-15.6}}$mol/L=10-7.8mol/L,对应的pH是6.2,则需控制溶液pH的范围为4.7≤pH<6.2,
故答案为:c;4.7≤pH<6.2;
(6)根据图象可知NiSO4的溶解度随温度的升高先增大后减小,所以据图分析操作B是加热浓缩、降温结晶,
故答案为:加热浓缩、降温结晶。
解析
- 考查要点:本题围绕废镍催化剂的回收工艺,综合考查化学反应条件控制、物质分离与提纯、溶液中离子沉淀条件、结晶方法选择等知识。
- 解题核心:
- 反应条件优化:通过外界条件(如温度、浓度、接触面积)影响反应速率;
- 物质成分分析:根据金属活动性、溶解性判断滤渣成分;
- 离子共存与沉淀条件:利用金属离子沉淀pH范围控制溶液酸碱度;
- 结晶方法选择:根据溶解度随温度变化趋势确定结晶方式。
(1)提高酸浸效率的措施
关键思路:通过增大反应速率的措施提高酸浸效率。
具体方法:
- 升高温度:加快反应速率;
- 增大硫酸浓度:提高反应物浓度;
- 搅拌:加速物质传递,减少局部浓度极化。
(2)滤渣1的主要成分
关键分析:
- 废镍催化剂中的SiO₂不与酸反应,直接进入滤渣;
- 铜的金属活动性弱于氢,不与稀硫酸反应,保留在滤渣中。
(3)操作A的玻璃仪器
操作判断:根据工艺流程,操作A为萃取分液,需用分液漏斗和烧杯。
(4)H₂O₂的作用
反应本质:H₂O₂将Fe²⁺氧化为Fe³⁺,便于后续沉淀。
离子方程式:
$2\text{Fe}^{2+} + \text{H}_2\text{O}_2 + 2\text{H}^+ \rightarrow 2\text{Fe}^{3+} + 2\text{H}_2\text{O}$
(5)pH调节剂的选择及范围
关键步骤:
- 选择调节剂:
- NiCO₃与酸反应生成Ni²⁺,消耗H⁺调节pH,且不引入新杂质。
- 确定pH范围:
- Al³⁺、Fe³⁺完全沉淀:需pH ≥ 4.7(Al³⁺完全沉淀);
- Ni²⁺未沉淀:需pH < 7.2(Ni²⁺开始沉淀)。
- 实际范围:结合Ni²⁺溶度积计算,最终控制pH为 4.7 ≤ pH < 6.2。
(6)操作B的确定
溶解度分析:
- 图2显示NiSO₄溶解度随温度先增大后减小,适合加热浓缩、降温结晶。