题目
在间歇反应器中有一级液相可逆反应,初始反应时CA0=0.5mol/L,CP0=0反应8min后,A的转化率为1/3,而平衡转化率是2/3,求此反应的动力学方程式.
在间歇反应器中有一级液相可逆反应,初始反应时CA0=0.5mol/L,CP0=0反应8min后,A的转化率为1/3,而平衡转化率是2/3,求此反应的动力学方程式.
题目解答
答案
解: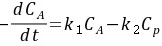
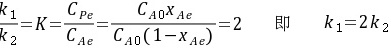
根据一级可逆反应积分式
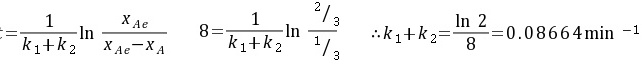
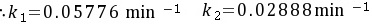
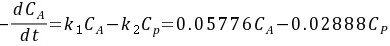
解析
步骤 1:确定反应速率方程
对于一级可逆反应,反应速率方程可以表示为:
$-\dfrac {d{C}_{A}}{dt}={k}_{1}{C}_{A}-{k}_{2}{C}_{P}$
其中,${k}_{1}$ 和 ${k}_{2}$ 分别是正向和逆向反应的速率常数,${C}_{A}$ 和 ${C}_{P}$ 分别是反应物A和产物P的浓度。
步骤 2:确定平衡常数
根据平衡转化率,可以确定平衡常数K:
$\dfrac {{K}_{1}}{{K}_{2}}=K=\dfrac {{C}_{Pe}}{{C}_{Ae}}=\dfrac {{C}_{AD}{A}_{Ae}}{{C}_{AD(1-{x}_{Ae})}}=2$
即 ${k}_{1}=2{k}_{2}$
步骤 3:确定速率常数
根据一级可逆反应积分式,可以确定速率常数${k}_{1}$和${k}_{2}$:
$\dfrac {1}{{k}_{1}+{k}_{2}}\ln \dfrac {{x}_{Ae}}{{x}_{Ae}-{x}_{A}}$
将已知条件代入,得到:
$8=\dfrac {1}{{k}_{1}+{k}_{2}}\ln \dfrac {2/3}{{1}_{3}}$
解得:${k}_{1}+{k}_{2}=\dfrac {\ln 2}{8}=0.08664{min}^{-1}$
结合${k}_{1}=2{k}_{2}$,可以解得:
${k}_{1}=0.05776min^{-1}$ .${k}_{2}=0.02888min^{-1}$
步骤 4:确定反应动力学方程
将速率常数代入反应速率方程,得到反应动力学方程:
$-\dfrac {d{C}_{A}}{dt}={k}_{1}{C}_{A}-{k}_{2}{C}_{P}=0.05776{C}_{A}-0.02888{C}_{P}$
对于一级可逆反应,反应速率方程可以表示为:
$-\dfrac {d{C}_{A}}{dt}={k}_{1}{C}_{A}-{k}_{2}{C}_{P}$
其中,${k}_{1}$ 和 ${k}_{2}$ 分别是正向和逆向反应的速率常数,${C}_{A}$ 和 ${C}_{P}$ 分别是反应物A和产物P的浓度。
步骤 2:确定平衡常数
根据平衡转化率,可以确定平衡常数K:
$\dfrac {{K}_{1}}{{K}_{2}}=K=\dfrac {{C}_{Pe}}{{C}_{Ae}}=\dfrac {{C}_{AD}{A}_{Ae}}{{C}_{AD(1-{x}_{Ae})}}=2$
即 ${k}_{1}=2{k}_{2}$
步骤 3:确定速率常数
根据一级可逆反应积分式,可以确定速率常数${k}_{1}$和${k}_{2}$:
$\dfrac {1}{{k}_{1}+{k}_{2}}\ln \dfrac {{x}_{Ae}}{{x}_{Ae}-{x}_{A}}$
将已知条件代入,得到:
$8=\dfrac {1}{{k}_{1}+{k}_{2}}\ln \dfrac {2/3}{{1}_{3}}$
解得:${k}_{1}+{k}_{2}=\dfrac {\ln 2}{8}=0.08664{min}^{-1}$
结合${k}_{1}=2{k}_{2}$,可以解得:
${k}_{1}=0.05776min^{-1}$ .${k}_{2}=0.02888min^{-1}$
步骤 4:确定反应动力学方程
将速率常数代入反应速率方程,得到反应动力学方程:
$-\dfrac {d{C}_{A}}{dt}={k}_{1}{C}_{A}-{k}_{2}{C}_{P}=0.05776{C}_{A}-0.02888{C}_{P}$