题目
乙烯是一种重要的化工原料,实验室和工业上分别可由乙醇和乙烷为原料制取。(一)实验室用乙醇在一定条件下脱水制乙烯的过程中通常涉及下列两个反应:脱水制乙烯Ⅰ:C2H5OH(g)⇌C2H4(g)+H2O(g)△H1K1脱水制乙醚Ⅱ:2C2H5OH(g)⇌C2H5OC2H5(g)+H2O(g)△H2K2研究所得相关信息如下:①已知上述反应的压强平衡常数与温度之间的关系如图1所示:7-|||-6-|||-5-|||-4 一脱水制乙烯-|||-3 脱水制乙醚-|||-2-|||-1-|||-D-|||-373 423 473523 573 623-|||-温度/K-|||-图1②不同温度下乙醇的转化率及产物的选择性如表: 反应温度(K) 乙醇转化率(%) 乙烯选择性(%) 乙醚选择性(%) 副产物选择性(%) 373 25.22 4.38 94.52 1.10 423 54.25 52.24 46.71 1.05 523 95.20 96.87 2.15 0.98 (1)下列说法正确的是 ____ 。A.反应Ⅰ在任何条件下均能自发进行B.若反应2C2H4(g)+H2O(g)⇌C2H5OC2H5(g)的平衡常数为K3,则K3=((K)_(2))/(({K)_{1)}^2}C.温度升高,反应I平衡正移程度大于反应II逆移程度,所以乙醇的转化率升高D.恒温密闭容器中,发生上述反应,达到平衡后,缩小容器体积,重新平衡时,与原平衡比较,乙烯的产率增大(2)为研究乙烯水化法合成乙醇,T℃时,发生反应C2H4(g)+H2O(g)⇌C2H5OH(g),向体积为1L的密闭容器中投入0.5molH2O(g)和0.5molC2H4(g),5min后恰好达到平衡。平衡时则得C2H5OH(g)的体积分数为(1)/(9),容器内的总压为9.0MPa,则该温度下反应的平衡常数Kp= ____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(二)工业上现代氧化裂解法利用乙烷制取乙烯的热化学方程式如下:C2H6(g)+1O2(g)═C2H4(g)+H2O(g)△H2=-110kJ/mol。已知乙烷的氧化裂解反应产物中除了C2H4外,还存在CH4、CO、CO2等副产物(副反应均为放热反应),且原料气中氧气含量低会导致反应产生积炭,堵塞反应管。[乙烯选择性=(n((C)_(2)/(H)_{4))}(n({C)_(2)(H)_(4))+n(C(H)_(4))+n(CO)+n(C(O)_(2))};乙烯收率=乙烷转化率×乙烯选择性](3)图2为温度对乙烷氧化裂解反应性能的影响。请解释随着温度的升高,乙烷的转化率升高而乙烯的选择性却下降的原因 ____ 。7-|||-6-|||-5-|||-4 一脱水制乙烯-|||-3 脱水制乙醚-|||-2-|||-1-|||-D-|||-373 423 473523 573 623-|||-温度/K-|||-图1(4)图3为(n((C)_(2)/(H)_{6))}(n({O)_(2))}的值对乙烷氧化裂解反应达到平衡时乙烷转化率和乙烯收率的影响。请分析乙烷氧化裂解反应过程中通常选择(n((C)_(2)/(H)_{6))}(n({O)_(2))}=2.0的理由是 ____ 。7-|||-6-|||-5-|||-4 一脱水制乙烯-|||-3 脱水制乙醚-|||-2-|||-1-|||-D-|||-373 423 473523 573 623-|||-温度/K-|||-图1(5)请在图3中绘出乙烯选择性随(n((C)_(2)/(H)_{6))}(n({O)_(2))}值变化的曲线(并用③标注) ____ 。
乙烯是一种重要的化工原料,实验室和工业上分别可由乙醇和乙烷为原料制取。
(一)实验室用乙醇在一定条件下脱水制乙烯的过程中通常涉及下列两个反应:
脱水制乙烯Ⅰ:C2H5OH(g)⇌C2H4(g)+H2O(g)△H1K1
脱水制乙醚Ⅱ:2C2H5OH(g)⇌C2H5OC2H5(g)+H2O(g)△H2K2
研究所得相关信息如下:
①已知上述反应的压强平衡常数与温度之间的关系如图1所示:
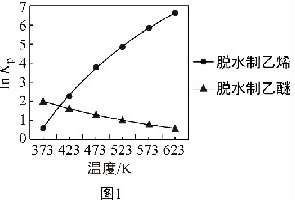
②不同温度下乙醇的转化率及产物的选择性如表:
(1)下列说法正确的是 ____ 。
A.反应Ⅰ在任何条件下均能自发进行
B.若反应2C2H4(g)+H2O(g)⇌C2H5OC2H5(g)的平衡常数为K3,则K3=$\frac{{K}_{2}}{{{K}_{1}}^{2}}$
C.温度升高,反应I平衡正移程度大于反应II逆移程度,所以乙醇的转化率升高
D.恒温密闭容器中,发生上述反应,达到平衡后,缩小容器体积,重新平衡时,与原平衡比较,乙烯的产率增大
(2)为研究乙烯水化法合成乙醇,T℃时,发生反应C2H4(g)+H2O(g)⇌C2H5OH(g),向体积为1L的密闭容器中投入0.5molH2O(g)和0.5molC2H4(g),5min后恰好达到平衡。平衡时则得C2H5OH(g)的体积分数为$\frac{1}{9}$,容器内的总压为9.0MPa,则该温度下反应的平衡常数Kp= ____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(二)工业上现代氧化裂解法利用乙烷制取乙烯的热化学方程式如下:C2H6(g)+1O2(g)═C2H4(g)+H2O(g)△H2=-110kJ/mol。已知乙烷的氧化裂解反应产物中除了C2H4外,还存在CH4、CO、CO2等副产物(副反应均为放热反应),且原料气中氧气含量低会导致反应产生积炭,堵塞反应管。[乙烯选择性=$\frac{n({C}_{2}{H}_{4})}{n({C}_{2}{H}_{4})+n(C{H}_{4})+n(CO)+n(C{O}_{2})}$;乙烯收率=乙烷转化率×乙烯选择性]
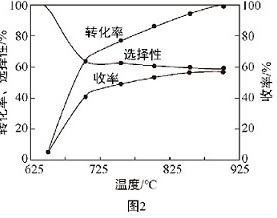
(3)图2为温度对乙烷氧化裂解反应性能的影响。请解释随着温度的升高,乙烷的转化率升高而乙烯的选择性却下降的原因 ____ 。
(4)图3为$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$的值对乙烷氧化裂解反应达到平衡时乙烷转化率和乙烯收率的影响。请分析乙烷氧化裂解反应过程中通常选择$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$=2.0的理由是 ____ 。
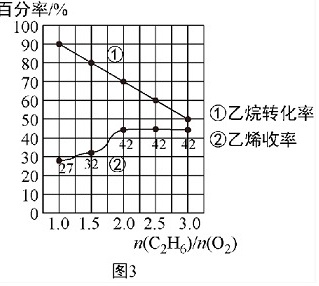
(5)请在图3中绘出乙烯选择性随$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$值变化的曲线(并用③标注) ____ 。
(一)实验室用乙醇在一定条件下脱水制乙烯的过程中通常涉及下列两个反应:
脱水制乙烯Ⅰ:C2H5OH(g)⇌C2H4(g)+H2O(g)△H1K1
脱水制乙醚Ⅱ:2C2H5OH(g)⇌C2H5OC2H5(g)+H2O(g)△H2K2
研究所得相关信息如下:
①已知上述反应的压强平衡常数与温度之间的关系如图1所示:

②不同温度下乙醇的转化率及产物的选择性如表:
| 反应温度(K) | 乙醇转化率(%) | 乙烯选择性(%) | 乙醚选择性(%) | 副产物选择性(%) |
| 373 | 25.22 | 4.38 | 94.52 | 1.10 |
| 423 | 54.25 | 52.24 | 46.71 | 1.05 |
| 523 | 95.20 | 96.87 | 2.15 | 0.98 |
A.反应Ⅰ在任何条件下均能自发进行
B.若反应2C2H4(g)+H2O(g)⇌C2H5OC2H5(g)的平衡常数为K3,则K3=$\frac{{K}_{2}}{{{K}_{1}}^{2}}$
C.温度升高,反应I平衡正移程度大于反应II逆移程度,所以乙醇的转化率升高
D.恒温密闭容器中,发生上述反应,达到平衡后,缩小容器体积,重新平衡时,与原平衡比较,乙烯的产率增大
(2)为研究乙烯水化法合成乙醇,T℃时,发生反应C2H4(g)+H2O(g)⇌C2H5OH(g),向体积为1L的密闭容器中投入0.5molH2O(g)和0.5molC2H4(g),5min后恰好达到平衡。平衡时则得C2H5OH(g)的体积分数为$\frac{1}{9}$,容器内的总压为9.0MPa,则该温度下反应的平衡常数Kp= ____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(二)工业上现代氧化裂解法利用乙烷制取乙烯的热化学方程式如下:C2H6(g)+1O2(g)═C2H4(g)+H2O(g)△H2=-110kJ/mol。已知乙烷的氧化裂解反应产物中除了C2H4外,还存在CH4、CO、CO2等副产物(副反应均为放热反应),且原料气中氧气含量低会导致反应产生积炭,堵塞反应管。[乙烯选择性=$\frac{n({C}_{2}{H}_{4})}{n({C}_{2}{H}_{4})+n(C{H}_{4})+n(CO)+n(C{O}_{2})}$;乙烯收率=乙烷转化率×乙烯选择性]
(3)图2为温度对乙烷氧化裂解反应性能的影响。请解释随着温度的升高,乙烷的转化率升高而乙烯的选择性却下降的原因 ____ 。

(4)图3为$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$的值对乙烷氧化裂解反应达到平衡时乙烷转化率和乙烯收率的影响。请分析乙烷氧化裂解反应过程中通常选择$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$=2.0的理由是 ____ 。

(5)请在图3中绘出乙烯选择性随$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$值变化的曲线(并用③标注) ____ 。
题目解答
答案
解:(1)A.分析图1可知,反应I为吸热熵增反应,结合吉布斯自由能公式ΔG=ΔH-TΔS<O,该反应可以在高温下自发进行,故A错误;
B.若反应2C2H4(g)+H2O(g)⇌C2H5OC2H5(g)的平衡常数为K3,设该反应为反应III,反应III=反应II×2-反应I,故K3=$\frac{{K}_{2}}{{{K}_{1}}^{2}}$,故B正确;
C.分析图像斜率可得,温度升高,反应I平衡正移程度大于反应II逆移程度,所以乙醇的转化率升高,故C正确;
D.恒温密闭容器中,发生上述反应,达到平衡后,缩小容器体积,相当于加压操作,反应I平衡左移,反应II平衡不一定,故D错误;
故答案为:BC;
(2)向体积为1L的密闭容器中投入0.5molH2O(g)和0.5molC2H4(g),5min后恰好达到平衡。平衡时则得C2H5OH(g)的体积分数为1/9,容器内的总压为9.0MPa,可得三段式
C2H4(g)+H2O(g)⇌C2H5OH(g)
起始 0.5 0.5 0
转化 x x x
终止 0.5-x 0.5-x x
平衡时则得C2H5OH(g)的体积分数为$\frac{1}{9}$,故$\frac{x}{0.5-x+0.5-x+x}$=$\frac{1}{9}$,x=0.1,平衡常数Kp=$\frac{p(CH{}_{3}CH{}_{2}OH)}{p(H{}_{2}O)×p(C{}_{2}H{}_{4})}$=$\frac{9.0×\frac{0.1}{0.9}}{9.0×\frac{0.4}{0.9}×9.0×\frac{0.4}{0.9}}$MPa-1=0.0625MPa-1,
故答案为:0.0625MPa-1;
(3)分析图2可得,乙烷的转化率升高而乙烯的选择性却下降的原因为温度升高,使反应物间的碰撞几率增大,加快了乙烷氧化裂解反应的速率,使乙烷的转化率增加;同时乙烷发生深度氧化的副反应也随温度升高而速率显著加快,从而使乙烯的选择性下降,
故答案为:温度升高,使反应物间的碰撞几率增大,加快了乙烷氧化裂解反应的速率,使乙烷的转化率增加;同时乙烷发生深度氧化的副反应也随温度升高而速率显著加快,从而使乙烯的选择性下降;
(4)分析图3可得,$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$小于2.0时,乙烯的收率降低,$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$大于2.0时,乙烯的收率并未增加且会产生更多的积炭,堵塞反应管,
故答案为:$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$小于2.0时,乙烯的收率降低,$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$大于2.0时,乙烯的收率并未增加且会产生更多的积炭,堵塞反应管;
(5)n(C2H6)/n(O2)=1.0时,乙烯选择性=0.3;
n(C2H6)/n(O2)=1.5时,乙烯选择性=0.4;
n(C2H6)/n(O2)=2.0时,乙烯选择性=0.6;
n(C2H6)/n(O2)=2.5时,乙烯选择性=0.7;
n(C2H6)/n(O2)=3.0时,乙烯选择性=0.84,故乙烯选择性随$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$值变化的曲线为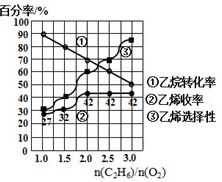 ,
,
故答案为: 。
。
B.若反应2C2H4(g)+H2O(g)⇌C2H5OC2H5(g)的平衡常数为K3,设该反应为反应III,反应III=反应II×2-反应I,故K3=$\frac{{K}_{2}}{{{K}_{1}}^{2}}$,故B正确;
C.分析图像斜率可得,温度升高,反应I平衡正移程度大于反应II逆移程度,所以乙醇的转化率升高,故C正确;
D.恒温密闭容器中,发生上述反应,达到平衡后,缩小容器体积,相当于加压操作,反应I平衡左移,反应II平衡不一定,故D错误;
故答案为:BC;
(2)向体积为1L的密闭容器中投入0.5molH2O(g)和0.5molC2H4(g),5min后恰好达到平衡。平衡时则得C2H5OH(g)的体积分数为1/9,容器内的总压为9.0MPa,可得三段式
C2H4(g)+H2O(g)⇌C2H5OH(g)
起始 0.5 0.5 0
转化 x x x
终止 0.5-x 0.5-x x
平衡时则得C2H5OH(g)的体积分数为$\frac{1}{9}$,故$\frac{x}{0.5-x+0.5-x+x}$=$\frac{1}{9}$,x=0.1,平衡常数Kp=$\frac{p(CH{}_{3}CH{}_{2}OH)}{p(H{}_{2}O)×p(C{}_{2}H{}_{4})}$=$\frac{9.0×\frac{0.1}{0.9}}{9.0×\frac{0.4}{0.9}×9.0×\frac{0.4}{0.9}}$MPa-1=0.0625MPa-1,
故答案为:0.0625MPa-1;
(3)分析图2可得,乙烷的转化率升高而乙烯的选择性却下降的原因为温度升高,使反应物间的碰撞几率增大,加快了乙烷氧化裂解反应的速率,使乙烷的转化率增加;同时乙烷发生深度氧化的副反应也随温度升高而速率显著加快,从而使乙烯的选择性下降,
故答案为:温度升高,使反应物间的碰撞几率增大,加快了乙烷氧化裂解反应的速率,使乙烷的转化率增加;同时乙烷发生深度氧化的副反应也随温度升高而速率显著加快,从而使乙烯的选择性下降;
(4)分析图3可得,$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$小于2.0时,乙烯的收率降低,$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$大于2.0时,乙烯的收率并未增加且会产生更多的积炭,堵塞反应管,
故答案为:$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$小于2.0时,乙烯的收率降低,$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$大于2.0时,乙烯的收率并未增加且会产生更多的积炭,堵塞反应管;
(5)n(C2H6)/n(O2)=1.0时,乙烯选择性=0.3;
n(C2H6)/n(O2)=1.5时,乙烯选择性=0.4;
n(C2H6)/n(O2)=2.0时,乙烯选择性=0.6;
n(C2H6)/n(O2)=2.5时,乙烯选择性=0.7;
n(C2H6)/n(O2)=3.0时,乙烯选择性=0.84,故乙烯选择性随$\frac{n({C}_{2}{H}_{6})}{n({O}_{2})}$值变化的曲线为
 ,
,故答案为:
 。
。