题目
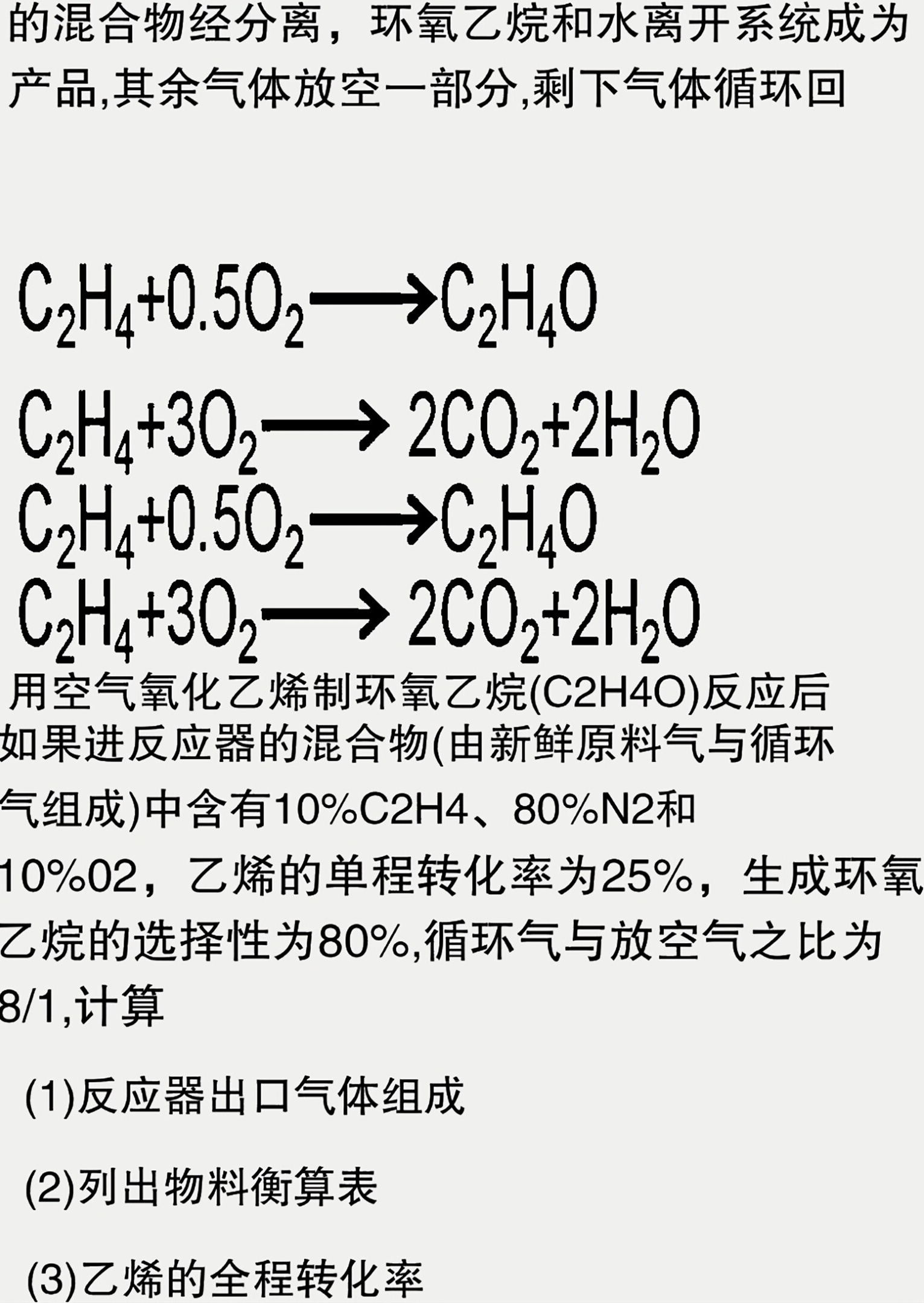
的混合物经分离,环氧乙烷和水离开系统成为-|||-产品,其余气体放空一部分,剩下气体循环回-|||-_(2)(H)_(4)+0.5(O)_(2)arrow (C)_(2)(H)_(4)O-|||-_(2)(H)_(4)+3(O)_(2)arrow 2C(O)_(2)+2(H)_(2)O-|||-_(2)(H)_(4)+0.5(O)_(2)arrow (C)_(2)(H)_(4)O-|||-2 4 +30 `2->2CO 2 +2H2-|||-用空气氧化乙烯制环氧乙烷(C2H4O)反应后-|||-如果进反应器的混合物(由新鲜原料气与循环-|||-气组成)中含有10%C2H4、80%N2和-|||-10%02,乙烯的单程转化率为25%,生成环氧-|||-乙烷的选择性为80%,循环气与放空气之比为-|||-8/1 ,计算-|||-(1)反应器出口气体组成-|||-(2)列出物料衡算表-|||-(3)乙烯的全程转化率
题目解答
答案
4.用空气氧化乙烯制环氧乙烷(C2H4O),反应后的混合物经分离,环氧乙烷和水离开系统成为产品,其余气体放空一部分,剩下的气体循环回反应器,若只考虑发生以下两个反应
如果进反应器的混合物(由新鲜原料气与循环气组成)中含有10%C2H4,80%N2,10%O2,乙烯的单程转化率为25%,生成环氧乙烷的选择性为80%,循环气与放空气之比为8/1,计算反应器出口气体的组成和乙烯的全程转化率。
如果进反应器的混合物(由新鲜原料气与循环气组成)中含有10%C2H4,80%N2,10%O2,乙烯的单程转化率为25%,生成环氧乙烷的选择性为80%,循环气与放空气之比为8/1,计算反应器出口气体的组成和乙烯的全程转化率。
解析
步骤 1:确定反应方程式
乙烯(C2H4)与氧气(O2)反应生成环氧乙烷(C2H4O)和二氧化碳(CO2)及水(H2O)的反应方程式为:
\[ C_2H_4 + \frac{1}{2}O_2 \rightarrow C_2H_4O \]
\[ C_2H_4 + 3O_2 \rightarrow 2CO_2 + 2H_2O \]
步骤 2:计算反应器出口气体组成
假设进入反应器的混合气体总量为100 mol,其中乙烯(C2H4)为10 mol,氮气(N2)为80 mol,氧气(O2)为10 mol。乙烯的单程转化率为25%,生成环氧乙烷的选择性为80%。
乙烯的转化量为:10 mol × 25% = 2.5 mol
生成环氧乙烷的量为:2.5 mol × 80% = 2 mol
生成二氧化碳和水的量为:2.5 mol × 20% = 0.5 mol
根据反应方程式,生成2 mol环氧乙烷需要消耗1 mol氧气,生成0.5 mol二氧化碳和水需要消耗1.5 mol氧气,因此总共消耗氧气为2 mol。
剩余氧气量为:10 mol - 2 mol = 8 mol
剩余乙烯量为:10 mol - 2.5 mol = 7.5 mol
因此,反应器出口气体组成如下:
乙烯(C2H4):7.5 mol
环氧乙烷(C2H4O):2 mol
氮气(N2):80 mol
氧气(O2):8 mol
二氧化碳(CO2):0.5 mol
水(H2O):0.5 mol
步骤 3:列出物料衡算表
物料衡算表如下:
| 物料 | 进料量(mol) | 反应量(mol) | 出料量(mol) |
|------|--------------|--------------|--------------|
| C2H4 | 10 | 2.5 | 7.5 |
| C2H4O| 0 | 2 | 2 |
| N2 | 80 | 0 | 80 |
| O2 | 10 | 2 | 8 |
| CO2 | 0 | 0.5 | 0.5 |
| H2O | 0 | 0.5 | 0.5 |
步骤 4:计算乙烯的全程转化率
循环气与放空气之比为8/1,因此循环气量为80 mol,放空气量为10 mol。乙烯的全程转化率为:
\[ \frac{2.5}{10} \times 100\% = 25\% \]
乙烯(C2H4)与氧气(O2)反应生成环氧乙烷(C2H4O)和二氧化碳(CO2)及水(H2O)的反应方程式为:
\[ C_2H_4 + \frac{1}{2}O_2 \rightarrow C_2H_4O \]
\[ C_2H_4 + 3O_2 \rightarrow 2CO_2 + 2H_2O \]
步骤 2:计算反应器出口气体组成
假设进入反应器的混合气体总量为100 mol,其中乙烯(C2H4)为10 mol,氮气(N2)为80 mol,氧气(O2)为10 mol。乙烯的单程转化率为25%,生成环氧乙烷的选择性为80%。
乙烯的转化量为:10 mol × 25% = 2.5 mol
生成环氧乙烷的量为:2.5 mol × 80% = 2 mol
生成二氧化碳和水的量为:2.5 mol × 20% = 0.5 mol
根据反应方程式,生成2 mol环氧乙烷需要消耗1 mol氧气,生成0.5 mol二氧化碳和水需要消耗1.5 mol氧气,因此总共消耗氧气为2 mol。
剩余氧气量为:10 mol - 2 mol = 8 mol
剩余乙烯量为:10 mol - 2.5 mol = 7.5 mol
因此,反应器出口气体组成如下:
乙烯(C2H4):7.5 mol
环氧乙烷(C2H4O):2 mol
氮气(N2):80 mol
氧气(O2):8 mol
二氧化碳(CO2):0.5 mol
水(H2O):0.5 mol
步骤 3:列出物料衡算表
物料衡算表如下:
| 物料 | 进料量(mol) | 反应量(mol) | 出料量(mol) |
|------|--------------|--------------|--------------|
| C2H4 | 10 | 2.5 | 7.5 |
| C2H4O| 0 | 2 | 2 |
| N2 | 80 | 0 | 80 |
| O2 | 10 | 2 | 8 |
| CO2 | 0 | 0.5 | 0.5 |
| H2O | 0 | 0.5 | 0.5 |
步骤 4:计算乙烯的全程转化率
循环气与放空气之比为8/1,因此循环气量为80 mol,放空气量为10 mol。乙烯的全程转化率为:
\[ \frac{2.5}{10} \times 100\% = 25\% \]