题目
随着煤和石油等不可再生能源的日益枯竭,同时在“碳达峰”与“碳中和”可持续发展的目标下,作为清洁能源的天然气受到了广泛的关注。甲烷干重整反应(DRM)可以将两种温室气体(CH4和CO2)直接转化为合成气(主要成分为CO和H2),兼具环境效益和经济效益。(1)已知:CH4、CO和H2的燃烧热(ΔH)分别为-893kJ•mol-1、-283kJ•mol-1和-284kJ•mol-1。写出甲烷干重整反应的热化学方程式: ____ 。(2)甲烷干重整过程中可能存在反应:R1:CO2(g)+CH4(g)⇌2CO(g)+2H2(g)(主反应)R2:CO2(g)+H2(g)⇌CO(g)+H2O(g)R3:CH4(g)⇌C(s)+2H2(g)R4:2CO(g)⇌C(s)+CO2(g)R5:CO(g)+H2(g)⇌C(s)+H2O(g)各反应的lgK(K为各反应的平衡常数)与温度的关系如图所示。-R-11-|||-←R2-|||-4 ←R3-|||-→R4-|||-3-|||-2 lgk=0-|||-当 ★-|||-0 ,-|||--1 方-|||--2-|||--3-|||-500 600 700 800 900 1000-|||-温度/℃由图可知,为提高主反应的转化率应 ____ (填“升高温度”或“降低温度”)。(3)在1×105Pa、进料配比n(CH4):n(CO2)=1:1、温度为500~1000℃的条件下,甲烷干重整过程中甲烷的转化率、CO2的转化率和积碳率随着温度变化的规律如图所示。-R-11-|||-←R2-|||-4 ←R3-|||-→R4-|||-3-|||-2 lgk=0-|||-当 ★-|||-0 ,-|||--1 方-|||--2-|||--3-|||-500 600 700 800 900 1000-|||-温度/℃①甲烷干重整的最佳温度为 ____ ℃。②在最佳温度、p条件下,向某2L的恒容密闭容器中加入2mol CO2和2mol CH4,设只发生R1、R2两个反应。达平衡后,测得容器中CO的浓度为1.4mol•L-1,CO2的转化率为90%,则此时R1反应的压强平衡常数Kp= ____ (保留两位有效数字,压强平衡常数用各组分的平衡分压代替物质的量浓度进行计算,平衡分压=物质的量分数×平衡总压强)。(4)恒容绝热条件下仅发生主反应时,下列情况能说明该反应达到平衡状态的有 ____ (填标号)。A.CH4和CO2的转化率相等B.2v(CH4)=v(CO)C.CH4的体积分数保持不变D.体系的温度不再变化(5)合成气可以用于生成甲醇,在容积为2L的恒容密闭容器中加入2mol H2和1mol CO,发生反应H2(g)+CO(g)→CH3OH(g)(未配平),各组分的物质的量随时间的变化如图所示。-R-11-|||-←R2-|||-4 ←R3-|||-→R4-|||-3-|||-2 lgk=0-|||-当 ★-|||-0 ,-|||--1 方-|||--2-|||--3-|||-500 600 700 800 900 1000-|||-温度/℃0~5min内v(H2)= ____ mol•L-1•min-1;15min时改变的条件不可能是 ____ (填标号)。A.充入H2B.充入COC.通入惰性气体
随着煤和石油等不可再生能源的日益枯竭,同时在“碳达峰”与“碳中和”可持续发展的目标下,作为清洁能源的天然气受到了广泛的关注。甲烷干重整反应(DRM)可以将两种温室气体(CH4和CO2)直接转化为合成气(主要成分为CO和H2),兼具环境效益和经济效益。
(1)已知:CH4、CO和H2的燃烧热(ΔH)分别为-893kJ•mol-1、-283kJ•mol-1和-284kJ•mol-1。写出甲烷干重整反应的热化学方程式: ____ 。
(2)甲烷干重整过程中可能存在反应:
R1:CO2(g)+CH4(g)⇌2CO(g)+2H2(g)(主反应)
R2:CO2(g)+H2(g)⇌CO(g)+H2O(g)
R3:CH4(g)⇌C(s)+2H2(g)
R4:2CO(g)⇌C(s)+CO2(g)
R5:CO(g)+H2(g)⇌C(s)+H2O(g)
各反应的lgK(K为各反应的平衡常数)与温度的关系如图所示。
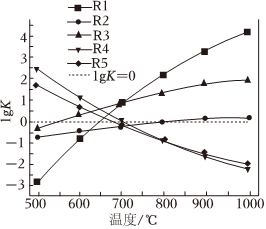
由图可知,为提高主反应的转化率应 ____ (填“升高温度”或“降低温度”)。
(3)在1×105Pa、进料配比n(CH4):n(CO2)=1:1、温度为500~1000℃的条件下,甲烷干重整过程中甲烷的转化率、CO2的转化率和积碳率随着温度变化的规律如图所示。
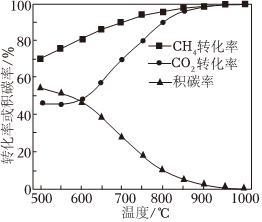
①甲烷干重整的最佳温度为 ____ ℃。
②在最佳温度、p条件下,向某2L的恒容密闭容器中加入2mol CO2和2mol CH4,设只发生R1、R2两个反应。达平衡后,测得容器中CO的浓度为1.4mol•L-1,CO2的转化率为90%,则此时R1反应的压强平衡常数Kp= ____ (保留两位有效数字,压强平衡常数用各组分的平衡分压代替物质的量浓度进行计算,平衡分压=物质的量分数×平衡总压强)。
(4)恒容绝热条件下仅发生主反应时,下列情况能说明该反应达到平衡状态的有 ____ (填标号)。
A.CH4和CO2的转化率相等
B.2v(CH4)=v(CO)
C.CH4的体积分数保持不变
D.体系的温度不再变化
(5)合成气可以用于生成甲醇,在容积为2L的恒容密闭容器中加入2mol H2和1mol CO,发生反应H2(g)+CO(g)→CH3OH(g)(未配平),各组分的物质的量随时间的变化如图所示。
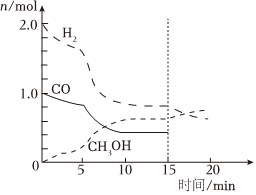
0~5min内v(H2)= ____ mol•L-1•min-1;15min时改变的条件不可能是 ____ (填标号)。
A.充入H2
B.充入CO
C.通入惰性气体
(1)已知:CH4、CO和H2的燃烧热(ΔH)分别为-893kJ•mol-1、-283kJ•mol-1和-284kJ•mol-1。写出甲烷干重整反应的热化学方程式: ____ 。
(2)甲烷干重整过程中可能存在反应:
R1:CO2(g)+CH4(g)⇌2CO(g)+2H2(g)(主反应)
R2:CO2(g)+H2(g)⇌CO(g)+H2O(g)
R3:CH4(g)⇌C(s)+2H2(g)
R4:2CO(g)⇌C(s)+CO2(g)
R5:CO(g)+H2(g)⇌C(s)+H2O(g)
各反应的lgK(K为各反应的平衡常数)与温度的关系如图所示。

由图可知,为提高主反应的转化率应 ____ (填“升高温度”或“降低温度”)。
(3)在1×105Pa、进料配比n(CH4):n(CO2)=1:1、温度为500~1000℃的条件下,甲烷干重整过程中甲烷的转化率、CO2的转化率和积碳率随着温度变化的规律如图所示。

①甲烷干重整的最佳温度为 ____ ℃。
②在最佳温度、p条件下,向某2L的恒容密闭容器中加入2mol CO2和2mol CH4,设只发生R1、R2两个反应。达平衡后,测得容器中CO的浓度为1.4mol•L-1,CO2的转化率为90%,则此时R1反应的压强平衡常数Kp= ____ (保留两位有效数字,压强平衡常数用各组分的平衡分压代替物质的量浓度进行计算,平衡分压=物质的量分数×平衡总压强)。
(4)恒容绝热条件下仅发生主反应时,下列情况能说明该反应达到平衡状态的有 ____ (填标号)。
A.CH4和CO2的转化率相等
B.2v(CH4)=v(CO)
C.CH4的体积分数保持不变
D.体系的温度不再变化
(5)合成气可以用于生成甲醇,在容积为2L的恒容密闭容器中加入2mol H2和1mol CO,发生反应H2(g)+CO(g)→CH3OH(g)(未配平),各组分的物质的量随时间的变化如图所示。

0~5min内v(H2)= ____ mol•L-1•min-1;15min时改变的条件不可能是 ____ (填标号)。
A.充入H2
B.充入CO
C.通入惰性气体
题目解答
答案
解:(1)根据题干信息,甲烷干重整反应(DRM)可以将两种温室气体(CH4和CO2)直接转化为合成气(主要成分为CO和H2),该反应方程式为CH4(g)+CO4(g)⇌2CO(g)+2H2(g),CH4、CO和H2的燃烧热(ΔH)分别为-893kJ•mol-1、-283kJ•mol-1和-284kJ•mol-1,写出热化学方程式为①CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH1=-893kJ/mol,②$CO(g)+\frac{1}{2}{O}_{2}(g)=C{O}_{2}(g)\;Δ{H}_{2}=-283kJ/mol$,③${H}_{2}(g)+\frac{1}{2}{O}_{2}(g)={H}_{2}O(l)\;Δ{H}_{3}=-284kJ/mol$,根据盖斯定律,①-2×②-2×③得到CH4(g)+CO4(g)⇌2CO(g)+2H2(g),故该反应的ΔH=ΔH1-2ΔH2-2ΔH3=+241kJ/mol,
故答案为:CH4(g)+CO4(g)⇌2CO(g)+2H2(g)ΔH=+241kJ/mol;
(2)从图中看出,随温度升高,主反应R1及R2、R3反应的lgK都增大,平衡常数增大,平衡都正向移动,R4、R5反应的lgK都减小,平衡常数减小,平衡逆向移动,但温度升高主反应R1的lgK与温度关系曲线的斜率,即正向反应程度大,转化率高,故升高温度,有利于提高主反应的转化率,
故答案为:升高温度;
(3)①从图中可看出,随温度升高,甲烷干重整过程中甲烷的转化率增大、CO2的转化率增大和积碳率减小,温度升高到900℃后CH4的转化率与CO2的转化率几乎相等,且达到97%以上,900℃后积碳率很低,说明几乎只发生甲烷干重整主反应R1,故甲烷干重整的最佳温度为900℃,
故答案为:900℃;
②设R1反应中CO2的物质的量变化量为xmol,R2反应中的物质的量变化量为ymol,由已知条件可知,平衡时CO2的转化率为90%,CO的浓度为1.4mol/L,根据三段式分析,
CO2(g)+CH4(g)⇌2CO(g)+2H2(g)$\begin{array}{c}\end{array}$
起始/mol:2 2 0 0
变化/mol:a a 2a 2a
CO2(g)+H2(g)⇌CO(g)+H2O(g)
起始/mol:2 2 0 0
变化/mol:b b b b
则$\frac{x+y}{2}×100%=90%$,$\frac{2x+y}{2}=1.4mol/L$,解得x=1mol,y=0.8mol,平衡时,CO2物质的量为0.2mol,CH4物质的量为1mol,CO物质的量为2.8mol,H2物质的量为1.2mol,H2O物质的量为0.8mol,气体总物质的量为6mol,平衡时气体总压强为${p}_{总}=\frac{6mol}{4mol}×{p}_{初}=1.5p$,R1反应的${K}_{p}=\frac{[{p}_{总}×\frac{n(CO)}{{n}_{总}}]^{2}×[{p}_{总}×\frac{n({H}_{2})}{{n}_{总}}]^{2}}{[{p}_{总}×\frac{n(C{O}_{2})}{{n}_{总}}]×[{p}_{总}×\frac{n(C{H}_{4})}{{n}_{总}}]}=\frac{(1.5p×\frac{2.8}{6})^{2}×(1.5p×\frac{1.2}{6})^{2}}{(1.5p×\frac{0.2}{6})×(1.5p×\frac{1}{6})}≈3.5{p}^{2}$,
故答案为:3.5p2;
(4)A.CO2和CH4的转化率相等,不能说明该反应达到平衡状态,故A错误;
B.2v(CH4)=v(CO),未说明反应速率表示的方向,不能体现v(正)=v(逆),不能说明该反应达到平衡状态,故B错误;
C.随反应进行CH4的体积分数减小,则CH4的体积分数保持不变,能说明该反应达到平衡状态,故C正确;
D.该反应为吸热反应,随反应进行,体系的温度降低,温度不再变化,能说明该反应达到平衡状态,故D正确;
故答案为:CD;
(5)从图中可看出,5min时,CH3OH(g)的物质的量为0.2mol,则根据2H2(g)+CO(g)⇌CH3OH(g)可知,消耗的H2(g)的物质的量为0.4mol,0~5min内$v({H}_{2})=\frac{\frac{0.4mol}{2L}}{5min}=0.04mol•{L}^{-1}•mi{n}^{-1}$;反应10~15min处于平衡状态,15min时,改变条件后,CH3OH(g)的物质的量逐渐增加,H2(g)的物质的量在原平衡状态下逐渐减小,说明平衡正移:
A.若充入H2(g),平衡正移,但H2(g)总量不是在原平衡基础上逐渐减小,而应是15min时显著增加,平衡正移,H2(g)逐渐减小,故A错误;
B.充入CO,平衡正移,H2(g)的物质的量逐渐减小,CH3OH(g)的物质的量逐渐增加,故B正确;
C.通入惰性气体,恒容密闭容器体积不变,总压增大,但各组分分压不变,平衡不移动,故C错误;
故答案为:0.04;AC。
故答案为:CH4(g)+CO4(g)⇌2CO(g)+2H2(g)ΔH=+241kJ/mol;
(2)从图中看出,随温度升高,主反应R1及R2、R3反应的lgK都增大,平衡常数增大,平衡都正向移动,R4、R5反应的lgK都减小,平衡常数减小,平衡逆向移动,但温度升高主反应R1的lgK与温度关系曲线的斜率,即正向反应程度大,转化率高,故升高温度,有利于提高主反应的转化率,
故答案为:升高温度;
(3)①从图中可看出,随温度升高,甲烷干重整过程中甲烷的转化率增大、CO2的转化率增大和积碳率减小,温度升高到900℃后CH4的转化率与CO2的转化率几乎相等,且达到97%以上,900℃后积碳率很低,说明几乎只发生甲烷干重整主反应R1,故甲烷干重整的最佳温度为900℃,
故答案为:900℃;
②设R1反应中CO2的物质的量变化量为xmol,R2反应中的物质的量变化量为ymol,由已知条件可知,平衡时CO2的转化率为90%,CO的浓度为1.4mol/L,根据三段式分析,
CO2(g)+CH4(g)⇌2CO(g)+2H2(g)$\begin{array}{c}\end{array}$
起始/mol:2 2 0 0
变化/mol:a a 2a 2a
CO2(g)+H2(g)⇌CO(g)+H2O(g)
起始/mol:2 2 0 0
变化/mol:b b b b
则$\frac{x+y}{2}×100%=90%$,$\frac{2x+y}{2}=1.4mol/L$,解得x=1mol,y=0.8mol,平衡时,CO2物质的量为0.2mol,CH4物质的量为1mol,CO物质的量为2.8mol,H2物质的量为1.2mol,H2O物质的量为0.8mol,气体总物质的量为6mol,平衡时气体总压强为${p}_{总}=\frac{6mol}{4mol}×{p}_{初}=1.5p$,R1反应的${K}_{p}=\frac{[{p}_{总}×\frac{n(CO)}{{n}_{总}}]^{2}×[{p}_{总}×\frac{n({H}_{2})}{{n}_{总}}]^{2}}{[{p}_{总}×\frac{n(C{O}_{2})}{{n}_{总}}]×[{p}_{总}×\frac{n(C{H}_{4})}{{n}_{总}}]}=\frac{(1.5p×\frac{2.8}{6})^{2}×(1.5p×\frac{1.2}{6})^{2}}{(1.5p×\frac{0.2}{6})×(1.5p×\frac{1}{6})}≈3.5{p}^{2}$,
故答案为:3.5p2;
(4)A.CO2和CH4的转化率相等,不能说明该反应达到平衡状态,故A错误;
B.2v(CH4)=v(CO),未说明反应速率表示的方向,不能体现v(正)=v(逆),不能说明该反应达到平衡状态,故B错误;
C.随反应进行CH4的体积分数减小,则CH4的体积分数保持不变,能说明该反应达到平衡状态,故C正确;
D.该反应为吸热反应,随反应进行,体系的温度降低,温度不再变化,能说明该反应达到平衡状态,故D正确;
故答案为:CD;
(5)从图中可看出,5min时,CH3OH(g)的物质的量为0.2mol,则根据2H2(g)+CO(g)⇌CH3OH(g)可知,消耗的H2(g)的物质的量为0.4mol,0~5min内$v({H}_{2})=\frac{\frac{0.4mol}{2L}}{5min}=0.04mol•{L}^{-1}•mi{n}^{-1}$;反应10~15min处于平衡状态,15min时,改变条件后,CH3OH(g)的物质的量逐渐增加,H2(g)的物质的量在原平衡状态下逐渐减小,说明平衡正移:
A.若充入H2(g),平衡正移,但H2(g)总量不是在原平衡基础上逐渐减小,而应是15min时显著增加,平衡正移,H2(g)逐渐减小,故A错误;
B.充入CO,平衡正移,H2(g)的物质的量逐渐减小,CH3OH(g)的物质的量逐渐增加,故B正确;
C.通入惰性气体,恒容密闭容器体积不变,总压增大,但各组分分压不变,平衡不移动,故C错误;
故答案为:0.04;AC。