题目
杭州亚运会开幕式使用一种液体火炬燃料——“零碳甲醇”,备受瞩目,它是CO2资源化利用的有效途径,是实现“碳中和”理念的重要途径。太阳-|||-光照 ⑥ 光合 CO2 燃-|||-作用 4 烧-|||-凝结的H2O ⑤ 蒸腾 ⑦ 呼吸-|||-O2 ⑧-|||-工-|||-① 蒸 ② 降水 O2 厂-|||-发 ③ H2O蒸 ④ o-|||-海洋 发 汽车↑-|||-煤、石油、天然气-|||-图1-|||-CO2 2含量-|||-高的空气 CO2-|||-固体 高温-|||-CaO-|||-C (OH)2溶液-|||-喷雾反应器-|||-液体-|||-CO2含量-|||-低的空气-|||-图2Ⅰ.“水循环、氧循环和碳循环”是自然界存在的三大重要循环,如图1。(1)以下说法正确的是 ____ 。a.从物质变化角度看,水循环与另外两种在变化上有本质的区别b.二氧化碳的消耗途径就是氧气的产生途径c.碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定(2)结合图1,可知绿色植物通过 ____ 吸收二氧化碳。Ⅱ.“碳捕获”并封存有利于减缓温室效应。同学们设计了一个简易CO2捕捉器,其流程如图2所示。(3)写出喷雾反应器中发生反应的符号表达式 ____ 。Ⅲ.“碳”的转化与利用转化一:CH4与CO2在固相催化剂作用下可得到CO和H2,反应过程如图3所示。太阳-|||-光照 ⑥ 光合 CO2 燃-|||-作用 4 烧-|||-凝结的H2O ⑤ 蒸腾 ⑦ 呼吸-|||-O2 ⑧-|||-工-|||-① 蒸 ② 降水 O2 厂-|||-发 ③ H2O蒸 ④ o-|||-海洋 发 汽车↑-|||-煤、石油、天然气-|||-图1-|||-CO2 2含量-|||-高的空气 CO2-|||-固体 高温-|||-CaO-|||-C (OH)2溶液-|||-喷雾反应器-|||-液体-|||-CO2含量-|||-低的空气-|||-图2(4)反应一段时间后,催化剂的催化效果 ____ ,导致此现象发生的原因是 ____ ,可在原料气中加入适量 ____ 气体以有效缓解上述问题。反应中各物质的量随温度变化的曲线如图4所示,说明随着温度的升高,生成的反应物越多。(5)利用液氮的低温可将CO液化分离,从而获得纯净的氢气,说明CO的沸点比氢气的沸点 ____ 。此反应过程中分子的种类 ____ (“改变”“不改变”)。转化二:以CO2为原料制取炭黑的太阳能工艺如图5所示。太阳-|||-光照 ⑥ 光合 CO2 燃-|||-作用 4 烧-|||-凝结的H2O ⑤ 蒸腾 ⑦ 呼吸-|||-O2 ⑧-|||-工-|||-① 蒸 ② 降水 O2 厂-|||-发 ③ H2O蒸 ④ o-|||-海洋 发 汽车↑-|||-煤、石油、天然气-|||-图1-|||-CO2 2含量-|||-高的空气 CO2-|||-固体 高温-|||-CaO-|||-C (OH)2溶液-|||-喷雾反应器-|||-液体-|||-CO2含量-|||-低的空气-|||-图2(6)采用太阳能作为能量来源的优点是 ____ 。(7)在整个转化过程中,CO2最终被转化为 ____ ,反应前后Fe3O4质量会 ____ (“变大”或“不变”或“变小”)。转化三:光催化还原法能实现二氧化碳的甲烷化,将二氧化碳和水转化为甲烷和氧气。(8)催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。可以发现温度在 ____ ℃之间,甲烷生成速率加快。太阳-|||-光照 ⑥ 光合 CO2 燃-|||-作用 4 烧-|||-凝结的H2O ⑤ 蒸腾 ⑦ 呼吸-|||-O2 ⑧-|||-工-|||-① 蒸 ② 降水 O2 厂-|||-发 ③ H2O蒸 ④ o-|||-海洋 发 汽车↑-|||-煤、石油、天然气-|||-图1-|||-CO2 2含量-|||-高的空气 CO2-|||-固体 高温-|||-CaO-|||-C (OH)2溶液-|||-喷雾反应器-|||-液体-|||-CO2含量-|||-低的空气-|||-图2
杭州亚运会开幕式使用一种液体火炬燃料——“零碳甲醇”,备受瞩目,它是CO2资源化利用的有效途径,是实现“碳中和”理念的重要途径。
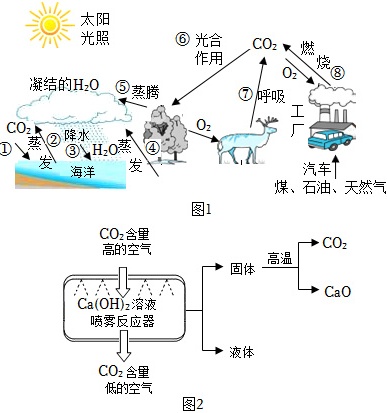
Ⅰ.“水循环、氧循环和碳循环”是自然界存在的三大重要循环,如图1。
(1)以下说法正确的是 ____ 。
a.从物质变化角度看,水循环与另外两种在变化上有本质的区别
b.二氧化碳的消耗途径就是氧气的产生途径
c.碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
(2)结合图1,可知绿色植物通过 ____ 吸收二氧化碳。
Ⅱ.“碳捕获”并封存有利于减缓温室效应。同学们设计了一个简易CO2捕捉器,其流程如图2所示。
(3)写出喷雾反应器中发生反应的符号表达式 ____ 。
Ⅲ.“碳”的转化与利用
转化一:CH4与CO2在固相催化剂作用下可得到CO和H2,反应过程如图3所示。
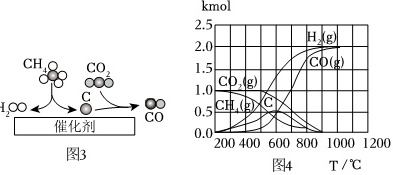
(4)反应一段时间后,催化剂的催化效果 ____ ,导致此现象发生的原因是 ____ ,可在原料气中加入适量 ____ 气体以有效缓解上述问题。反应中各物质的量随温度变化的曲线如图4所示,说明随着温度的升高,生成的反应物越多。
(5)利用液氮的低温可将CO液化分离,从而获得纯净的氢气,说明CO的沸点比氢气的沸点 ____ 。此反应过程中分子的种类 ____ (“改变”“不改变”)。
转化二:以CO2为原料制取炭黑的太阳能工艺如图5所示。
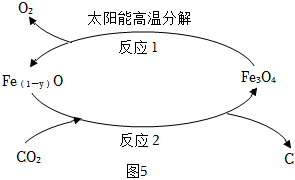
(6)采用太阳能作为能量来源的优点是 ____ 。
(7)在整个转化过程中,CO2最终被转化为 ____ ,反应前后Fe3O4质量会 ____ (“变大”或“不变”或“变小”)。
转化三:光催化还原法能实现二氧化碳的甲烷化,将二氧化碳和水转化为甲烷和氧气。
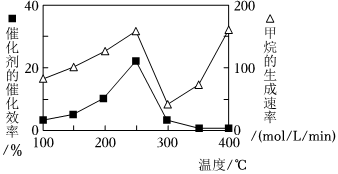
(8)催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。可以发现温度在 ____ ℃之间,甲烷生成速率加快。

Ⅰ.“水循环、氧循环和碳循环”是自然界存在的三大重要循环,如图1。
(1)以下说法正确的是 ____ 。
a.从物质变化角度看,水循环与另外两种在变化上有本质的区别
b.二氧化碳的消耗途径就是氧气的产生途径
c.碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定
(2)结合图1,可知绿色植物通过 ____ 吸收二氧化碳。
Ⅱ.“碳捕获”并封存有利于减缓温室效应。同学们设计了一个简易CO2捕捉器,其流程如图2所示。
(3)写出喷雾反应器中发生反应的符号表达式 ____ 。
Ⅲ.“碳”的转化与利用
转化一:CH4与CO2在固相催化剂作用下可得到CO和H2,反应过程如图3所示。

(4)反应一段时间后,催化剂的催化效果 ____ ,导致此现象发生的原因是 ____ ,可在原料气中加入适量 ____ 气体以有效缓解上述问题。反应中各物质的量随温度变化的曲线如图4所示,说明随着温度的升高,生成的反应物越多。
(5)利用液氮的低温可将CO液化分离,从而获得纯净的氢气,说明CO的沸点比氢气的沸点 ____ 。此反应过程中分子的种类 ____ (“改变”“不改变”)。
转化二:以CO2为原料制取炭黑的太阳能工艺如图5所示。

(6)采用太阳能作为能量来源的优点是 ____ 。
(7)在整个转化过程中,CO2最终被转化为 ____ ,反应前后Fe3O4质量会 ____ (“变大”或“不变”或“变小”)。
转化三:光催化还原法能实现二氧化碳的甲烷化,将二氧化碳和水转化为甲烷和氧气。
(8)催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。可以发现温度在 ____ ℃之间,甲烷生成速率加快。

题目解答
答案
解:(1)a.从物质变化角度看,水循环(物理变化)与另外两种在变化(化学变化)上有本质的区别,故选项正确。
b.二氧化碳的消耗途径不一定是氧气的产生途径,故选项不正确。
c.碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定,故选项正确。
(2)结合图1,可知绿色植物通过光合作用吸收二氧化碳。
(3)喷雾反应器中氢氧化钙和二氧化碳反应生成碳酸钙和水,发生反应的符号表达式是CO2+Ca(OH)2→CaCO3+H2O。
(4)反应一段时间后,催化剂的催化效果降低,导致此现象发生的原因是甲烷分解生成的碳附在催化剂表面,可在原料气中加入适量二氧化碳气体以有效缓解上述问题。
(5)利用液氮的低温可将CO液化分离,从而获得纯净的氢气,说明CO的沸点比氢气的沸点低。此反应过程中分子的种类不改变。
(6)采用太阳能作为能量来源的优点是环保、节约、充分利用自然资源。
(7)在整个转化过程中,CO2最终被转化为碳,反应前后Fe3O4质量会变小。
(8)催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。可以发现温度在300-400℃之间,甲烷生成速率加快。
故答案为:(1)ac。
(2)光合作用。
(3)CO2+Ca(OH)2→CaCO3+H2O。
(4)降低;甲烷分解生成的碳附在催化剂表面;二氧化碳。
(5)低;不改变。
(6)环保、节约、充分利用自然资源。
(7)碳;变小。
(8)300-400。
b.二氧化碳的消耗途径不一定是氧气的产生途径,故选项不正确。
c.碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定,故选项正确。
(2)结合图1,可知绿色植物通过光合作用吸收二氧化碳。
(3)喷雾反应器中氢氧化钙和二氧化碳反应生成碳酸钙和水,发生反应的符号表达式是CO2+Ca(OH)2→CaCO3+H2O。
(4)反应一段时间后,催化剂的催化效果降低,导致此现象发生的原因是甲烷分解生成的碳附在催化剂表面,可在原料气中加入适量二氧化碳气体以有效缓解上述问题。
(5)利用液氮的低温可将CO液化分离,从而获得纯净的氢气,说明CO的沸点比氢气的沸点低。此反应过程中分子的种类不改变。
(6)采用太阳能作为能量来源的优点是环保、节约、充分利用自然资源。
(7)在整个转化过程中,CO2最终被转化为碳,反应前后Fe3O4质量会变小。
(8)催化剂的催化效率和甲烷的生成速率随温度的变化关系如图所示。可以发现温度在300-400℃之间,甲烷生成速率加快。
故答案为:(1)ac。
(2)光合作用。
(3)CO2+Ca(OH)2→CaCO3+H2O。
(4)降低;甲烷分解生成的碳附在催化剂表面;二氧化碳。
(5)低;不改变。
(6)环保、节约、充分利用自然资源。
(7)碳;变小。
(8)300-400。